题目内容
【题目】粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙)。某实验小组的同学在粗盐提纯实验中,并把少量可溶性杂质CaCl2,MgCl2一并除去,设计如下实验方案,请回答问题:
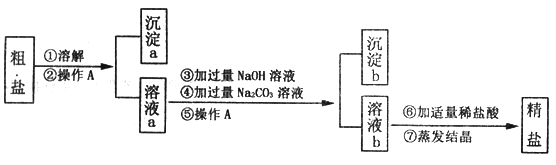
(1)实验操作A的名称是___________________;
(2)写出步骤③中发生反应的主要化学方程式_________________;沉淀b中含有物质____________(填化学式);
(3)实验中某同学对溶液b的成分进行了探究。
【提出问题】溶液b中除了含有水和氯化钠外,还含有哪些物质?
【提出猜想】根据实验①②③④⑤的操作后,作出如下猜想。
猜想一:还含有碳酸钠;
猜想二:还含有氢氧化钠;
猜想三:还含有碳酸钠和氢氧化钠。
【验证猜想】
步骤 | 实验操作 | 实验现象 | 推断 |
1 | 取少量溶液b于试管中,加入过量的氯化钙溶液,振荡,静置 | _______________ | 溶液b中还含有________溶质 |
2 | 取步骤1反应后的混合液过滤后,取滤液少量于试管中加入__________(填指示剂) | _______________ | 溶液b中还含有氢氧化钠 |
【实验结论】经过兴趣小组的实验分析,判断猜想___________是正确的。
【反思与拓展】为了使制得的精盐水只含有水和氯化钠,步骤⑥的作用是除去杂质,请写出其中一个反应的化学方程式:________________。
【答案】 过滤 MgCl2+2NaOH=Mg(OH)2↓+2NaCl Mg(OH)2 CaCO3 产生白色沉淀 溶液b中还含有碳酸钠(或Na2CO3) 取步骤1反应后的混合液过滤后,取滤液少量于试管中加入无色酚酞试液 溶液变红色 三 HCl+NaOH=NaCl+H2O或2HCl+Na2CO3=2NaCl+H2O+CO2↑
【解析】 (1). 过滤 (2).氢氧化钠和氯化镁生成氢氧化镁沉淀和氯化钠,反应方程式为 MgCl2+2NaOH=Mg(OH)2↓+2NaCl (3).碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,所以沉淀中有 Mg(OH)2 和 CaCO3 (4). 碳酸钠和 氯化钙溶液,氢氧化钠和氯化钙不反应,所以产生白色沉淀 证明溶液b中还含有碳酸钠(或Na2CO3) (6).由于步骤1加入过量的氯化钙溶液,所以碳酸钠被除尽, 取步骤1反应后的混合液过滤后,取滤液少量于试管中加入无色酚酞试液 ,溶液变红色 ,说明溶液中还有氢氧化钠. 判断猜想三是正确的。 (9). 为了使制得的精盐水只含有水和氯化钠,步骤⑥的作用是除掉除杂时引入的氢氧化钠和碳酸钠杂质,反应方程式为HCl+NaOH=NaCl+H2O或2HCl+Na2CO3=2NaCl+H2O+CO2↑

 教材全解字词句篇系列答案
教材全解字词句篇系列答案【题目】
(1)用文字表示铁丝在氧气中燃烧的化学反应: 。
(2)探究一:蜡烛燃烧产生火焰的原因是什么?

点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示)。由此可知:蜡烛燃烧产生的火焰是由 (填“固态”或“气态”)物质燃烧形成的。
(3)探究二:物质燃烧产生火焰的根本原因是什么?
【查阅资料】
物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
石蜡 | 50~70 | 300~550 | 约600 |
铁 | 1535 | 2750 | 约1800 |
钠 | 97.8 | 883 | 约1400 |
由上表可知:物质燃烧能否产生火焰与其 (填“熔点”或“沸点”)和燃烧时温度有关。由此推测:钠在燃烧时, (填“有”或“没有”)火焰产生。