题目内容
【题目】归纳是学习化学的重要方法。小明总结出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应),请帮助完成下列空白:

(1)在图中空白方框中可填写指示剂或________(填物质类别);
(2)利用反应⑦制取金属铜,写出该反应的化学方程式________;
(3)通过分析可知酸的化学性质有________条;
(4)写出一个符合反应⑤的化学方程式________________;
(5)验证反应①,可以选择下列________(填字母序号)两种物质进行反应;
A. KNO3 B. CuSO4 C. BaCl2 D. NaOH
(6)碱具有相似的化学性质是因为碱溶液中都含有________(填粒子符号),但是氢氧化钠和氢氧化钙的化学性质又有差异,氢氧化钠溶液不能同碳酸钠溶液反应,而氢氧化钙溶液却能与碳酸钠溶液反应,产生不同现象的原因是________________________________。
【答案】 氧化物 Fe+CuSO4=FeSO4+Cu符合要求即可 5 Fe2O3+6HCl=2FeCl3+3H2O符合要求即可 BD OH- 所含的金属离子不同(每空1分,化学方程式2分)
【解析】(1)酸的溶液能使紫色石蕊变红,碱的溶液能使紫色石蕊变蓝,使无色酚酞变红;碱的溶液能和二氧化碳等非金属氧化物反应生成盐和水;酸能和金属氧化物反应生成盐和水;所以图中空白方框中可填写指示剂或氧化物;在金属活动顺序表中,排在氢前边的金属能和酸发生置换反应生成盐和氢气。金属的位置越靠前,金属的活动性越强。位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。所以活动顺序表中铜前边的金属能将铜从溶液中置换出来;如:Fe+CuSO4=FeSO4+Cu;(3)通过分析可知酸的化学性质有5条;和碱、金属氧化物、某些盐、金属、酸碱指示剂反应;(4)用酸除铁锈是利用了酸和金属氧化物反应生成盐和水如:Fe2O3+6HCl=2FeCl3+3H2O;(5)氢氧化钠和硫酸铜反应生成硫酸钠和氢氧化铜沉淀;(6)溶液的性质是由溶液中的微粒决定的,相同的微粒决定相同的化学性质,碱具有相似的化学性质是因为碱溶液中都含有氢离子;但是氢氧化钠和氢氧化钙的化学性质又有差异,氢氧化钠溶液不能同碳酸钠溶液反应,而氢氧化钙溶液却能与碳酸钠溶液反应,产生不同现象的原因是金属离子不同。

 阅读快车系列答案
阅读快车系列答案【题目】粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙)。某实验小组的同学在粗盐提纯实验中,并把少量可溶性杂质CaCl2,MgCl2一并除去,设计如下实验方案,请回答问题:
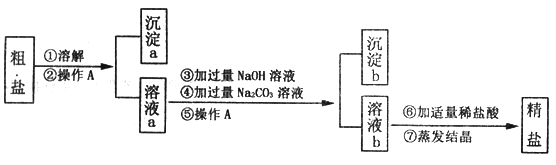
(1)实验操作A的名称是___________________;
(2)写出步骤③中发生反应的主要化学方程式_________________;沉淀b中含有物质____________(填化学式);
(3)实验中某同学对溶液b的成分进行了探究。
【提出问题】溶液b中除了含有水和氯化钠外,还含有哪些物质?
【提出猜想】根据实验①②③④⑤的操作后,作出如下猜想。
猜想一:还含有碳酸钠;
猜想二:还含有氢氧化钠;
猜想三:还含有碳酸钠和氢氧化钠。
【验证猜想】
步骤 | 实验操作 | 实验现象 | 推断 |
1 | 取少量溶液b于试管中,加入过量的氯化钙溶液,振荡,静置 | _______________ | 溶液b中还含有________溶质 |
2 | 取步骤1反应后的混合液过滤后,取滤液少量于试管中加入__________(填指示剂) | _______________ | 溶液b中还含有氢氧化钠 |
【实验结论】经过兴趣小组的实验分析,判断猜想___________是正确的。
【反思与拓展】为了使制得的精盐水只含有水和氯化钠,步骤⑥的作用是除去杂质,请写出其中一个反应的化学方程式:________________。