题目内容
【题目】如图,A、B、C分别是某微粒的结构示意图,回答下列问题:
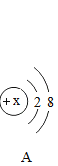
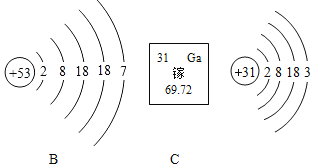
(1)若x=11,则A表示的粒子为_____(用化学用语填空);
(2) B位于元素周期表的第_____周期;
(3)若x=7,请写出A、C元素形成的化合物的化学式_____。
【答案】Na+ 五 GaN
【解析】
(1)质子数为11的是钠元素,若x=11,A粒子中质子数大于核外电子数,则A表示的粒子为钠离子,故填:Na+;
(2)B的原子结构示意图中有5个电子层,位于元素周期表的第五周期;故填:五;
(3)质子数为7的是氮元素,若x=7,则A是得到3个电子而形成的氮离子,显-3价,C粒子的最外层有3个电子,在化学反应中败给易失去最外层的3个电子而显+3价,所以二者组成的化合物氮化镓的化学式为GaN;故填:GaN。

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案【题目】人类的生活和生产都离不开金属,铁是世界产量最高且应用最广泛的金属。
(1)生活中用铁锅作炊具,是利用了铁的____性;
(2)铁制品生锈的主要条件是铁与____直接接触,铁锈的主要成分是____(填化学式);防止铁生锈的方法有____(答一种即可)。
(3)Pb的化合价有+2和+4价,Pb3O4属氧化物,也属于盐,其盐的化学式可表示为Pb2(PbO4),铁的氧化物Fe3O4也属于盐,则其盐的化学式可表示为____;
(4)取某钢样粉末50.0 g(假设只含Fe和C),在氧气流中充分反应,将产生的气体通入足量的澄清石灰水中,得到2.5 g白色沉淀。另取三份不同质量的该钢样粉末分别加入到100.0 g质量分数相同的稀H2SO4中,充分反应后,测得的实验数据如下表所示:
实验序号 | 甲 | 乙 | 丙 |
加入钢样粉末的质量(g) | 10.0 | 20.0 | 40.0 |
生成气体的质量(g) | 0.355 | 0.71 | 1.0 |
①根据表中数据可计算出稀硫酸中H2SO4的质量分数为____;
②若要使实验甲中的剩余硫酸全部消耗完,则至少需要再加入____g钢样粉末。