题目内容
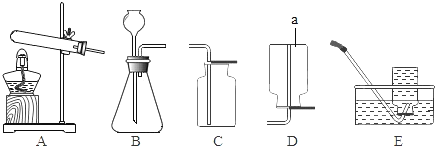
【题目】如图所示为实验室中常见气体制备、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器)。试根据题目要求,回答下列问题:
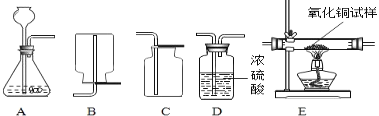
(1)若以H2O2溶液为原料(以MnO2为催化剂)在实验室中制备并收集干燥的氧气.
①所选仪器的连接顺序为________(填写仪器序号字母).
②生成氧气时,仪器A中发生的化学反应方程式是________.
③实验室也可以用排水法收集氧气,其原因是________.
(2)若用锌和稀硫酸反应制取氢气,并用来测定某不纯的氧化铁样品的纯度(杂质为少量单质铁),所选仪器的连接顺序为:A→D1→E→D2→D3.(已知:Fe2O3+3H2=2Fe+3H2O;D1、D2、D3为3个盛有浓硫酸的洗气瓶)
①仪器D1的作用是________.
②充分反应后洗气瓶D2的质量增加了3.6g,则E装置内固体质量减少了________g.
【答案】ADC 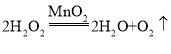 氧气不易溶于水 吸水干燥氢气 3.2g
氧气不易溶于水 吸水干燥氢气 3.2g
【解析】
过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,锌和稀硫酸反应生成硫酸锌和氢气。
(1)①用双氧水制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气;氧气的密度比空气的密度大,不易溶于水,用向上排空气法和排水法收集,在实验室中制备并收集干燥的氧气,氧气和硫酸不反应,可以用浓硫酸干燥,干燥后只能用向上排空气法收集,所选仪器的连接顺序为ADC。
②生成氧气时,仪器A中发生的反应是过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,反应的化学方程式是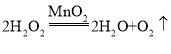 。
。
③实验室也可以用排水法收集氧气,其原因是氧气不易溶于水。
(2)①锌和稀硫酸反应制取氢气,氢气带有水蒸气,故仪器D1的作用是吸水干燥氢气。
②洗气瓶D2的质量增加了3.6g,增加的质量是水的质量,E装置内固体减少的质量为
![]() 。
。

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案【题目】现有一家庭使用纯碱样品,其中含杂质氯化钠(不含其它杂质),为了测定样品中杂质氯化钠的质量分数,李明同学进行了三次实验,实验数据如表:
编号 | 第1次 | 第2次 | 第3次 |
所取固体样品的质量/g | 15 | 12 | 12 |
加入氯化钙溶液的质量/g | 100 | 100 | 150 |
反应后生成沉淀的质量/g | 10 | 10 | 10 |
完成下列计算(计算结果精确到0.1%):
(1)样品中氯化钠的质量分数_____;
(2)恰好完全反应时,反应后所得溶液中氯化钠的质量分数_____.