题目内容
【题目】取一条表面氧化的铝片,加入足量的稀盐酸,充分反应后共收集到1.40 g氢气。将反应后的溶液蒸干,得到66. 75 g氯化铝。
(1)根据化学方程式计算铝片中铝单质的质量。_____________
(2)计算该铝片的氧化程度(计算结果保留到0.1%)。_____________
提示:铝片的氧化程度指被氧化的铝的质量占未氧化时铝片总质量的百分数。
【答案】12.60g。6.7%。
【解析】
(1)由反应产生氢气的质量,根据反应的化学方程式,计算与酸反应的铝的质量;(2)根据氯化铝的质量计算其中铝元素的质量,可得氧化铝中铝元素的质量,进一步计算铝片的氧化程度。
解:(1)设铝片中铝单质的质量为x
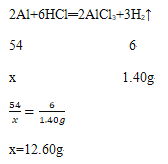
(2)氯化铝中铝元素的质量:66.75g×![]() ×100%=13.50g
×100%=13.50g
氧化铝中铝元素的质量:13.50g-12.60g=0.90g
铝片的氧化程度:![]() ×100%=6.7%
×100%=6.7%
答:(1)铝单质的质量为12.60g。
(2)铝片的氧化程度为6.7%。

 阅读快车系列答案
阅读快车系列答案【题目】设计方案是实验探究的保证,感悟方法是探究的根本目的.某化学学习小组欲对实验室失去标签的三瓶无色溶液A、B、C的成分进行探究,它们可能是NH4Cl溶液、NaOH溶液、Na2CO3溶液中的一种,探究过程如下:
(分析)从组成上看,NH4Cl属于铵盐,含有NH4+,与强碱溶液反应会有氨气产生,NaOH溶液和Na2CO3溶液中因为含有不同阴离子,所以性质不同,据此可鉴别.
(设计方案并实验)
实验操作 | 现象 | 结论 |
(1)小红分别取适量A、B、C三种溶液于三只试管中,再分别加入氢氧化钠溶液微热 | A中产生有刺激性气味的气体,B、C中无气味 | A是NH4Cl溶液. A与氢氧化钠溶液反应的化学方程式:______________. |
(2)小贝分别取适量B、C两种溶液于两只试管中,再分别滴加酚酞溶液 | 酚酞溶液变红 | B、C都是NaOH溶液 |
(3)小明也分别取适量B、C两种溶液于两只试管中,再分别滴加______________. | ______________ | B是Na2CO3溶液 C是NaOH溶液 |
(反思与评价)小组同学讨论后一致认为小贝的结论不正确,理由是______________.
(方法感悟)在检验物质时,要分析物质的组成和______________,据此选择加入适当的试剂,最后根据不同现象得出结论.
(问题处理)几天后,小明才发现取完C后忘了及时盖上瓶塞,若要除去其中杂质,可向其中加入适量的________________________溶液.