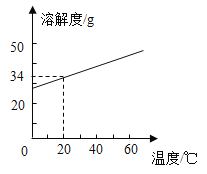
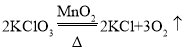题目内容
【题目】某些元素的相关信息如下图所示,请认真分析并回答问题。
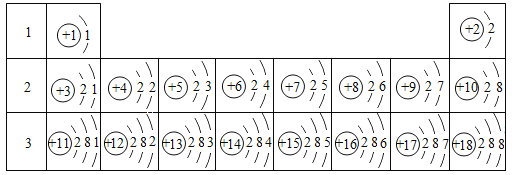
(1)原子序数为7的元素位于元素周期表中第___周期,它属于___(填“金属”或“非金属”)元素;
(2)在化学反应中,原子序数为11的元素的原子容易___(填“得”或“失”)电子,形成离子的符号是____;
(3)根据上表中原子结构示意图分析,氧元素与___(填元素符号)的化学性质相似。
【答案】二 非金属 失 ![]() S
S
【解析】
(1)如图所示原子序数为7的元素位于元素周期表中第二横行,即位于第二周期,该元素是“氮元素”,由元素名称可知为“气”字头,它属于非金属元素;
(2)原子序数为11的元素为Na,如图所示其原子结构示意图中最外层电子数为1,通常情况下,最外层电子数小于4的原子在化学变化中容易失去电子,因此在化学反应中,钠原子容易失电子,形成带1个单位正电荷的钠离子,表示离子所带的电荷数时写在元素或原子团的右上角,数字在前,正负号在后,“1”通常省略不写,则钠离子的符号是![]() ;
;
(3)根据原子结构示意图可知元素原子的最外层电子数相同,元素的化学性质相似,由上表中原子结构示意图可知,氧原子的最外层电子数为6,硫原子的最外层电子数为6,氧元素与S的化学性质相似。

【题目】实验室用碳酸钠溶液与氯化钙溶液反应制取高纯度碳酸钙粉末,烧杯中现有100g碳酸钠溶液,将140g氯化钙溶液分四次加入,充分反应,
注:发生反应的化学方程式为![]()
四次测量所得数据如表所示:
次数 | 累计加入氯化钙溶液的质量/g | 烧杯中溶液的总质量/g |
一 | 40 | 135 |
二 | 80 | 170 |
三 | 120 | 205 |
四 | 140 | 225 |
(1)恰好完全反应时,生成沉淀的总质量为 g。
(2)第四次测量时,所得溶液中的溶质有 (填化学式)。
(3)计算氯化钙溶液的溶质质量分数(写出计算过程,计算结果保留到0.1%)