题目内容
【题目】某兴趣小组制取氧气,并尝试回收部分药品。可能用到的部分装置如图。
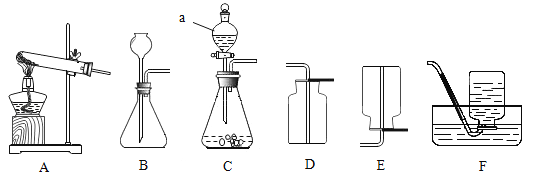
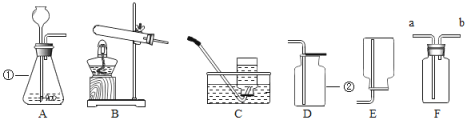
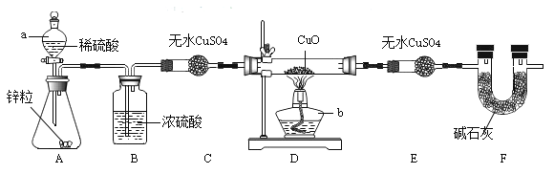
(1)上图中仪器a的名称是_______________。
(2)用双氧水和MnO2制氧气。发生反应的化学方程式为_____,收集氧气的装置可选用_____(填字母)。
(3)加热KClO3固体制氧气(1.5gMnO2作催化剂),并对KClO3完全分解后的残留固体进行分离。(已知反应原理为: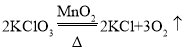 )
)
①发生装置应选用____________(填字母)。
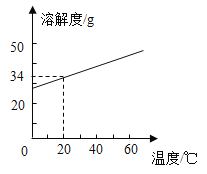
②KCl的溶解度曲线如图所示。将残留固体冷却至室温(20℃),称得其质量为4.8g。欲将KCl全部溶解,至少应加入该温度下蒸馏水的体积约________(填字母)。
a.5 mL
b. 10 mL
c. 20 mL
d. 30 mL
③对溶解所得混合物进行过滤,滤渣经处理得MnO2。从滤液中获得KC1晶体的最佳方法是___。
【答案】分液漏斗 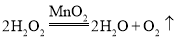 D或F A b 蒸发结晶
D或F A b 蒸发结晶
【解析】
(1)上图中仪器a的名称是分液漏斗,一般用于添加液体药品。
(2)用双氧水和MnO2制氧气。发生反应的化学方程式为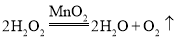 ,由于氧气的密度比空气大,且不易溶于水,收集氧气的方法可用向上排空气法或排水法,故装置可选用D或F。
,由于氧气的密度比空气大,且不易溶于水,收集氧气的方法可用向上排空气法或排水法,故装置可选用D或F。
(3)
①加热KClO3固体制氧气,根据反应原理,发生装置应选用固体加热型,故选A。
②二氧化锰是该反应的催化剂,在反应前后质量不变,根据题意,反应后KCl的质量=4.8g-1.5g=3.3g,根据溶解度曲线,20℃时氯化钾的溶解度为34g,表示该温度下100g水中溶解34g氯化钾达到饱和状态,欲将3.3gKCl全部溶解,至少应加入该温度下蒸馏水的质量=![]() ,约10 mL,故选b。
,约10 mL,故选b。
③根据溶解度曲线可知,氯化钾受温度的影响变化较小,从滤液中获得KC1晶体的最佳方法是蒸发结晶。

【题目】新能源页岩气,正在冲击传统能源体系。据报道,我国页岩气储量排名世界第一,合理开采将有利于改善我国的能源结构,川南页岩气田分布在泸州等地。页岩气是藏身于地下3000多米的页岩层裂缝中的天然气,在此高压环境中,还有部分溶解于裂缝中存在的少量石油里。目前,开采页岩气时从地表钻井到页岩层,向地下压入大量水和沙,使页岩气所在的地层产生缝隙,因压强降低,页岩气将从其藏匿处逸岀。这些水和沙将被抽回地面,形成返排液。
回答下列问题:
(1)页岩气中主要成分的化学式是_____,溶解在石油中的页岩气逸出的原因_____。
(2)页岩气中还可能含有乙烷(C2H6),写出乙烷完全燃烧的化学方程式_____。
(3)返排液是油、水溶液和沙组成的混合物。从返排液中分离出沙的实验操作名称是____;下表是某返排液中水溶液的主要成分及其含量,质量分数最高的金属离子是____,这些离子的含量远高于自然水。
离子 | K+ | Ca2+ | Mg2+ | HCO | Cl- |
含量(mg/L) | 310 | 491 | 129 | 470 | 26.1 |
(4)结合上文分析简答:开采时可能产生的主要环保问题是___(写一点),你的解决建议是_____。
【题目】碳酸钠俗称纯碱或苏打,在生活、生产和实验硏究中均有广泛应用。
(配制溶液)配制溶质质量分数分別为1%、2%和4%的Na2CO3溶液
(1)若配制50g溶质质量分数为4%的Na2CO3溶液,下列操作正确的是______(填字母)。
a.用托盘天平称取2gNa2CO3固体
b.选用50mL量筒量取所需体积的水
c.选用带玻璃塞的广口试剂瓶,将配好的溶液装瓶并贴标签
(2)分别测定25℃时,上述3种溶液的pH,记录数据如下:
实验编号 | Ⅰ | Ⅱ | Ⅲ |
溶质质量分数 | 1% | 2% | 4% |
溶液pH | 11.62 | 11.76 | 11.90 |
分析I、Ⅱ、Ⅲ三组数据可得出的结论是________。
(制备物质)用Na2CO3溶液和FeSO4溶液发生复分解反应制备FeCO3
(已知溶液pH大于8.8时,Fe2+完全生成Fe(OH)2沉淀)
(3)在烧杯中制备FeCO3沉淀时,应选用的加料方式是______(填字母)。
a.将FeSO4溶液与Na2CO3溶液同时加入到烧杯中
b.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的烧杯中
c.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的烧杯中
(4)潮湿的FeCO3固体置于空气中易变质,反应如下:![]() ,则X的化学式为___________。
,则X的化学式为___________。
(标定浓度)标定待测盐酸的溶质质量分数
(5)将Na2CO3固体在270℃干燥至恒重,准确称取0.212g无水Na2CO3于锥形瓶中,加入50mL蒸馏水溶解,滴入待测盐酸,当两者恰好完全反应时,消耗盐酸的体积为20.00mL(该盐酸的密度近似等于1g·mL-1,反应中Na2CO3所含的碳元素全部转化为CO2)。
①列式计算待测盐酸的溶质质量分数_____(结果用百分数表示,保留两位小数)。
②若上述测定过程中Na2CO3固体未经充分干燥,则测出盐酸的溶质质量分数将_____(填“偏大”、“偏小”或“无影响”)。
【题目】阅读下面科普短文
人类目前所消耗的能量主要来自于化石能源,化石燃料是由古代生物的遗骸经过一系列复杂的变化形成的。化石燃料燃烧时产生的一些物质。如一氧化碳、二氧化硫、未燃烧的碳氢化合物及碳粒、氮的氧化物等排放到空气中,会对空气造成污染。二氧化硫和氮的氧化物在空气中发生反应后的生成物溶于雨水,会形成酸雨。天然气是一种重要的化石燃料,主要含有碳和氢组成的碳氢化合物,其中最主要的是甲烷。不同地区天然气的主要成分有较大差异,我国部分地区天然气的主要成分如下表所示:
CH4 | C2H6 | C3H8 | CO2 | N2 | H2S | |
西南油田 | 93.1098 | 3.8914 | 0.1447 | 1.3092 | 0.5341 | — |
华北油田 | 80.8430 | 9.7326 | 5.7538 | 0.9288 | 0.3200 | — |
陕甘宁油田 | 95.9500 | 0.9675 | 0.1367 | 1.5038 | — | 0.0002 |
注:1.表中数据均表示体积分数。2.“—”表示含量过低,当前所用仪器未检出。
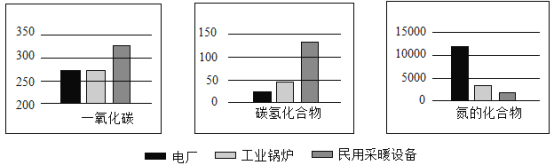
天然气的用途非常广泛,可作为燃料直接使用。天然气在不同设备中燃烧产生的污染物的含量也不尽相同,几种常见设备中天然气燃烧时产生的污染物(kg/Mm3)如图所示:
现代社会对能量的需要量越来越大,化石燃料日渐枯竭,人们正在利用和开发其他能源。这些能源的利用,可以部分解决化石燃料面临耗尽的问题,并在一定程度上减少了对耗尽的污染。
依据文章内容,回答下列问题。
(1)化石燃料是_____________(填“可再生”或“不可再生”)能源,主要包括______、_______和天然气。
(2)________油田的天然气中丙烷(C3H8)含量最高,写出丙烷完全燃烧的化学方程式____________。
(3)氮的氧化物排放到空气中可形成酸雨,酸雨是pH<_______的降雨。
(4)在电厂、工业锅炉和民用采暖设备中天然气燃烧效率最低的是___________。
A电厂 B工业锅炉 C民用采暖设备
(5)甲烷除用作燃料外,在工业上也有这样的用途。科学家探索出在一定条件下用甲烷为原料制成了金刚石,写出该反应的化学方程式______________。