题目内容
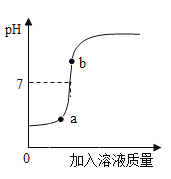
【题目】已知A、E、F是单质,B、C、D是化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成。其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如右图所示。
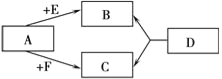
(1)则A、F的化学式为A: ,F:
(2)请你写出下列变化的化学方程式:
A+E→B
D→B+C
【答案】(1)A:O2 F:C
(2)O2+2H2![]() 2H2O H2CO3
2H2O H2CO3![]() H2O+CO2↑
H2O+CO2↑
【解析】
试题由于B是相对分子质量最小的氧化物,所以可以确定B是水;根据“C、D是化合物,它们分别是由碳、氢、氧三种元素中几种组成,D物质很不稳定,容易分解生成B水和C”,可以确定D是碳酸,则C为二氧化碳;再根据“E、F是单质,均可以与单质A反应,分别生成B水和C二氧化碳”,所以可确定A是氧气,E是氢气,F是碳。则A+E→B的化学方程式为O2+2H2![]() 2H2O,D→B+C的化学方程式为H2CO3
2H2O,D→B+C的化学方程式为H2CO3![]() H2O+CO2↑。
H2O+CO2↑。

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目