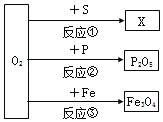
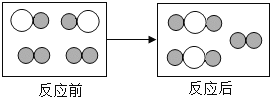
��Ŀ����
����Ŀ��ijУ��ȤС����ʵ�����������ȡ������ʵ�顣����ȡ����غͶ������̵Ļ���ﹲ3.0g������Թ��м���,���ڲ�ͬʱ�̲ⶨ�Թ���ʣ��������ʵ�����(���±�):�����������ݣ�����������⣺
��Ӧʱ��/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
ʣ���������g | 2.55 | 2.25 | 2.10 | 2.04 | 2.04 |
��1����ȫ��Ӧ����������������Ϊ_____g
��2��������������Ԫ�ص���������_____
��3��ԭ�����������ص����������Ƕ���_____?(��ȷ��0.1%)
���𰸡�0.96 63.2% 81.7%
��������
��1���ɱ��е����������֪����Ӧ��2.5����ʱ������Ѿ���ȫ��Ӧ�����������غ㶨�ɣ���Ӧǰ�����ʵ������ܺ���ȣ�����������������=��Ӧǰ���ʵ�����-��Ӧ��ʣ����������=3.0g-2.04g=0.96g��
��2��������������Ԫ�ص�����������![]() ��
��
��3����ԭ�����������ص�����Ϊx��
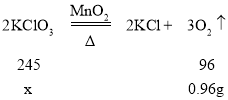
![]()
��ã�x=2.45g
ԭ�����������ص�����������![]() ��
��

����Ŀ��ͨ��������ˮ�ķе���100�棬����ѹǿ����ˮ�ķе�������ߡ���ͼ���о�ˮ�е�����ѹ�仯��ʵ�顣�ر�ֹˮ�У����Ӻ�װ�ã� �ٽ�Һ�� A�����Թܢ��У����ӣ��Թܢ��ڵ�ˮ���̷��ڡ���Һ��A������B����Ͽ�����
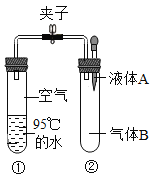
��� | A | B | C | D |
Һ��A | ˮ | ˮ | ʯ��ˮ | ˮ |
����B | ���� | ���� | ������̼ | ���� |
A.AB.BC.CD.D