题目内容
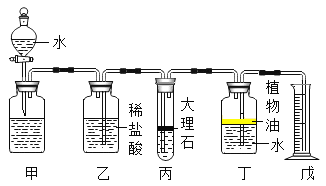
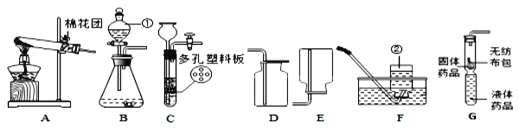
【题目】下图为化学实验装置,回答有关问题。

(1)写出图中标有字母的仪器的名称:b______________。
(2)实验室用氯酸钾制取纯净的氧气应选择的装置是___________,反应的化学方程式是___________。制得的氧气用来做如图2所示的实验,发现G中铁丝燃烧而 H 中铁丝不燃烧,其原因是____________。写出G中反应的化学方程式______________。
(3)实验室制取二氧化碳若用装置 E 收集二氧化碳,则气体应从填______________端进入,其验满的方法是____________或______________。若要检验二氧化碳气体,可将装置 B 和装置D用胶皮管连接,其反应的化学方程式是___________,若D 中只见有气泡产生,未见其它现象,则可能原因是_______________。
(4)实验室常用装置C代替装置 B 制取气体,装置 C 的优点是_____________。检查装置B的气密性的方法是______________。
【答案】锥形瓶 AF 2KClO3![]() 2KCl + 3O2 ↑ 收集的氧气不纯(合理即可) 3Fe + 2O2
2KCl + 3O2 ↑ 收集的氧气不纯(合理即可) 3Fe + 2O2![]() Fe3O4 ① 是在②端处放燃着的木条,若熄灭,则集满 在②端处放涂有澄清石灰水的玻璃片,若玻璃片变得模糊,则集满 CO2 +Ca(OH)2 =CaCO3↓+ H2O 可能是盐酸浓度太大,挥发出的氯化氢气体与石灰水反应,也有可能是石灰水变质 可以随时控制反应的发生与停止 在导气管装上软管,用弹簧夹夹住软管,从长颈漏斗处加入适量的水,若长颈漏斗中形成稳定的水柱则气密性良好
Fe3O4 ① 是在②端处放燃着的木条,若熄灭,则集满 在②端处放涂有澄清石灰水的玻璃片,若玻璃片变得模糊,则集满 CO2 +Ca(OH)2 =CaCO3↓+ H2O 可能是盐酸浓度太大,挥发出的氯化氢气体与石灰水反应,也有可能是石灰水变质 可以随时控制反应的发生与停止 在导气管装上软管,用弹簧夹夹住软管,从长颈漏斗处加入适量的水,若长颈漏斗中形成稳定的水柱则气密性良好
【解析】
(1)图中标有字母b的仪器的名称是锥形瓶。
(2)用氯酸钾制取氧气,反应物是固体,反应条件是加热,属于固体加热型,氧气密度大于空气,不易溶于水,可用向上排空气法收集或排水法收集,用排水法收集的气体较为纯净,若要制取并收集一瓶比较纯净的氧气,应选用的装置是AF;氯酸钾在二氧化锰催化作用下加热分解生在成氯化钾和氧气,反应的化学方程式是2KClO3![]() 2KCl + 3O2 ↑。制得的氧气用来做如图2所示的实验,发现 G 中铁丝燃烧而 H 中铁丝不燃烧,其 原因是收集的氧气不纯。铁和氧气在点燃的条件下生成四氧化三铁,G 中反应的化学方程式为:3Fe + 2O2
2KCl + 3O2 ↑。制得的氧气用来做如图2所示的实验,发现 G 中铁丝燃烧而 H 中铁丝不燃烧,其 原因是收集的氧气不纯。铁和氧气在点燃的条件下生成四氧化三铁,G 中反应的化学方程式为:3Fe + 2O2 ![]() Fe3O4。
Fe3O4。
(3)实验室制取二氧化碳若用装置E收集二氧化碳,二氧化碳密度大于空气,则气体应从填①端进入;二氧化碳不能燃烧也不能支持燃烧,能使燃着的木条熄灭。其验满的方法是在②端处放燃着的木条,若熄灭,则集满或在②端处放涂有澄清石灰水的玻璃片,若玻璃片变模糊,则集满。二氧化碳能使澄清石灰水变浑浊,常用于检验二氧化碳。若要检验二氧化碳气体,可将装置B和装置D用胶皮管连接,其反应的化学方程式是CO2 +Ca(OH)2 =CaCO3↓+ H2O,若 D 中只见有气泡产生,未见其它现象,则可能原因是可能是盐酸浓度太大,挥发出的氯化氢气体与石灰水反应,也有可能是石灰水变质。
(4)在装置C中,固体药品放在多孔隔板上,液体药品从长颈漏斗中加入。反应后关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行。实验室常用装置C代替装置B制取气体,装置C的优点是可以随时控制反应的发生与停止。检查装置 B 的气 密性的方法是在导气管装上软管,用弹簧夹夹住软管,从长颈漏斗处加入适量的水,若长颈漏斗中形成稳定的水柱则气密性良好。

【题目】某校兴趣小组在实验室中完成制取氧气的实验。他们取氯酸钾和二氧化锰的混合物共3.0g放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):分析表中数据,完成下列问题:
反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
剩余固体质量g | 2.55 | 2.25 | 2.10 | 2.04 | 2.04 |
(1)完全反应后,生成氧气的质量为_____g
(2)二氧化锰中锰元素的质量分数_____
(3)原混合物中氯酸钾的质量分数是多少_____?(精确到0.1%)