题目内容
甲、乙两位同学分别利用下图装置研究可燃物的燃烧条件。
已知:白磷的着火点为 40℃,红磷的着火点为 240℃。
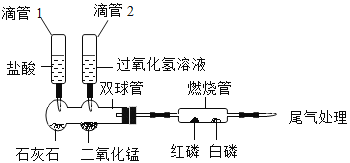
甲同学:挤压滴管 1,一段时间后,加热燃烧管至 260℃以上,白磷和红磷均不燃烧。
乙同学:微热燃烧管至 a℃,一段时间后,挤压滴管 2,白磷迅速燃烧,而红磷不燃烧。
(1)甲同学挤压滴管 1 后有二氧化碳生成,请写出该反应的化学方程式:_______。
(2)从燃烧条件角度分析,甲同学实验中白磷和红磷均不燃烧的原因是_______。
(3)乙同学实验能证明可燃物燃烧需要温度达到着火点,则 a 应选择_______(填字母序号)。
A25℃ B80℃ C260℃
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案化学与生活、生产及可持续发展密切相关,下列说法正确的是( )
A性质与用途 | B环保与能源 |
①干冰升华吸热,可用于保鲜食品、人工降雨 ②红磷燃烧产生大量白色烟雾,可用作烟雾弹、发令枪 ③浓硫酸不慎沾皮肤上,立即用 NaOH 溶液清洗 | ①推广使用的乙醇汽油是纯净物 ②为减少“白色污染”,使用可降解塑料 ③冬天用煤炉取暖为防止热量散失,需紧闭门窗,可在屋内放一盆水防止煤气中毒 |
C健康与安全 | D化学与生活 |
①人体缺维生素 A 会引起夜盲症 ②误食重金属盐中毒后,立即服用鸡蛋清或牛奶解毒 ③用甲醛溶液浸泡水产品,对人体健康会造成危害 | ①用工业酒精可以勾兑饮用酒 ②用活性炭可对水进行杀菌消毒 ③用钢丝球除去铝壶表面污渍 |
A.A B.B C.C D.D
请从 A 或B 两题中任选一个作答,若两题均作答,按 A 计分。
在一定条件下,Mg 和 MgH2的相互转化可以实现氢气的储存和释放。其工作原理如图。
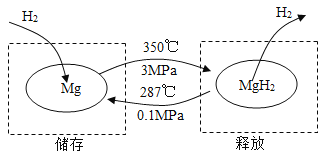
A | B |
(1)氢气储存时发生反应的化学方程式为_______。 (2)氢气很容易逃逸,若氢气存储效率为 10%,储存 1 kg 氢气,至少需要 Mg 的质量为_______ kg。 | (1)氢气释放时发生反应的化学方程式 为_______。 (2)理论上,52 kg MgH2最多能释放氢气的质量为_______ kg。 |
已知 KNO3的溶解度如下表所示,下列说法不正确的是
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
A.在 10℃-70℃之间,随着温度的升高,KNO3的溶解度增大
B.20℃时,向 100 g 水中加入 35 g KNO3,充分搅拌,所得溶液质量为 131.6 g
C.将 70℃时不饱和的 KNO3溶液降低温度,有可能转化为饱和溶液
D.50℃时,饱和 KNO3溶液中溶质的质量分数为 85.5%
生产、生活和科技发展离不开化学。请回答下列问题:
(1)端午节是中国传统节日,吃粽子已成传统风俗。在制作粽子的原料中,糯米所富含的营养素是_____________。
(2)在燃气中加入少量有特殊气味的乙硫醇(C2H5SH),可在燃气泄漏时及时发现,其燃烧的化学方程式为2C2H5SH+9O2 4CO2+2X+6H2O,则X的化学式为_______。
4CO2+2X+6H2O,则X的化学式为_______。
(3)下表列出了家庭中一些常用物品的pH:
物品 | 食醋 | 牙膏 | 食盐溶液 | 肥皂水 |
pH | 3 | 9 | 7 | 10 |
黄蜂的刺是碱性的,若你被黄蜂刺了,应用上述物质中的_________ 涂在皮肤上。



 排水法收集氧气
排水法收集氧气 探究液体压强的特点
探究液体压强的特点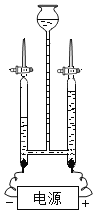 探究水的组成
探究水的组成 探究流体压强与流速的关系
探究流体压强与流速的关系