��Ŀ����
����Ŀ��ʵ������ȡ����ʱ��Ҫ��һЩװ����ͼ��ʾ����ش��������⡣

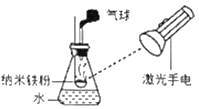
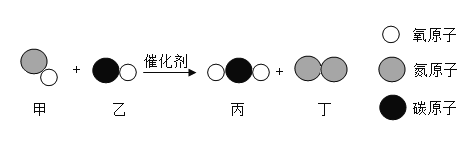
��1��д��������ŵ��������ƣ���_____��
��2��ʵ������ʯ��ʯ��ϡ������ȡ������̼���÷�Ӧ�Ļ�ѧ����ʽΪ_____��ϡ���ỹ�������������⣬д���漰�ķ�Ӧ����ʽ_____��
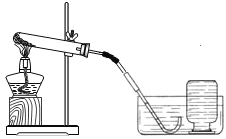
��3��װ��A�ø��������������������һ��Ķ���_____��Fװ����Ũ���������ˮ�ԣ��ɸ���������ϡ���������_____�ˣ�������ң�ͨ�롣
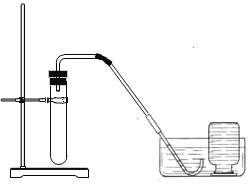
��4����ȡ���ռ����� �Ķ�����̼��ѡ�õ�װ��_____������ţ���
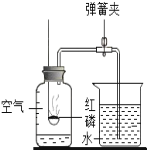
��5��ij��ȤС���ͬѧ����B��G��Hװ�ý���ʵ�顣��ʵ��ʱGװ��������ȼ�ո����ң�Hװ������Һ����ǣ������Gװ�õ�������_____��Hװ���з�Ӧ�Ļ�ѧ����ʽΪ_____��
��6��ͼ1��̽��������ˮ��ȼ�յ�ʵ��װ�á���װ�õIJ���֮���У���ͨ������ʱ�������ױ���ɢ�������������Ӵ�������ɢ��������������ɿ�����Ⱦ�� ͼ2��̽��������ˮ��ȼ�յĸĽ�ʵ��װ�ã���A��B��C��������ɡ��������Ķ��������ݲ��ش��й����⣺�����Ͽ�����������������CO2��SO2��SiO2��P2O5�������

�����������м���1ҩ�������̣���ע��������Լ40mL5%�Ĺ���������Һ��Ȼ��ע��������ͷ������Ƥ���С�
���ڹ��ƿ�м�������������Һ�������ϲ�������˫��������������������Һ��Ŀ����_____��
��ȡһ���̶���С�İ�����С�Թ��У��ټ�������Լ80����ˮ����ˮ�ĸ߶���С�Թܸ߶ȵĶ���֮һΪ�ˣ����Ű����Թܱ���ҪС����ԭ����_____��
���������ƶ�ע�������������з�����Ӧ�Ļ�ѧ����ʽΪ_____��װ��BС�Թ��й۲쵽������Ϊ���������ݲ�������_____��
V��P2O5����Ԫ�صĻ��ϼ�Ϊ_____��
���𰸡��ƾ��� CaCO3+2HCl��CaCl2+H2O+CO2���� Fe2O3+6HCl�T2FeCl3+3H2O�� ���Թܿڷ�һ������ �� BFE ������ CO2+Ca��OH��2��CaCO3��+H2O�� ������ɢ�����������ף����ٻ��� �������������Ӵ� 2H2O2![]() 2H2O+O2���� ����ȼ�գ������������� +5
2H2O+O2���� ����ȼ�գ������������� +5
��������
��1���������Ǿƾ��ƣ�����ƾ��ƣ�
��2��ʯ��ʯ����Ҫ�ɷ���̼��ƣ�̼��������ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼���������Ҫ�ɷ����������������������ᷴӦ�����Ȼ�����ˮ�����CaCO3+2HCl��CaCl2+H2O+CO2����Fe2O3+6HCl�T2FeCl3+3H2O��
��3��ʵ�����ø��������ȡ����ʱ����Ҫ���Թܿڷ�һ��������ֹ������ط�ĩ���뵼�ܣ���������ʱӦ�ó����̳����������������ͨ�룻������Թܿڷ�һ��������
��4����ʯ��ʯ��ϡ������ȡ������̼�����ڹ�Һ�����ͣ�����Ӧ��ѡ��Bװ������ȡ������̼���壻������̼�ܶȱȿ�����������ˮ������Ӧ��ѡ��Eװ�����ռ�������̼��Ũ���������ˮ�ԣ��ɽ�������̼ͨ��ʢ��Ũ�����װ��E�Զ�����̼���и�����BFE��
��5��ʵ��ʱGװ��������ȼ�ո����ң�˵��Bװ�������������������������ڶ������̵Ĵ������·ֽ�����ˮ��������ʯ��ȼ�����ɵĶ�����̼�����������Ʒ�Ӧ����̼��Ƴ�����ˮ�����������CO2+Ca��OH��2��CaCO3��+H2O��
��6��������������������CO2��SO2��SiO2��P2O5�ȣ�����Ӧ�������ڹ��ƿ�м�������������Һ�������ϲ�������˫��������������������Һ��Ŀ����������ɢ�����������ף����ٻ�����Ⱦ�����������ɢ�����������ף����ٻ�����
���Թܵ������������������ĽӴ����������װ�����Թܱ���ҪС����ԭ���ǰ������������Ӵ�������������������Ӵ���
�������������ڶ������̵Ĵ�����������ˮ����������ѧ����ʽΪ��2H2O2![]() 2H2O+O2�������������ڵ�ȼ���������������������ף�����װ��BС�Թ��й۲쵽������Ϊ���������ݲ������ڰ���ȼ�գ������������̡����2H2O2
2H2O+O2�������������ڵ�ȼ���������������������ף�����װ��BС�Թ��й۲쵽������Ϊ���������ݲ������ڰ���ȼ�գ������������̡����2H2O2![]() 2H2O+O2��������ȼ�գ������������̣�
2H2O+O2��������ȼ�գ������������̣�
V���ڻ������У���Ԫ���ԩ�2�ۣ��ɻ������и�Ԫ���������ϼ۵Ĵ�����Ϊ��ԭ���֪��P2O5����Ԫ�صĻ��ϼ�Ϊ+5�����+5��

����Ŀ����ѧ��ȤС��Ϊ��֤�����غ㶨�ɣ�����þ���ڿ�����ȼ�յ�ʵ�飨��ͼ1����ͬѧ�ǹ۲쵽þ���ڿ����о���ȼ�գ�����ҫ�۵�ǿ�⣬�����Ĵ������������������У������ʯ�����ϵõ�һЩ��ɫ���塣
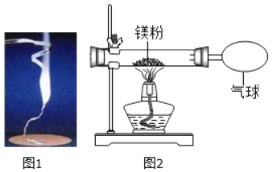
��1��ͨ���������֣���ʯ�������ռ������������С��þ��������������Ϊ��������ʵ������ԭ�������_____��
��2�����ۺ�ͬѧ�ǰ���ͼװ�øĽ�ʵ�飬��֤�������غ㶨�ɣ������ֲ�������������ɫ���塣
��������⣩��ɫ������ʲô��
���������ϣ�������þΪ��ɫ���壺��þ���뵪�����ҷ�Ӧ���ɻ�ɫ�ĵ���þ��Mg3N2�����壻������þ����ˮ���ҷ�Ӧ������������������ʹʪ��ĺ�ɫʯ����ֽ������
���������룩��ɫ������Mg3N2
��ʵ��̽���������ʵ�飬��֤���룺
ʵ����� | ʵ������ | ʵ����� |
_____ | _____ | ��ɫ������Mg3N2 |
����˼�뽻����
������þ�е�Ԫ�صĻ��ϼ���_____��
��������N2�ĺ���Զ����O2�ĺ���������þ���ڿ�����ȼ�ղ���MgOȴԶ����Mg3N2�������Ľ�����_____��
�����㣺36gþ���ڿ�������ȫȼ�գ����ù���������þ����������_____�ˡ���д��������̣�
����Ŀ��С���ι�ij�����ʱ������ķ���ũ�������������һ�ֵ���ɫ���������������ƣ�������������еĺ�������
С����ѧ��������ʵ�����Ʒ�����������ɷ��ù���������ȡ������
��������⣩�������ƿɷ�������ȡ����?
���������ϣ������������£��������ƣ�CaO2���������ȶ�����300��ʱ�ֽ�������������Ҫ��;������������ɱ�����ȡ�
����������֤��
��1��С������������ʾ�����ȹ������ƿ���ȡ������
ʵ��װ�� | ʵ����Ҫ���� |
| �����װ�������ԡ��������£��Ƚ���������Һ���£����ֽ����Թܣ��۲쵽________���ɿ��ֺ��ܿ���Һ�������� |
ʵ����ۣ����ȹ������ƿ���ȡ������
��2��С�����뵽ũ���ù���������������еĺ����������������.
������������������ˮ��Ӧ����ȡ������
ʵ��װ�� | ʵ����Ҫ���� |
| �����װ�������ԡ� |
ʵ����ۣ������ù���������ˮ��Ӧ��ȡ������
�����뷴˼��
��Ȼû�п����ռ����������������ɴ�ʵ������С���Ƶ���ũ���ù�������������������Ҫԭ���� ��
��3��С��ϣ���Դ�ʵ����иĽ���ʹ�÷�Ӧ�ӿ죬���ܰ������������
��ĺ������飺 ��
��Щ�����Ƿ���У������һ��ͨ��ʵ����֤��