题目内容
【题目】结合下列图示装置,回答有关问题:

(1)写出标号①仪器的名称: 。
(2)实验室用装置A制取氧气,其反应的化学方程式 ,若用排水法收集氧气,要把集满氧气的集气瓶转移到桌面上的具体操作是 。
(3)实验室常用 和稀盐酸反应制取二氧化碳,其反应的化学方程式是 ,生成的二氧化碳中常含有少量 气体杂质,为获得纯净的二氧化碳气体,导管口连接的正确顺序是:
a→( )→( )→( )→( )→b
【答案】(1)集气瓶
(2)2H2O2 MnO2 2H2O+ O2↑ 在水中用玻璃片的磨砂面盖住瓶口,取出后正放于桌面
(3)大理石 CaCO3+2HCl==CaCl2+H2O+CO2↑ 水蒸气、氯化氢 f→g→d→e
【解析】
试题分析:(1)常见仪器的识记:集气瓶
(2)气体发生装置的选择依据:反应物的状态和反应条件,A装置适用于固体和液体在常温条件下反应,故实验室用装置A制取氧气,其反应的化学方程式:2H2O2 MnO2 2H2O+ O2↑;若用排水法收集氧气,要把集满氧气的集气瓶转移到桌面上的具体操作是:在水中用玻璃片的磨砂面盖住瓶口,取出后正放于桌面
(3)实验室制取二氧化碳是用大理石和稀盐酸;反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;由于盐酸具有挥发性,故生成的二氧化碳中常含有少量水蒸气、氯化氢气体杂质;为获得纯净的二氧化碳气体,应将这两种气体杂质除去,但应先除去氯化氢,再除水蒸气,故导管口连接的正确顺序是: f→g→d→e

 智能训练练测考系列答案
智能训练练测考系列答案【题目】(11分)实验室里有一瓶长期暴露在空气中的氢氧化钠固体,某化学兴趣小组对其进行了如下探究。
(1)确定固体的成分。
【提出猜想】猜想Ⅰ:固体中只含碳酸钠;
猜想Ⅱ:固体中只含氢氧化钠;
猜想Ⅲ:固体中含有 。
【进行实验】
实验步骤 | 实验现象 | 实验结论 |
①取少量固体溶于水,加入 ; | 产生白色沉淀 | 猜想Ⅲ成立 |
②将上述反应后的混合液过滤,取少量滤液,加入 。 |
(2)测定固体中碳酸钠的质量分数。
【查阅资料】二氧化碳几乎不溶于饱和碳酸氢钠溶液中。
【进行实验】取2g固体,在25℃、101kPa下用如图所示装置进行实验,步骤如下:

①连接好装置并检查气密性;
②装入药品,通过分液漏斗滴加足量稀硫酸后,关闭分液漏斗活塞;
③充分反应后,恢复至25℃、101kPa,量筒中液体的体积为220mL。
【实验分析】
①装置B中的饱和碳酸氢钠溶液不能用水代替,原因是 。
②充分反应后,装置A中残留的的二氧化碳对实验结果是否有明显影响? (选填“有”或“没有”)。
③已知在25℃、101kPa下二氧化碳的密度为1.8g/L,则固体中碳酸钠的质量分数为 (结果保留至0.1%)。
(3)除去固体中的碳酸钠。
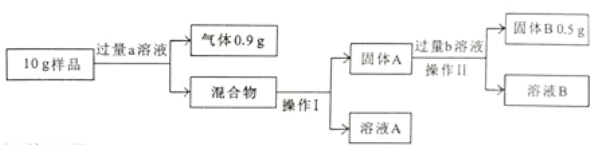
【进行实验】实验流程如下图:
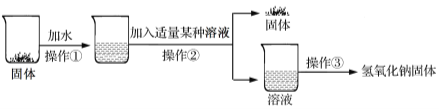
【实验分析】该流程中发生反应的化学方程式为 。
操作①、②、③均需用到的一种仪器是 。