题目内容
【题目】硅晶体广泛应用于电子工业的各个领域,工业上常用焦炭在高温下还原二氧化硅固体初步制得,主要反应为:SiO2+2C![]() Si+2CO↑,求:
Si+2CO↑,求:
(1)二氧化硅中硅元素的质量分数_________;
(2)要生产含硅质量分数为90%的粗硅2.8吨,计算至少需要焦炭______吨?
【答案】46.7% 2.16t
【解析】
(1)根据二氧化硅的化学式可知二氧化硅的相对分子质量=28+16×2=60,硅元素的质量分数为![]() ×100%≈46.7%,故填46.7%;
×100%≈46.7%,故填46.7%;
(2)已知生成物质量,根据化学方程式进行计算,解:设需要焦炭的质量是x,
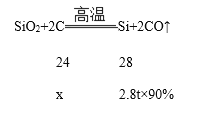
![]() =
=![]() 解得x=2.16t,故填2.16t;写出答:(1)二氧化硅中硅元素的质量分数为46.7%,(2)要生产含硅质量分数为90%的粗硅2.8吨,至少需要焦炭2.16t。
解得x=2.16t,故填2.16t;写出答:(1)二氧化硅中硅元素的质量分数为46.7%,(2)要生产含硅质量分数为90%的粗硅2.8吨,至少需要焦炭2.16t。

 小题狂做系列答案
小题狂做系列答案【题目】下列反应中,属于置换反应的是
A. 2Al2O3![]() 4Al+3O2↑ B. C2H5OH+302
4Al+3O2↑ B. C2H5OH+302![]() 2CO2+3H20
2CO2+3H20
C. 2Mg+CO2![]() 2MgO+C D. AgNO3+NaCl=NaNO3+AgCl↓
2MgO+C D. AgNO3+NaCl=NaNO3+AgCl↓
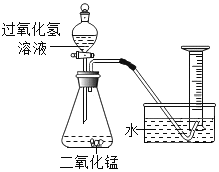
【题目】过氧化氢在生产生活中有广泛应用。实验小组对过氧化氢的某些性质进行研究。
Ⅰ.不稳定性
(1)如图所示进行实验,过氧化氢分解的化学方程式为______,产生3.2gO2时分解的过氧化氢的质量为______g。
(2)能用排水法收集O2的原因是______。
(3)探究温度对过氧化氢分解速率的影响
同学们进行了如下的实验,实验数据如下表:
实验序号 | ① | ② | ③ |
H2O2溶液的浓度% | 30 | 30 | 30 |
H2O2溶液的体积/mL | 6 | 6 | 6 |
温度/℃ | 20 | 35 | 55 |
MnO2的用量/g | 0 | 0 | 0 |
收集O2的体积/mL | 0 | 1.9 | 7.8 |
反应时间 | 40min | 40min | 40min |
由此得出的结论是______。
Ⅱ.腐蚀性
(査阅资料)H2O2溶液有腐蚀性。
(进行实验)
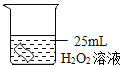
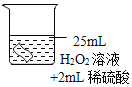
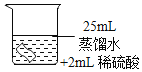
将铜片分别浸泡在3种溶液中进行实验,如下表。
编号 | ① | ② | ③ |
实验 |
|
|
|
一段时间后的现象 | 无明显变化 | 溶液变蓝,缓慢产生细小气泡 | 无明显变化 |
(解释与结论)
(4)实验①的作用是______。
(5)铜片被腐蚀的反应如下,补全该反应的化学方程式:Cu+H2O2+H2SO4=CuSO4+______。
(反思交流)
(6)某同学提出,实验②中,除发生(5)的反应外。还发生了一个反应导致有细小气泡产生,该反应的反应物为______。