1.[2008珠海一模]已知A、B、C、D和E五种分子所含原子的数目依次为1、2、3、4和6,且都含有18个电子,又知B、C和D是由两种元素的原子组成,且D分子中两种原子个数比为1:1。
请回答:
(1) 组成A分子的原子的核外电子排布式是 ;
(2) B和C的分子式分别是 和 ;C分子的立体结构呈 形,该分子属于 分子(填“极性”或“非极性”);
(3) 向D的稀溶液中加入少量氯化铁溶液现象是 ,该反应的化学方程式为
(4) 若将1molE在氧气中完全燃烧,只生成1molCO2和2molH2O,则E的分子式是 。
|
(3)有无色气体产生 2H2O2===2H2O+O2↑ (4)CH4O。
2 [2008茂名一模]Al和Si、Ge和As在元素周期表金属和非金属过渡位置上,在其单质和化合物在建筑业、电子工业和石油化工等方面应用广泛。请回答下列问题:
 (1) As 的价层电子构型为
(1) As 的价层电子构型为
(2) AlCl3是化工生产中的常用催化剂,熔点为192.6℃,熔融状态以二聚体A12C16形式存在,其中铝原子与氯原子的成键类型是
(3)超高导热绝缘耐高温纳米氮化铝(AlN)在绝缘材料中的应用广泛,AlN晶体与金刚石类似,每个Al原子与个N原子相连,与同一个Al原子相连的N原子构成的空间构型为。在四大晶体类型中,AlN属于 晶体。
(4)Si和C 同主族,Si、C和0成键情况如下:
在C和0之间可以形成双键形成CO2分子,而Si和O则不能和碳那样形成有限分子原因是
(5)SiCl4(l)常用作烟雾剂,原因Si存在3d轨道,能同H20 (l)配位而剧烈水解,在潮湿的空气中发烟,试用化学方程式表示其原理
(l) 4s24p3( l 分) (2)共价键(或σ键) (l分)
(3) 4 (l分)正四面体(l分)原子(2分) (4) Si一0大于C一0的键,C=0的键能大于Si=O的键能,所以Si和O成单键,而C和O以双键形成稳定分子( 2 分)
(5)SiCl4(l) + 3H2O (l) = H2Si03 (s) + 4HCl(aq) ( 2 分)
选修有机化学5
3.元素电离能和元素电负性
第一电离能:气态电中性基态原子失去1个电子,转化为气态基态正离子所需要的能量叫做第一电离能。常用符号I1表示,单位为kJ/mol。
(1).原子核外电子排布的周期性.
 随着原子序数的增加,元素原子的外围电子排布呈现周期性的变化:每隔一定数目的元素,元素原子的外围电子排布重复出现从ns1到ns2np6的周期性变化.
随着原子序数的增加,元素原子的外围电子排布呈现周期性的变化:每隔一定数目的元素,元素原子的外围电子排布重复出现从ns1到ns2np6的周期性变化.
(2).元素第一电离能的周期性变化.
随着原子序数的递增,元素的第一电离能呈周期性变化:
★同周期从左到右,第一电离能有逐渐增大的趋势,稀有气体的第一电离能最大,碱金属的第一电离能最小;
★同主族从上到下,第一电离能有逐渐减小的趋势.
说明:
①同周期元素,从左往右第一电离能呈增大趋势。电子亚层结构为全满、半满时较相邻元素要大即第 ⅡA 族、第 ⅤA 族元素的第一电离能分别大于同周期相邻元素。Be、N、Mg、P
②.元素第一电离能的运用:
a.电离能是原子核外电子分层排布的实验验证.
b.用来比较元素的金属性的强弱. I1越小,金属性越强,表征原子失电子能力强弱.
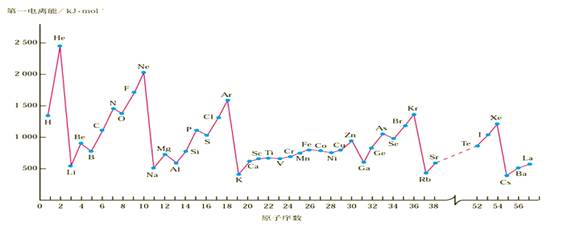
(3).元素电负性的周期性变化.
元素的电负性:元素的原子在分子中吸引电子对的能力叫做该元素的电负性。
随着原子序数的递增,元素的电负性呈周期性变化:同周期从左到右,主族元素电负性逐渐增大;同一主族从上到下,元素电负性呈现减小的趋势.
电负性的运用:
a.确定元素类型(一般>1.8,非金属元素;<1.8,金属元素).
b.确定化学键类型(两元素电负性差值>1.7,离子键;<1.7,共价键).
c.判断元素价态正负(电负性大的为负价,小的为正价).
d.电负性是判断金属性和非金属性强弱的重要参数(表征原子得电子能力强弱).
例8.下列各组元素,按原子半径依次减小,元素第一电离能逐渐升高的顺序排列的是
A.K、Na、Li B.N、O、C C.Cl、S、P D.Al、Mg、Na
例9.已知X、Y元素同周期,且电负性X>Y,下列说法错误的是
A.X与Y形成化合物时,X显负价,Y显正价
B.第一电离能可能Y小于X
 C.最高价含氧酸的酸性:X对应的酸性弱于Y对应的酸性
C.最高价含氧酸的酸性:X对应的酸性弱于Y对应的酸性
D.气态氢化物的稳定性:HmY小于HmX
例10.气态中性原子失去一个电子转化为气态正离子所需要的最低能量叫做第一电离能(I1),气态正离子继续失去电子所需最低能量依次称为第二电离能(I2)、第三电离能(I3)……下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据.
|
元素 |
I1/eV |
I2/eV |
I3/eV |
|
甲 |
5.7 |
47.4 |
71.8 |
|
乙 |
7.7 |
15.1 |
80.3 |
|
丙 |
13.0 |
23.9 |
40.0 |
|
丁 |
15.7 |
27.6 |
40.7 |
下列说法正确的是
A.甲的金属性比乙强 B.乙的化合价为+1价
C.丙一定为非金属元素 D.丁一定是金属元素
例11.在下面的电子结构中,第一电离能最小的原子可能是
A.ns2np3 B.ns2np5 C.ns2np4 D.ns2np6
例12.第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量.下图是部分元素原子的第一电离能I1随原子序数变化的曲线图.
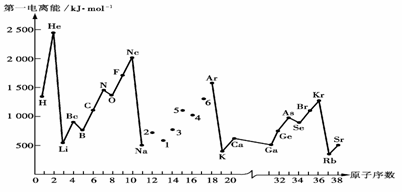
请回答以下问题:
(1).认真分析上图中同周期元素第一电离能的变化规律,将Na--Ar之间六种元素用短线连接起来,构成完整的图像.
(2).从上图分析可知,同一主族元素原子的第一电离能I1变化规律是______________;
(3).上图中5号元素在周期表中的位置是________________________________________;
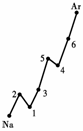 (4).上图中4、5、6三种元素的气态氢化物的沸点均比同主族上一周期的元素气态氢化物低很多,原因是:__________________________________.
(4).上图中4、5、6三种元素的气态氢化物的沸点均比同主族上一周期的元素气态氢化物低很多,原因是:__________________________________.
例12.(1).见上图(右) (2).从上到下依次减小
 (3).第三周期,ⅤA族
(3).第三周期,ⅤA族
(4).因同主族上一周期的元素的氢化物分子间存在氢键
例13.1932年美国化学家鲍林首先提出了电负性的概念.电负性(用X表示)也是元素的一种重要性质,若 x 越大,其原子吸引电子的能力越强,在所形成的分子中成为带负电荷的一方.下面是某些短周期元素的 x 值:
|
元素符号 |
Li |
Be |
B |
C |
O |
F |
Na |
Al |
Si |
P |
S |
Cl |
|
x 值 |
0.98 |
1.57 |
2.04 |
2.55 |
3.44 |
3.98 |
0.93 |
1.61 |
1.90 |
2.19 |
2.58 |
3.16 |
⑴.通过分析 x 值变化规律,确定N、Mg的 x 值范围:
<x (N)< , <x (Mg)< .
⑵.推测x值与原子半径的关系是 ;根据短周期元素的x值变化特点,体现了元素性质的 变化规律.
⑶.某有机化合物结构中含S-N键,其共用电子对偏向 (写原子名称).
⑷.经验规律告诉我们:当成键的两原子相应元素的 x 差值△x>1.7时,一般为离子键,当△ x<1.7时,一般为共价键.试推断AlBr3中化学键类型是 .
⑸.预测周期表中, x 值最小的元素位于 周期 族.(放射性元素除外)
例13.(1).2.55 3.44 0.93 1.57
(2).电负性随原子半径减小而增大,周期性
(3).氮 (4).共价键 (5).6,IA
『综合模拟训练』
2.(构造原理)
了解多电子原子中核外电子分层排布遵循的原理,能用电子排布式表示1-36号元素原子核外电子的排布.
(1).原子核外电子的运动特征可以用电子层、原子轨道(亚层)和自旋方向来进行描述.在含有多个核外电子的原子中,不存在运动状态完全相同的两个电子.
(2).原子核外电子排布原理.
①.能量最低原理:电子先占据能量低的轨道,再依次进入能量高的轨道.
②.泡利不相容原理:每个轨道最多容纳两个自旋状态不同的电子.
③.洪特规则:在能量相同的轨道上排布时,电子尽可能分占不同的轨道,且自旋状态相同.
洪特规则的特例:在等价轨道的全充满(p6、d10、f14)、半充满(p3、d5、f7)、全空时(p0、d0、f0)的状态,具有较低的能量和较大的稳定性.如24Cr [Ar]3d54s1、29Cu [Ar]3d104s1.
(3).掌握能级交错图和1-36号元素的核外电子排布式.
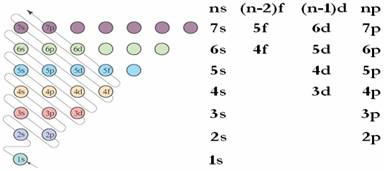
①根据构造原理,基态原子核外电子的排布遵循图⑴箭头所示的顺序。
②根据构造原理,可以将各能级按能量的差异分成能级组如图⑵所示,由下而上表示七个能级组,其能量依次升高;在同一能级组内,从左到右能量依次升高。基态原子核外电子的排布按能量由低到高的顺序依次排布。
例3.表示一个原子在第三电子层上有10个电子可以写成
A.310 B.3d10 C.3s23p63d2 D. 3s23p64s2
例4.下列电子排布中,原子处于激发状态的是
 A.1s22s22p5
B. 1s22s22p43s2
A.1s22s22p5
B. 1s22s22p43s2
C. 1s22s22p63s23p63d44s2 D. 1s22s22p63s23p63d34s2
例5.下列关于价电子构型为3s23p4的粒子描述正确的是
A.它的元素符号为O
B.它的核外电子排布式为1s22s22p63s23p4
C.它可与H2生成液态化合物
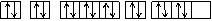 D.其电子排布图为:
D.其电子排布图为:
1s 2s 2p 3s 3p
例6.按所示格式填写下表有序号的表格:
|
原子序数 |
电子排布式 |
价层电子排布 |
周期 |
族 |
|
17 |
① |
② |
③ |
④ |
|
⑤ |
1s22s22p6 |
⑥ |
⑦ |
⑧ |
|
⑨ |
⑩ |
3d54s1 |
⑾ |
ⅥB |
例6.①.1s22s22p63s23p5 ②.3s23p5 ③.3 ④.ⅦA ⑤.10 ⑥.2s22p6
⑦.2 ⑧.0 ⑨.24 ⑩.1s22s22p63s23p63d54s1 ⑾.4
例7.(1).砷原子的最外层电子排布式是4s24p3,在元素周期表中,砷元素位于__________
周期 族;最高价氧化物的化学式为 ,砷酸钠的化学式是 .
(2).已知下列元素在周期表中的位置,写出它们最外层电子构型和元素符号:
①.第4周期ⅣB族 ;
②.第5周期ⅦA族 .
例7.(1).4 ⅤA As2O5 Na3AsO4
(2).①.3d24s2 Ti ②.5S25p5 I
28.(12分) 某化学兴趣小组有一次活动的内容是:对一包干燥的红色粉末组成进行探究。请你参与并回答有关问题。
[教师提醒]它由Cu 、Fe2O3 、Fe(OH)3三种固体中的一种或两种组成。
[提出猜想]红色粉末可能的组成有:
①只有Cu ②只有Fe2O3
③只有 Fe(OH)3 ④是Fe2O3 、Fe(OH)3的混合物
⑤是Cu 、Fe2O3的混合物 ⑥是Cu 、Fe(OH)3的混合物
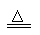 [资料获悉](1)2Fe(OH)3 Fe2O3
+3H2O
[资料获悉](1)2Fe(OH)3 Fe2O3
+3H2O
(2)白色无水CuSO4遇水变蓝
 (3)Cu在FeCl3溶液中发生反应:2FeCl3+Cu 2FeCl2+CuCl2
(3)Cu在FeCl3溶液中发生反应:2FeCl3+Cu 2FeCl2+CuCl2
 [探究思路]利用物质的性质不同设计实验加以甄别,先分别探究其中是否含有Fe(OH)3 、Cu等,逐步缩小范围,然后再选择适当的试剂和方法通过实验探究其组成。
[探究思路]利用物质的性质不同设计实验加以甄别,先分别探究其中是否含有Fe(OH)3 、Cu等,逐步缩小范围,然后再选择适当的试剂和方法通过实验探究其组成。
(装置内空气中的水蒸气、CO2忽略不计)
[实验探究]
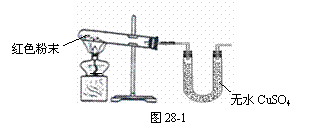
(1)甲同学取适量红色粉末装入试管中,按图28-1
进行实验。结果无水CuSO4没有变蓝,从而排除
猜想中的 ▲ 。(填猜想中的序号)
(2)在甲同学实验结论的基础上,乙同学另取少量红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解,溶液变色。乙同学认为可以排除猜想中的①和⑤,而丙同学认为只能排除猜想①,你认为 ▲ 的观点正确(填“乙”或“丙”)。
 (3)丁同学为进一步确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按图28-2在通风橱中进行实验。开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却。反应前后称量相关装置和物质的总质量,其数据如下表:
(3)丁同学为进一步确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按图28-2在通风橱中进行实验。开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却。反应前后称量相关装置和物质的总质量,其数据如下表:
|
|
反应前 |
反应后 |
|
Ⅰ 组 |
玻璃管和红色粉末的总质量为37.3 g |
玻璃管和固体物质的总质量为36.1 g |
|
Ⅱ 组 |
洗气瓶和所盛溶液 的总质量为180.0 g |
洗气瓶和瓶中物质 的总质量为183.1 g |
[交流讨论]
(1)在装置A中先通CO气体的作用是 ▲ 。
(2)应该选择 ▲ 组的实验数据计算来确定红色粉末的组成。最终计算结果表明:该红色粉末的组成是猜想中的第 ▲ 组(填序号)。
(3)写出A装置中发生反应的化学方程式 ▲ ;实验中观察到A装置中的现象为 ▲ 。
(4)为了防止溶液倒吸,本实验停止加热前是否需要先断开A和B的连接处? ▲ (填“需要”或“不需要”),理由是 ▲ 。
[反思评价] 戊同学指出:从环保角度,图28-2装置有严重不足之处。你认为应该如何改进? ▲ 。
[拓展延伸]有同学提出丁同学上述实验中的CO还可以用H2代替,并将图28-2中B装置换成盛有碱石灰(生石灰和氢氧化钠固体混合物)的干燥管,来确定该红色粉末的组成,你认为是否可行? ▲ (填“可行”或“不可行”)。
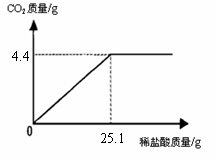 (7分) 某班一次社会实践活动是到连云港碱厂参观,该厂主要产品之一是小苏打(碳酸氢钠)。参观结束,同学们带回一些化验室里废弃的小苏打样品,来测定其中碳酸氢钠的质量分数(假设该样品中只含有氯化钠一种杂质)。取样品9.3
g逐滴加入稀盐酸,生成CO2气体的质量与滴加稀盐酸的质量关系如右图所示,求:(计算结果用百分数表示,保留到小数点后一位数字)
(7分) 某班一次社会实践活动是到连云港碱厂参观,该厂主要产品之一是小苏打(碳酸氢钠)。参观结束,同学们带回一些化验室里废弃的小苏打样品,来测定其中碳酸氢钠的质量分数(假设该样品中只含有氯化钠一种杂质)。取样品9.3
g逐滴加入稀盐酸,生成CO2气体的质量与滴加稀盐酸的质量关系如右图所示,求:(计算结果用百分数表示,保留到小数点后一位数字)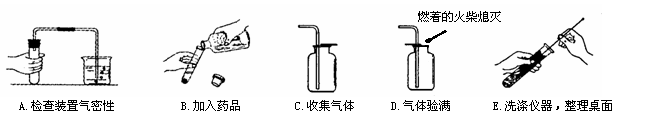
 的转化关系如图所示(其中“
”代表物质之间的转化关
的转化关系如图所示(其中“
”代表物质之间的转化关
 (2)写出下列转化的化学反应方程式:A C ▲ ; H G ▲
;
(2)写出下列转化的化学反应方程式:A C ▲ ; H G ▲
; 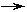 判断:H G的反应属于基本反应类型中的
▲ 反应。
判断:H G的反应属于基本反应类型中的
▲ 反应。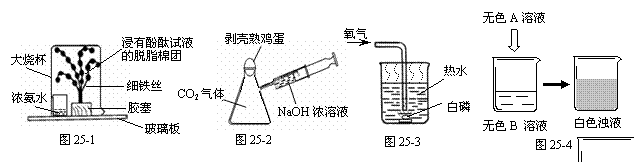 (8分) 2009年春节联欢晚会上,刘谦的魔术表演激起了人们强烈的好奇心,并在全国范围内掀起了魔术表演的热潮。在学校科技节活动中,一位九年级同学给低年级同学表演了一组化学小魔术,请你利用所学化学知识揭开其中之谜。
(8分) 2009年春节联欢晚会上,刘谦的魔术表演激起了人们强烈的好奇心,并在全国范围内掀起了魔术表演的热潮。在学校科技节活动中,一位九年级同学给低年级同学表演了一组化学小魔术,请你利用所学化学知识揭开其中之谜。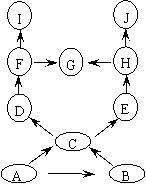 道具如图25-4所示,当A溶液加到烧杯中,无色溶液变成白色浊液。若A为酸溶液,则A、B的可能组合:A为 ▲ ;B为 ▲
。(只需写一组)
道具如图25-4所示,当A溶液加到烧杯中,无色溶液变成白色浊液。若A为酸溶液,则A、B的可能组合:A为 ▲ ;B为 ▲
。(只需写一组)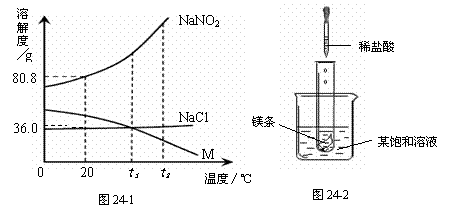 (6分) NaNO2(亚硝酸钠)、NaCl和物质M (不含结晶水)的溶解度曲线如图24-1所示,请根据图像和有关信息回答下列问题:
(6分) NaNO2(亚硝酸钠)、NaCl和物质M (不含结晶水)的溶解度曲线如图24-1所示,请根据图像和有关信息回答下列问题: