10.明矾能够用来净水的原理
|
[特别提醒]:盐类水解的应用都是从水解的本质出发的。会解三类习题:(1)比较大小型,例:比较PH值大小;比较离子数目大小等。(2)实验操作型,例:易水解物质的制取;中和滴定中指示剂选定等。(3)反应推理型,例:判断金属与盐溶液的反应产物;判断盐溶液蒸干时的条件;判断离子方程式的正误;判断离子能否共存等。 |
[例3]蒸干FeCl3水溶液后再强热,得到的固体物质主要是 ( )
A. FeCl3 B. FeCl3·6H2O C. Fe(OH)3 D. Fe2O3
[解析] FeCl3水中发生水解:FeCl3+3H2O 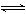 Fe(OH)3 + 3HCl,加热促进水解,由于HCl具有挥发性,会从溶液中挥发出去,从而使FeCl3彻底水解生成Fe(OH)3,Fe(OH)3为不溶性碱,受热易分解,最终生成Fe2O3。
Fe(OH)3 + 3HCl,加热促进水解,由于HCl具有挥发性,会从溶液中挥发出去,从而使FeCl3彻底水解生成Fe(OH)3,Fe(OH)3为不溶性碱,受热易分解,最终生成Fe2O3。
[答案]D
[规律总结] 易挥发性酸所生成的盐在加热蒸干时水解趋于完全不能得到其晶体。例如:AlCl3、FeCl3;
而高沸点酸所生成的盐,加热蒸干时可以得到相应的晶体,例:CuSO4、NaAlO2。
 Na+(aq)+Cl-(aq)
AgCl(s)
Na+(aq)+Cl-(aq)
AgCl(s)