摘要:2.要将100g10%的蔗糖溶液变为40%可向原溶液中加入多少克蔗糖固体或蒸发多少克水?
网址:http://m.1010jiajiao.com/timu_id_925432[举报]
 某同学绘制如图所示的a、b、c三种固体物质的溶解度曲线,回答下列问题:
某同学绘制如图所示的a、b、c三种固体物质的溶解度曲线,回答下列问题:①在t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是
c<b<a
c<b<a
(填写物质序号).t2℃时30g a物质加入到50g水中不断搅拌,能形成80g溶液吗?不能
不能
(填写“能”或“不能”).点P表示的意义t1℃时,a、c物质的溶解度相等
t1℃时,a、c物质的溶解度相等
.②溶解度受温度影响变化较小的物质是
b
b
,要从它的饱和溶液中得到大量晶体应采用蒸发溶剂
蒸发溶剂
的方法.要从a的饱和溶液溶液中得到大量晶体应采用冷却热饱和溶液
冷却热饱和溶液
.若要将接近饱和的c溶液变为饱和溶液,可采取的方法是升高温度(加入c物质或蒸发溶剂)
升高温度(加入c物质或蒸发溶剂)
.③t1℃时a的饱和溶液升高到t2℃,此时溶液中溶质的质量分数将
不变
不变
(填“变大”“变小”“不变”,后同),其溶解度将增大
增大
.④将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是
A
A
(填写选项序号).A、b>a>c B、a>b>c C、a=b>c. 下表是氯化钠和硝酸钾的溶解度(部分):
下表是氯化钠和硝酸钾的溶解度(部分):| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 100℃ | |
| KNO3的溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 246 |
| NaCl的溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 39.8 |
蒸发溶剂
蒸发溶剂
、③降低温度
降低温度
;(2)从结晶的方法看,海水晒盐属于
蒸发
蒸发
结晶(选填“蒸发”或“降温”),使用该方法的原因是:氯化钠的溶解度受温度影响小
小
(选填“小”或“大”);(3)10℃时,在各盛有100g水的甲、乙两烧杯中,分别加入 等质量的氯化钠和硝酸钾固体,充分溶解后,现象如图所示.甲烧杯中加入的物质是
硝酸钾
硝酸钾
,加入的质量范围为:所加质量大于20.9克小于等于35.8克
所加质量大于20.9克小于等于35.8克
.
下表是氯化钠和硝酸钾的溶解度(部分):
(1)若要将接近饱和的硝酸钾溶液变为饱和溶液,可采取的方法有:①继续加入硝酸钾固体、② 、③ ;
(2)从结晶的方法看,海水晒盐属于 结晶(选填“蒸发”或“降温”),使用该方法的原因是:氯化钠的溶解度受温度影响 (选填“小”或“大”);
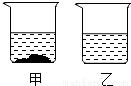
(3)10℃时,在各盛有100g水的甲、乙两烧杯中,分别加入 等质量的氯化钠和硝酸钾固体,充分溶解后,现象如图所示.甲烧杯中加入的物质是 ,加入的质量范围为: .
 查看习题详情和答案>>
查看习题详情和答案>>
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 100℃ | |
| KNO3的溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 246 |
| NaCl的溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 39.8 |
(2)从结晶的方法看,海水晒盐属于 结晶(选填“蒸发”或“降温”),使用该方法的原因是:氯化钠的溶解度受温度影响 (选填“小”或“大”);
(3)10℃时,在各盛有100g水的甲、乙两烧杯中,分别加入 等质量的氯化钠和硝酸钾固体,充分溶解后,现象如图所示.甲烧杯中加入的物质是 ,加入的质量范围为: .
 查看习题详情和答案>>
查看习题详情和答案>>
某同学绘制如图所示的a、b、c三种固体物质的溶解度曲线,回答下列问题:
①在t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是 (填写物质序号).t2℃时30g a物质加入到50g水中不断搅拌,能形成80g溶液吗? (填写“能”或“不能”).点P表示的意义 .
②溶解度受温度影响变化较小的物质是 ,要从它的饱和溶液中得到大量晶体应采用 的方法.要从a的饱和溶液溶液中得到大量晶体应采用 .若要将接近饱和的c溶液变为饱和溶液,可采取的方法是 .
③t1℃时a的饱和溶液升高到t2℃,此时溶液中溶质的质量分数将 (填“变大”“变小”“不变”,后同),其溶解度将 .
④将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是 (填写选项序号).A、b>a>c B、a>b>c C、a=b>c.
 查看习题详情和答案>>
查看习题详情和答案>>
①在t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是 (填写物质序号).t2℃时30g a物质加入到50g水中不断搅拌,能形成80g溶液吗? (填写“能”或“不能”).点P表示的意义 .
②溶解度受温度影响变化较小的物质是 ,要从它的饱和溶液中得到大量晶体应采用 的方法.要从a的饱和溶液溶液中得到大量晶体应采用 .若要将接近饱和的c溶液变为饱和溶液,可采取的方法是 .
③t1℃时a的饱和溶液升高到t2℃,此时溶液中溶质的质量分数将 (填“变大”“变小”“不变”,后同),其溶解度将 .
④将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是 (填写选项序号).A、b>a>c B、a>b>c C、a=b>c.
 查看习题详情和答案>>
查看习题详情和答案>>
 下表是氯化钠和硝酸钾的溶解度(部分):
下表是氯化钠和硝酸钾的溶解度(部分):
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 100℃ | |
| KNO3的溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 246 |
| NaCl的溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 39.8 |
(2)从结晶的方法看,海水晒盐属于______结晶(选填“蒸发”或“降温”),使用该方法的原因是:氯化钠的溶解度受温度影响______(选填“小”或“大”);
(3)10℃时,在各盛有100g水的甲、乙两烧杯中,分别加入 等质量的氯化钠和硝酸钾固体,充分溶解后,现象如图所示.甲烧杯中加入的物质是______,加入的质量范围为:______. 查看习题详情和答案>>