摘要:A.I处试液变蓝 B.Ⅱ处溶液变浑浊C.Ⅲ处溶液颜色逐渐变浅 D.Ⅳ处试纸变红
网址:http://m.1010jiajiao.com/timu_id_921437[举报]
小王同学对化学充满了兴趣,喜欢做各种实验.有一次他和其它同学对镁进行了一些研究:
【Ⅰ】他们用砂纸打磨掉表面灰黑色的物质,将其放入水中,未看到有明显的现象,改用酒精灯加热后,观察到表面有大量气泡,经验是氢气.他们又向溶液中滴加无色酚酞试液,发现酚酞变成红色,说明有
【Ⅱ】该小组成员开始研究镁带表面的灰黑色物质,小王大胆提出了三个假设:
假设1该物质是MgO;假设2该物质是Mg(OH)2;假设3镁可能会象铜一样生成碱式碳酸镁.
但其它同这立即否定了他的假设1和2,因为根据所学的知识MgO,Mg(OH)2都是
【III】他们在取镁带表面灰黑色样品时感到比较困难,索性将表面发黑的镁带全部磨成粉末,放入干燥的硬质试管中加热,一段时间后,镁粉突然出现红热燃烧起来,反应停止后有少量黑色物质A粘在试管壁上,这黑色物质A中混有什么?他们查资料筛选出几条有价值的信息:
(1)2Mg+CO2=2MgO+C; (2)C+2H2SO4(浓)=CO2↑+SO2↑+H2O;(3)SO2+Ca(OH)2=CaSO3↓(白)+H2O.
试分析A物质为
【Ⅳ】为验证碳和浓硫酸反应的三种产物,应将气体通过下列三种试剂(假设每步均完全)即:
气体→
(现象依次为)
【V】该兴趣小组的同学进一步又查出胃药碱式碳酸镁有多种不同的组成,如Mg2(OH)2CO3、Mg4(OH)2(CO3)3、Mg5(OH)2(CO3)4等.小红同学为确定碱式碳酸镁的组成,设计如图所示的实验:
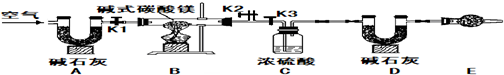
实验步骤(1)按图组装置后,首先进行的操作是
实验步骤(2)称取样品31g,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量为87.6g,装碱石灰的U型管D的质量为74.7g.
实验步骤(3)打开活塞
实验步骤(4)关闭活塞
实验步骤(5)打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,称得洗气瓶C的质量为89.4g,U型管D的质量为87.9g,则该碱式碳酸镁的化学式为
【Ⅵ】小明认为其化学式可用Mgx(OH)2(CO3)y表示,根据化合价规律,x和y的关系是
小明设计了两套方案(忽略装置中原来的气体)
方案I:只测定分解后生成的水,连接方案是A→C→B,则C中盛放的药品是
方案II:只测定分解生成的CO2的质量,连接方案是A→C→B→C,则B中的药品是
请你设计出更简单的实验方法
若取样品7.88克,方案I测得生成水0.36g,方案II测得生成CO2 3.52g,请你选择实验数据,通过计算得出碱式碳酸镁的化学式.
查看习题详情和答案>>
【Ⅰ】他们用砂纸打磨掉表面灰黑色的物质,将其放入水中,未看到有明显的现象,改用酒精灯加热后,观察到表面有大量气泡,经验是氢气.他们又向溶液中滴加无色酚酞试液,发现酚酞变成红色,说明有
OH-
OH-
产生.该实验表明化学反应的发生和速率与温度
温度
有关,许多物质的反应速度
反应速度
随温度的升高而增大.【Ⅱ】该小组成员开始研究镁带表面的灰黑色物质,小王大胆提出了三个假设:
假设1该物质是MgO;假设2该物质是Mg(OH)2;假设3镁可能会象铜一样生成碱式碳酸镁.
但其它同这立即否定了他的假设1和2,因为根据所学的知识MgO,Mg(OH)2都是
白
白
色固体.对于假设3,他们设计了如下方案| 实验方案 | 实验现象 | 实验结论 |
| 证明有CO32- | ||
| 取样于试管,加热 | 证明有氢元素 |
(1)2Mg+CO2=2MgO+C; (2)C+2H2SO4(浓)=CO2↑+SO2↑+H2O;(3)SO2+Ca(OH)2=CaSO3↓(白)+H2O.
试分析A物质为
C
C
,根据上述信息,他们又设计了下列实验,帮助他们完成实验报告:| 实验方案 | 实验现象 | 实验结论 |
| 取反应后试管内样品,先滴加过量的 稀硫酸 稀硫酸 |
固体部分溶解 | |
| 再 加热 加热 (填一具体的实验操作) |
黑色固体全部溶解 |
气体→
无水硫酸铜
无水硫酸铜
→高锰酸钾溶液
高锰酸钾溶液
→澄清石灰水
澄清石灰水
;(现象依次为)
白色固体变蓝
白色固体变蓝
、紫红色褪去
紫红色褪去
、澄清石灰水变浑浊
澄清石灰水变浑浊
【V】该兴趣小组的同学进一步又查出胃药碱式碳酸镁有多种不同的组成,如Mg2(OH)2CO3、Mg4(OH)2(CO3)3、Mg5(OH)2(CO3)4等.小红同学为确定碱式碳酸镁的组成,设计如图所示的实验:

实验步骤(1)按图组装置后,首先进行的操作是
检查装置的气密性
检查装置的气密性
.E处干燥管内盛放的药品是碱石灰
碱石灰
,其作用是防止空气中的水蒸气进入装置
防止空气中的水蒸气进入装置
.实验步骤(2)称取样品31g,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量为87.6g,装碱石灰的U型管D的质量为74.7g.
实验步骤(3)打开活塞
K1K2
K1K2
,关闭K3
K3
,缓慢鼓入空气数分钟.实验步骤(4)关闭活塞
K1K2
K1K2
,打开K3
K3
,点燃酒精灯加热至不再产生气体为止.实验步骤(5)打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,称得洗气瓶C的质量为89.4g,U型管D的质量为87.9g,则该碱式碳酸镁的化学式为
Mg4(OH)2CO3
Mg4(OH)2CO3
.【Ⅵ】小明认为其化学式可用Mgx(OH)2(CO3)y表示,根据化合价规律,x和y的关系是
x=y+1
x=y+1
,写出该物质分解的方程式:Mgx(OH)2(CO3)y
xMgO+H2O+yCO2↑
| ||
Mgx(OH)2(CO3)y
xMgO+H2O+yCO2↑
| ||
小明设计了两套方案(忽略装置中原来的气体)
方案I:只测定分解后生成的水,连接方案是A→C→B,则C中盛放的药品是
浓硫酸
浓硫酸
,B中盛放的药品是氯化钙固体
氯化钙固体

方案II:只测定分解生成的CO2的质量,连接方案是A→C→B→C,则B中的药品是
碱石灰
碱石灰
,最后连接的C中的药品是氢氧化钠溶液
氢氧化钠溶液
请你设计出更简单的实验方法
加热碱式碳酸镁称量反应前后固体质量
加热碱式碳酸镁称量反应前后固体质量
.若取样品7.88克,方案I测得生成水0.36g,方案II测得生成CO2 3.52g,请你选择实验数据,通过计算得出碱式碳酸镁的化学式.
20、(1)汽车行驶时,在电火花作用下,在气缸里发生了一系列化学反应,其中包括:N2+O2═2NO,在通常状况下,一氧化氮气体的密度比空气的略大、难溶于水;一氧化氮有毒,跟氧气很容易化合生成红棕色气体二氧化氮.二氧化氮易溶于水并与水反应生成一氧化氮和硝酸.
①上述内容中,描述一氧化氮物理性质的 是
②汽车在行驶的过程中,还发生了一氧化氮和氧气的化合反应,其化学方程式:
③如右图,将一支充满NO2气体的试管倒立在烧杯中,一段时间后,试分析可能出现的实验现象:
(2)一次性塑料包装袋造成的环境污染已经引起了社会的高度关注,许多城市已经开始使用纸制的食品袋.同学们经过查阅资料,得知食品袋的组成成分含有碳元素和氢元素,请选择以下实验装置进行验证:
①你所选择的实验装置的连接顺序是纯氧→
②简单叙述实验现象及结论
③验中选择纯氧而不选用空气的原因是
查看习题详情和答案>>
①上述内容中,描述一氧化氮物理性质的 是
在通常状况下,一氧化氮气体的密度比空气略大,难溶于水
.②汽车在行驶的过程中,还发生了一氧化氮和氧气的化合反应,其化学方程式:
2NO+O2=2NO2
.③如右图,将一支充满NO2气体的试管倒立在烧杯中,一段时间后,试分析可能出现的实验现象:
a试管内气体红棕逐渐变淡,最后变成无色
、b试管内液面上升,约至离试管口2/3处
、c烧杯内液体全由紫色变红色
.(2)一次性塑料包装袋造成的环境污染已经引起了社会的高度关注,许多城市已经开始使用纸制的食品袋.同学们经过查阅资料,得知食品袋的组成成分含有碳元素和氢元素,请选择以下实验装置进行验证:
①你所选择的实验装置的连接顺序是纯氧→
a
→b
→c
→i
→h
(用a、b等符号表示)②简单叙述实验现象及结论
无水硫酸铜变蓝,证明食品袋中含有氢元素;石灰水变浑浊,证明食品袋中含有碳元素
.③验中选择纯氧而不选用空气的原因是
因为空气中含有CO2和H2O,影响测定
.
(2008?延庆县一模)(1)【探究I】某同学在一食品包装内发现有白色颗粒状固体A的小纸袋,上面写着“生石灰、干燥剂,请勿食用”.他随手将小纸袋放在窗台上,过一段时间后发现纸袋内的白色颗粒粘在一起成为块状固体B.他取块状固体B加入盛有一定量水的试管内(反应完全),振荡、静置、过滤后得到少量白色固体C.(不考虑其他杂质)
[提出问题]块状固体C的成分是什么?
[猜想与假设]白色固体C所有可能的组成是
[实验探究]实验方案设计(填写下表)
(2)【探究II】实验中,通常用饱和石灰水检验CO2,用浓NaOH溶液吸收CO2.针对这一方法,小明设计了以下实验.在两个体积相同的盛满CO2的广口瓶中,分别加入等体积的饱和石灰水和浓NaOH溶液.实验装置和现象如图 所示.
所示.
①甲、乙装置中实验现象的不同之处是
②通过上述实验可知,吸收CO2较多的溶液是
查看习题详情和答案>>
[提出问题]块状固体C的成分是什么?
[猜想与假设]白色固体C所有可能的组成是
①CaCO3、Ca(OH)2②CaCO3③Ca(OH)2
①CaCO3、Ca(OH)2②CaCO3③Ca(OH)2
;[实验探究]实验方案设计(填写下表)
| 实验步骤 | 实验现象 | 结论 |
| ①向盛有少量固体C的试管中加入适量稀盐酸 | 若有气泡生成 若无气泡生成 若有气泡生成 若无气泡生成 |
含CaCO3 不含CaCO3 含CaCO3 不含CaCO3 |
| ② 将少量固体放入足量水中,充分搅拌,静置,向其中滴加紫色石蕊试液 将少量固体放入足量水中,充分搅拌,静置,向其中滴加紫色石蕊试液 |
变蓝 不变蓝(或仍呈紫色) 变蓝 不变蓝(或仍呈紫色) |
含Ca(OH)2 不含Ca(OH)2 含Ca(OH)2 不含Ca(OH)2 |
 所示.
所示.①甲、乙装置中实验现象的不同之处是
甲、乙装置中气球都变大,但甲中气球体积小于乙中气球体积;甲装置中石灰水变浑浊,乙装置中液体仍澄清
甲、乙装置中气球都变大,但甲中气球体积小于乙中气球体积;甲装置中石灰水变浑浊,乙装置中液体仍澄清
,请写出乙实验中有关反应的化学方程式2NaOH+CO2═Na2CO3+H2O
2NaOH+CO2═Na2CO3+H2O
.②通过上述实验可知,吸收CO2较多的溶液是
NaOH溶液
NaOH溶液
. 将一只大烧杯倒扣在培养皿上,培养皿上所放物质如图所示.下列对有关实验现象的描述,肯定不正确的是
将一只大烧杯倒扣在培养皿上,培养皿上所放物质如图所示.下列对有关实验现象的描述,肯定不正确的是