摘要:方案一 方案二[进行实验]按上述两个方案进行多次实验.[反思与评价]a.实验中磷的量应为足量.原因是 ① .b.两个方案的实验测定结果不同.测定结果比较准确的是方案 ② .原因是 ③ . c.经过A.B两组同学的实验.A组测得的含氧量总是大于B组的.你认为原因是 ④ .
网址:http://m.1010jiajiao.com/timu_id_911490[举报]
小明用过氧化氢溶液做实验室制取氧气的实验,有关反应的化学方程式为:______.
小明在操作中误将黑色粉末氧化铜当成二氧化锰放入过氧化氢溶液中,发现迅速产生大量气泡,经检验为氧气,反应停止后,黑色物质仍然存在.
【提出问题】氧化铜在上述实验中的作用是什么?
【作出猜想】氧化铜是过氧化氢分解的催化剂.
【设计方案】
称取一定质量的氧化铜 
 .
.
【实验方案】小明按以上方案进行实验.

(1)为准确称量反应后黑色粉末的质量,把黑色粉末后进行称量.经称量,黑色粉末的质量与反应前加入的氧化铜质量相等.
(2)取少量黑色粉末,放入试管中,滴加足量稀硫酸,充分振荡.观察到:______,证明黑色粉末是氧化铜.
通过以上探究,证明氧化铜在此实验中是过氧化氢分解的催化剂.
【拓展探究】氧化铁也是过氧化氢分解的催化剂.若通过实验比较氧化铁与氧化铜催化能力的大小,可取相同颗粒大小、相等质量的两种粉末,在室温条件下分别加入到______的过氧化氢溶液中,观察产生气泡的快慢.
查看习题详情和答案>>
小明用过氧化氢溶液做实验室制取氧气的实验,有关反应的化学方程式为:______.
小明在操作中误将黑色粉末氧化铜当成二氧化锰放入过氧化氢溶液中,发现迅速产生大量气泡,经检验为氧气,反应停止后,黑色物质仍然存在.
【提出问题】氧化铜在上述实验中的作用是什么?
【作出猜想】氧化铜是过氧化氢分解的催化剂.
【设计方案】
称取一定质量的氧化铜
.
【实验方案】小明按以上方案进行实验.

(1)为准确称量反应后黑色粉末的质量,把黑色粉末后进行称量.经称量,黑色粉末的质量与反应前加入的氧化铜质量相等.
(2)取少量黑色粉末,放入试管中,滴加足量稀硫酸,充分振荡.观察到:______,证明黑色粉末是氧化铜.
通过以上探究,证明氧化铜在此实验中是过氧化氢分解的催化剂.
【拓展探究】氧化铁也是过氧化氢分解的催化剂.若通过实验比较氧化铁与氧化铜催化能力的大小,可取相同颗粒大小、相等质量的两种粉末,在室温条件下分别加入到______的过氧化氢溶液中,观察产生气泡的快慢.
查看习题详情和答案>>
小明在操作中误将黑色粉末氧化铜当成二氧化锰放入过氧化氢溶液中,发现迅速产生大量气泡,经检验为氧气,反应停止后,黑色物质仍然存在.
【提出问题】氧化铜在上述实验中的作用是什么?
【作出猜想】氧化铜是过氧化氢分解的催化剂.
【设计方案】
称取一定质量的氧化铜
| 将其放入过氧化氢溶液中 |
| 反应结束后 |
|
【实验方案】小明按以上方案进行实验.

(1)为准确称量反应后黑色粉末的质量,把黑色粉末后进行称量.经称量,黑色粉末的质量与反应前加入的氧化铜质量相等.
(2)取少量黑色粉末,放入试管中,滴加足量稀硫酸,充分振荡.观察到:______,证明黑色粉末是氧化铜.
通过以上探究,证明氧化铜在此实验中是过氧化氢分解的催化剂.
【拓展探究】氧化铁也是过氧化氢分解的催化剂.若通过实验比较氧化铁与氧化铜催化能力的大小,可取相同颗粒大小、相等质量的两种粉末,在室温条件下分别加入到______的过氧化氢溶液中,观察产生气泡的快慢.
小明用过氧化氢溶液做实验室制取氧气的实验,有关反应的化学方程式为:
。
小明在操作中误将黑色粉末氧化铜当成二氧化锰放入过氧化氢溶液中,发现迅速产生大量气泡,经检验为氧气,反应停止后,黑色物质仍然存在。
【提出问题】氧化铜在上述实验中的作用是什么?
【作出猜想】氧化铜是过氧化氢分解的催化剂。
【设计方案】

|
|
 称取一定质量的氧化铜
称取一定质量的氧化铜 检验黑色粉末的化学性质
【实验方案】小明按以上方案进行实验。
(1)为准确称量反应后黑色粉末的质量,把黑色粉末后进行称量。经称量,黑色粉末的质量与反应前加入的氧化铜质量相等。
(2)取少量黑色粉末,放入试管中,滴加足量稀硫酸,充分振荡。观察到:
,证明黑色粉末是氧化铜。

通过以上探究,证明氧化铜在此实验中是过氧化氢分解的催化剂。
【拓展探究】氧化铁也是过氧化氢分解的催化剂。若通过实验比较氧化铁与氧化铜催化能力的大小 ,可取相同颗粒大小、相等质量的两种粉末,在室温条件下分别加入到
的过氧化氢溶液中,观察产生气泡的快慢。
查看习题详情和答案>>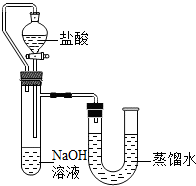 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其证明与某盐酸发生了中和反应.
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其证明与某盐酸发生了中和反应.(1)配制100g质量分数为8%的氢氧化钠溶液.
①计算:需要氢氧化钠固体的质量为
②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的
③溶解:用量筒量取所需的水,倒入盛有氢氧化钠固体的烧杯里,搅拌,使其溶解,并冷却至室温.
④把配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签.
(2)某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
【实验方案】
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且最终小至小于7,则证明NaOH溶液与稀盐酸发生了化学反应.
①用pH试纸测定NaOH溶液pH时,正确的操作是:
②简述强调“测得的pH小于7”的理由:
方案二:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生.如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应.该组同学在没使用温度计的情况下,通过如图所示装置完成了实验.则该组同学根据
 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其证明与某盐酸发生了中和反应.
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其证明与某盐酸发生了中和反应.