网址:http://m.1010jiajiao.com/timu_id_904142[举报]
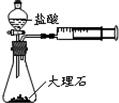 某实验小组利用下图装置对实验室制取CO2的速率快慢进行了研究.他们实验时所用的试剂和使用的反应条件如下表所示:
某实验小组利用下图装置对实验室制取CO2的速率快慢进行了研究.他们实验时所用的试剂和使用的反应条件如下表所示:
| 盐酸 | 大理石 | 温度条件 |
| 5% | 细颗粒 | 20℃ |
| 10% | 粗颗粒 | 40℃ |
| 每次用量均 | 每次用量均5g |
(1)实验小组同学设计的实验方案部分如下表,请根据表中信息帮助填写完整:
| 实验编号 | 温度 | 大理石规格 | HCl浓度 | 探究目的 |
| ① | 20℃ | 粗颗粒 | 5% | (I)实验①和②探究浓度对反应快慢的影响; (II)实验②和________探究温度对反应快慢的影响; (III)实验________和________探究大理石粗、细对反应快慢的影响. |
| ② | 20℃ | 粗颗粒 | ________ | |
| ③ | ________ | 细颗粒 | 5% | |
| ④ | 40℃ | ________ | 10% |
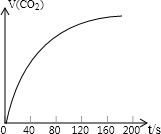
右图是根据某次实验数据作出的CO2和时间变化的关系曲.
请分析在80秒以后,产生CO2逐渐减慢的可能原因:
________.
 查看习题详情和答案>>
查看习题详情和答案>>
[查阅资料]
资料一:Fe粉和Fe3O4粉末能被磁铁吸引而FeO(黑色)不能;
资料二:Fe3O4中铁元素有+2、+3两种化合价,其化学式可用FeO?Fe2O3 的形式表示;
[提出猜想]黑色物质可能是Fe3O4、FeO和Fe粉中的一种或几种.
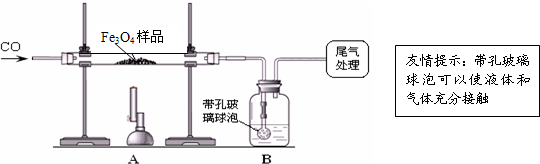
[进行实验]兴趣小组收集了CO与Fe2O3反应生成的黑色物质进行了下列实验:
| 实验方案 | 实验现象 | |
| 甲 | 取少量黑色物质用磁铁吸引 | 黑色物质全部被磁铁吸引 |
| 乙 | 取少量黑色物质加入30%热的盐酸中 | 无气泡、溶液颜色变成黄绿色 |
| 丙 | 取少量黑色物质加入硫酸铜溶液中 | 无任何现象 |
(1)甲实验现象说明黑色物质中没有
(2)生成的黑色物质应为Fe3O4;
(3)写出黑色粉末和热的盐酸反应的化学方程式
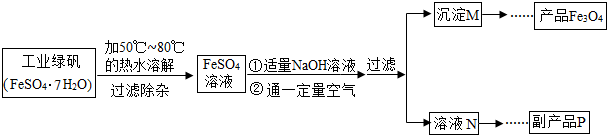
[拓展探究]同学们对Fe3O4产生了兴趣,从参考资料中找到了氧化沉淀法生产复印用高档Fe3O4粉的工艺流程简图.
[生产流程]
[查阅资料]
资料一:硫酸亚铁在不同温度下的溶解度如表所示:
| 温度/℃ | 0 | 10 | 30 | 50 | 60 | 70 | 80 | 90 |
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.3 | 33.0 | 30.5 | 27.0 |
资料三:获得Fe3O4的反应原理为:Fe(OH)2+2Fe(OH)3
| ||
[问题讨论]
(1)溶解时,用50℃至80℃的热水目的是
(2)写出加入适量NaOH溶液时发生反应的化学方程式
(3)上述过程中,要控制“通一定量空气”的目的是
(4)要使四氧化三铁的产率最高,则上述流程中产生的Fe(OH)2和Fe(OH)3的最佳质量比为
(5)副产品P是硫酸钠,由溶液N获得该副产品的操作顺序是b→
a.过滤 b.加热浓缩 c.冷却结晶 d.晶体加热至完全失去结晶水
[组成确定]为确定用以上方法制得的四氧化三铁中可能含有的杂质,同学们又进行了下列实验探究.
[查阅资料]
资料一:难溶性碱受热时能分解产生金属氧化物和水(反应中各种元素的化合价不变);
资料二:Fe2O3和CO反应是随温度升高而逐步进行的,先生成Fe3O4,再生成FeO(黑色),最后生成Fe;
[提出猜想]Fe3O4中可能含有的杂质是Fe2O3和FeO中的一种或两种.
[实验设计]同学们称取了23.28g该Fe3O4样品进行了下列实验:
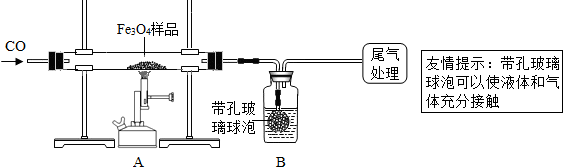
[实验分析]因探究思路不同,兴趣小组分成甲、乙两小组.
甲组:
(1)该组同学欲通过B装置反应前后的质量变化来计算确认该Fe3O4样品中的杂质.
B中的最佳试剂是
①澄清石灰水 ②氢氧化钠浓溶液 ③稀盐酸 ④水
(2)上述实验过程中,CO气体除作为反应物外,能起到的作用是:
①实验开始时,排尽装置中的空气,防止
②停止加热后,继续通CO气体,防止
在本实验中,CO气体还能起到的作用是③
(3)尾气如何处理?
乙组:
利用仪器测定并绘制成反应过程中A装置中玻璃管内的固体质量随温度的变化曲线(如图)
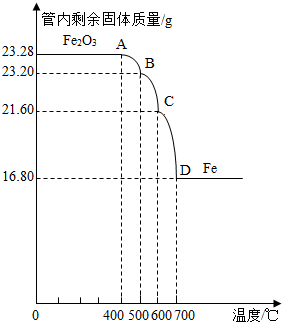
(1)写出BC段发生反应的化学方程式:
| ||
| ||
(2)通过分析计算确定:该Fe3O4样品中含有的杂质是
某同学利用化工厂的废碱液(主要成分为Na2CO3,还含有少量NaCl,其它杂质不计)和石灰乳为原料制备烧碱,并对所得的烧碱粗产品的成分进行分析和测定.
[粗产品制备](1)将废碱液加热蒸发浓缩,形成较浓的溶液,冷却后与石灰乳混合,发生反应的化学方程式为________.
(2)将反应后的混合物过滤,得到的滤液进行蒸发结晶,制得NaOH粗产品.
[粗产品成分分析](1)取适量粗产品溶于水,滴加Ba(NO3)2溶液出现白色浑浊,发生反应的化学方程式为________,该粗产品中一定不含有________,理由是________.
(2)该小组同学通过对粗产品成分的实验分析,确定该粗产品中含有三种物质.
[粗产品含量测定]Na2CO3含量的测定:
(1)该兴趣小组的同学设计了下图所示的实验装置.取10.0 g粗产品,进行实验.
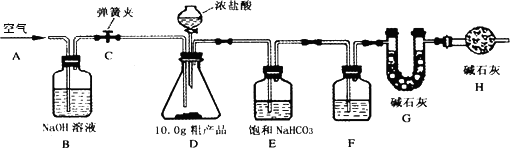
[说明]碱石灰是CaO与NaOH的固体混合物.E装置中的饱和NaHCO3溶液是为了除去二氧化碳气体中的氯化氢,发生的反应为NaHCO3+HC1=NaCl十CO2↑十H2O.
(2)操作步骤
①连接好装置,检查气密性;②打开弹簧夹C,在A处缓缓通入一段时间空气;③称量G的质量;④关闭弹簧夹C,慢慢滴加浓盐酸至过量,直至D中无气泡冒出;⑤打开弹簧夹C,再次缓缓通入一段时间空气;⑥再次称量G的质量,得前后两次质量差为0.48 g.
(3)问题探究 F中的试剂应为________,B装置的作用是________,H装置的作用是________.
若没有H装置,则测定的Na2CO3的质量分数会________(填“偏大”、“偏小”、“不变”).事实上10.0 g粗产品只能产生0.44 g CO2.请你仔细分析上述实验,解释实验值0.48 g比正确值0.44 g偏大的原因(假设操作均正确)________
(4)数据计算
根据正确值0.44 g可求得粗产品中Na2CO3的质量分数为________%.
NaOH含量的测定:该小组同学又另取10.0 g粗产品,逐滴加入20%的盐酸至恰好完全反应时,消耗盐酸的质量为36.5 g.放出CO2 0.44 g(不考虑二氧化碳气体的溶解).求原粗产品中NaOH的质量分数.(写出计算过程)
| 盐酸 | 大理石 | 温度条件 |
| 5% | 细颗粒 | 20℃ |
| 10% | 粗颗粒 | 40℃ |
| 每次用量均 | 每次用量均5g |
(1)实验小组同学设计的实验方案部分如下表,请根据表中信息帮助填写完整:
| 实验编号 | 温度 | 大理石规格 | HCl浓度 | 探究目的 |
| ① | 20℃ | 粗颗粒 | 5% | (I)实验①和②探究浓度对反应快慢的影响; (II)实验②和______探究温度对反应快慢的影响; (III)实验______和______探究大理石粗、细对反应快慢的影响. |
| ② | 20℃ | 粗颗粒 | ______ | |
| ③ | ______ | 细颗粒 | 5% | |
| ④ | 40℃ | ______ | 10% |
右图是根据某次实验数据作出的CO2和时间变化的关系曲.
请分析在80秒以后,产生CO2逐渐减慢的可能原因:
______.

 查看习题详情和答案>>
查看习题详情和答案>>
【查阅资料】
资料一:Fe粉和Fe3O4粉末能被磁铁吸引而FeO(黑色)不能;
资料二:Fe3O4中铁元素有+2、+3两种化合价,其化学式可用FeO?Fe2O3 的形式表示;
【提出猜想】黑色物质可能是Fe3O4、FeO和Fe粉中的一种或几种.
【进行实验】兴趣小组收集了CO与Fe2O3反应生成的黑色物质进行了下列实验:
| 实验方案 | 实验现象 | |
| 甲 | 取少量黑色物质用磁铁吸引 | 黑色物质全部被磁铁吸引 |
| 乙 | 取少量黑色物质加入30%热的盐酸中 | 无气泡、溶液颜色变成黄绿色 |
| 丙 | 取少量黑色物质加入硫酸铜溶液中 | 无任何现象 |
(1)甲实验现象说明黑色物质中没有
(2)生成的黑色物质应为Fe3O4;
(3)写出黑色粉末和热的盐酸反应的化学方程式
【拓展探究】同学们对Fe3O4产生了兴趣,从参考资料中找到了氧化沉淀法生产复印用高档Fe3O4粉的工艺流程简图.
【生产流程】
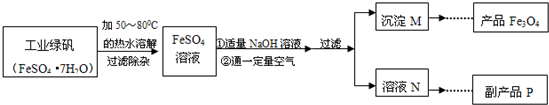
【查阅资料】
资料一:硫酸亚铁在不同温度下的溶解度如下表所示:
| 温度/℃ | 0 | 10 | 30 | 50 | 60 | 70 | 80 | 90 |
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.3 | 33.0 | 30.5 | 27.0 |
资料三:获得Fe3O4的反应原理为:Fe(OH)2+2Fe(OH)3
| ||
【问题讨论】
(1)溶解时,用50℃至80℃的热水目的是
(2)写出加入适量NaOH溶液时发生反应的化学方程式
(3)上述过程中,要控制“通一定量空气”的目的是
(4)要使四氧化三铁的产率最高,则上述流程中产生的Fe(OH)2和Fe(OH)3的最佳质量比为
(5)副产品P是硫酸钠,由溶液N获得该副产品的操作顺序是b→
a.过滤 b.加热浓缩 c.冷却结晶 d.晶体加热至完全失去结晶水
【组成确定】为确定用以上方法制得的四氧化三铁中可能含有的杂质,同学们又进行了下列实验探究.
【查阅资料】
资料一:难溶性碱受热时能分解产生金属氧化物和水(反应中各种元素的化合价不变);
资料二:Fe2O3和CO反应是随温度升高而逐步进行的,先生成Fe3O4,再生成FeO(黑色),最后生成Fe;
【提出猜想】Fe3O4中可能含有的杂质是Fe2O3和FeO中的一种或两种.
【实验设计】同学们称取了23.28g该Fe3O4样品进行了下列实验:
【实验分析】因探究思路不同,兴趣小组分成甲、乙两小组.
甲组:
(1)该组同学欲通过B装置反应前后的质量变化来计算确认该Fe3O4样品中的杂质.B中的最佳试剂是_
①澄清石灰水 ②氢氧化钠浓溶液 ③稀盐酸 ④水
(2)上述实验过程中,CO气体除作为反应物外,还能起到的作用是:①实验开始时,排尽装置中的空气,防止加热时发生爆炸;②停止加热后,防止A中生成物被氧化,B中的溶液倒吸入A中;③
(3)乙组同学认为B装置反应前后的
 质量差会偏小而影响计算、分析,你认为他们的理由是
质量差会偏小而影响计算、分析,你认为他们的理由是乙组:
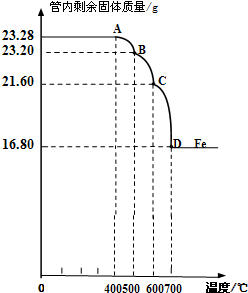
利用仪器测定并绘制成反应过程中A装置中玻璃管内的固体质量随温度的变化曲线(右图).
(1)写出BC段发生反应的化学方程式:
| ||
| ||
(2)通过计算确定:该Fe3O4样品中含有的杂质是