摘要:下列关于Na2CO3 和NaHCO3的叙述中.不正确的是A.两者都是碳酸盐 B.两者都能受热分解生成二氧化碳C.两者的水溶液pH都大于7 D.两者都能与过量的澄清石灰水反应生成白色沉淀
网址:http://m.1010jiajiao.com/timu_id_899651[举报]
18、以下是Na2CO3和NaHCO3的溶解度表及溶解度曲线.根据图表回答下列问题:
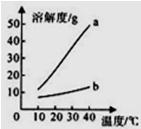

(1)Na2CO3的溶解度曲线应为
(2)欲使接近饱和的Na2CO3溶液变饱和,可采用的方法是
(3)已知Na2CO3转化为NaHCO3的反应为:Na2CO3+CO2+H2O=2NaHCO3,根据以上信息,向20℃饱和Na2CO3溶液中能入足量CO2气体,可观察到的现象是
查看习题详情和答案>>


(1)Na2CO3的溶解度曲线应为
a
(填“a”或“b”).(2)欲使接近饱和的Na2CO3溶液变饱和,可采用的方法是
降低温度
(3)已知Na2CO3转化为NaHCO3的反应为:Na2CO3+CO2+H2O=2NaHCO3,根据以上信息,向20℃饱和Na2CO3溶液中能入足量CO2气体,可观察到的现象是
有晶体析出.
(只写一种).(2005?海门市)已知碳酸氢钠不稳定,受热易分解2NaHCO3
Na2CO3+CO2↑+H2O.现取Na2CO3和NaHCO3的混合物10g,加热到质量不再改变为止,剩余固体质量为6.9g.下列说法正确的是( )
| ||
查看习题详情和答案>>
小明同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡.为了解其反应过程,他与学习小组的同学进行了如下探究.
教师提供了一瓶过碳酸钠(Na2CO4),小组同学进行了如下实验探究:

【提出问题】无色溶液X中的溶质有哪些物质?
【猜想与假设】根据以上实验现象,无色溶液X中一定存在的溶质是 .根据质量守恒定律,同学们对溶液X中还可能存在其它溶质,作出如下猜想:
①Na2CO3 ②NaHCO3 ③Na2CO3和NaHCO3的混合物
【查阅资料】
(1)氯化钙溶液呈中性;氯化钙溶液与碳酸氢钠溶液混合不发生反应;氯化钙溶液与碳酸钠溶液混合后发生如下反应:
Na2CO3+CaCl2═CaCO3↓+2NaCl
(2)NaHCO3溶液呈碱性,与石灰水反应生成白色沉淀;碳酸氢钠、碳酸钠与足量的酸反应产物相同.
(3)柠檬酸是一种有机酸,与盐酸具有类似的化学性质
【实验探究】小组同学对溶液X中的溶质进行了如下实验.请将下列实验方案填写完整.
【得出结论】综合上述两个探究活动的结果,同学们明确了上述猜想 (填序号)是正确的.
查看习题详情和答案>>
教师提供了一瓶过碳酸钠(Na2CO4),小组同学进行了如下实验探究:

【提出问题】无色溶液X中的溶质有哪些物质?
【猜想与假设】根据以上实验现象,无色溶液X中一定存在的溶质是
①Na2CO3 ②NaHCO3 ③Na2CO3和NaHCO3的混合物
【查阅资料】
(1)氯化钙溶液呈中性;氯化钙溶液与碳酸氢钠溶液混合不发生反应;氯化钙溶液与碳酸钠溶液混合后发生如下反应:
Na2CO3+CaCl2═CaCO3↓+2NaCl
(2)NaHCO3溶液呈碱性,与石灰水反应生成白色沉淀;碳酸氢钠、碳酸钠与足量的酸反应产物相同.
(3)柠檬酸是一种有机酸,与盐酸具有类似的化学性质
【实验探究】小组同学对溶液X中的溶质进行了如下实验.请将下列实验方案填写完整.
| 实验操作 | 实验现象 | 实验结论 |
| ①取溶液X适量于试管中,加入过量CaCl2 溶液 |
溶液中含 | |
| ②取①中反应后上层清液适量,加入适量 |
溶液中不含 |
已知碳酸氢钠不稳定,受热易分解(2NaHCO3
Na2CO3+H2O+CO2↑),现取Na2CO3和NaHCO3的混合物40g,加热到质量不再改变为止,剩余固体质量为27.6g,下列说法正确的是( )
| ||
| A、反应后生成CO2的质量为12.4g |
| B、反应后CO2和H2O的质量比为22:9 |
| C、原混合物中NaHCO3的质量为16.8g |
| D、原混合物中Na2CO3的质量分数为16% |