��Ŀ����
18��������Na2CO3��NaHCO3���ܽ�ȱ����ܽ�����ߣ�����ͼ���ش��������⣺
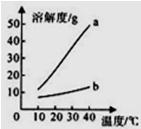

��1��Na2CO3���ܽ������ӦΪ
��2����ʹ�ӽ����͵�Na2CO3��Һ�䱥�ͣ��ɲ��õķ�����
��3����֪Na2CO3ת��ΪNaHCO3�ķ�ӦΪ��Na2CO3+CO2+H2O=2NaHCO3������������Ϣ����20�汥��Na2CO3��Һ����������CO2���壬�ɹ۲쵽��������


��1��Na2CO3���ܽ������ӦΪ
a
���a����b��������2����ʹ�ӽ����͵�Na2CO3��Һ�䱥�ͣ��ɲ��õķ�����
�����¶�
��3����֪Na2CO3ת��ΪNaHCO3�ķ�ӦΪ��Na2CO3+CO2+H2O=2NaHCO3������������Ϣ����20�汥��Na2CO3��Һ����������CO2���壬�ɹ۲쵽��������
���������
��ֻдһ�֣������������ܽ������ͼ��֪����ͬ������ͬһ�¶�ʱ���ܽ�ȴ�С�����Ҳ��֪��ͬһ�����ڲ�ͬ�¶�ʱ���ܽ�ȱ仯�����
����⣺��1����ͼ����֪��̼���Ƶ��ܽ����ͬһ�¶�ʱ��̼�����Ƶ��ܽ�ȴ�����a��ʾ̼���Ƶ��ܽ�ȣ�
��2�����ܽ������ͼ��֪��̼���Ƶ��ܽ�����¶ȵ����߶����ߣ�������ʹ�ӽ����͵�Na2CO3��Һ�䱥�ͣ��ɲ��ý����¶ȵķ�����
��3����ͼ����֪��̼�����Ƶ��ܽ�ȱ�̼���Ƶ��ܽ��С�����Ե�ͨ�������̼ʱ��������̼��̼��������̼�����ƣ�̼�����Ƶ��ܽ��С�������д����ľ���������
�ʴ�Ϊ��
��1��a��
��2�����£�
��3�����������
��2�����ܽ������ͼ��֪��̼���Ƶ��ܽ�����¶ȵ����߶����ߣ�������ʹ�ӽ����͵�Na2CO3��Һ�䱥�ͣ��ɲ��ý����¶ȵķ�����
��3����ͼ����֪��̼�����Ƶ��ܽ�ȱ�̼���Ƶ��ܽ��С�����Ե�ͨ�������̼ʱ��������̼��̼��������̼�����ƣ�̼�����Ƶ��ܽ��С�������д����ľ���������
�ʴ�Ϊ��
��1��a��
��2�����£�
��3�����������
������̼�����Ʊ�̼���Ƶ��ܽ��С�����������ں�ˮ�Ƽ�ʱ���ڱ��Ͱ���ˮ��ͨ�������̼ʱ�����о���������

��ϰ��ϵ�д�
 �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д� Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�
�����Ŀ
������Na2CO3��NaHCO3���ܽ�ȱ����ܽ�����ߣ�����ͼ���ش��������⣺
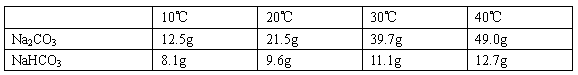
| 10�� | 20�� | 30�� | 40�� | |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
 ��1��Na2CO3���ܽ������ӦΪ________���a����b������
��1��Na2CO3���ܽ������ӦΪ________���a����b��������2����ʹ�ӽ����͵�Na2CO3��Һ�䱥�ͣ��ɲ��õķ�����________��
��3����֪Na2CO3ת��ΪNaHCO3�ķ�ӦΪ��Na2CO3+CO2+H2O=2NaHCO3������������Ϣ����20�汥��Na2CO3��Һ����������CO2���壬�ɹ۲쵽��������________��ֻдһ�֣���
������Na2CO3��NaHCO3���ܽ�ȱ����ܽ�����ߣ�����ͼ���ش��������⣺
��1��Na2CO3���ܽ������ӦΪ______���a����b������
��2����ʹ�ӽ����͵�Na2CO3��Һ�䱥�ͣ��ɲ��õķ�����______��
��3����֪Na2CO3ת��ΪNaHCO3�ķ�ӦΪ��Na2CO3+CO2+H2O=2NaHCO3������������Ϣ����20�汥��Na2CO3��Һ����������CO2���壬�ɹ۲쵽��������______��ֻдһ�֣���

| 10�� | 20�� | 30�� | 40�� | |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
��2����ʹ�ӽ����͵�Na2CO3��Һ�䱥�ͣ��ɲ��õķ�����______��
��3����֪Na2CO3ת��ΪNaHCO3�ķ�ӦΪ��Na2CO3+CO2+H2O=2NaHCO3������������Ϣ����20�汥��Na2CO3��Һ����������CO2���壬�ɹ۲쵽��������______��ֻдһ�֣���

������Na2CO3��NaHCO3���ܽ�ȱ����ܽ�����ߣ�����ͼ���ش��������⣺
��1��Na2CO3���ܽ������ӦΪ______���a����b������
��2����ʹ�ӽ����͵�Na2CO3��Һ�䱥�ͣ��ɲ��õķ�����______��
��3����֪Na2CO3ת��ΪNaHCO3�ķ�ӦΪ��Na2CO3+CO2+H2O=2NaHCO3������������Ϣ����20�汥��Na2CO3��Һ����������CO2���壬�ɹ۲쵽��������______��ֻдһ�֣���

| 10�� | 20�� | 30�� | 40�� | |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
��2����ʹ�ӽ����͵�Na2CO3��Һ�䱥�ͣ��ɲ��õķ�����______��
��3����֪Na2CO3ת��ΪNaHCO3�ķ�ӦΪ��Na2CO3+CO2+H2O=2NaHCO3������������Ϣ����20�汥��Na2CO3��Һ����������CO2���壬�ɹ۲쵽��������______��ֻдһ�֣���