摘要:(1)该试剂瓶中硫酸溶液的质量是 g.现要将100g这种浓硫酸稀释为质量分数为20%的硫酸.需要水的质量是 g.
网址:http://m.1010jiajiao.com/timu_id_890383[举报]
 现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.
现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.
(1)H2SO4的相对分子质量是
98
98
.(2)H2SO4分子中,H、S、O的原子个数比为
2:1:4
2:1:4
.(3)该瓶浓硫酸的质量为
920
920
g.(4)用100g98%的该浓硫酸稀释成19.6%的稀硫酸,需要水多少g?
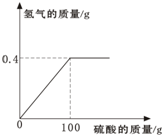
(5)某同学用锌粒与19.6%的稀硫酸反应制取氢气,反应所用的稀硫酸和生成氢气的关系如右图.
计算:
①至少需要多少g的锌粒?
②完全反应后所得溶液的溶质质量分数为多少?(保留一位小数点)
实验室中浓硫酸的商标如图所示。请根据有关信息计算:

(1)该试剂瓶中硫酸溶液的质量是 _____ g。
(2)欲配制100g溶质质量分数为19.6%的稀硫酸,需这种浓硫酸多少克?
查看习题详情和答案>>
(2)欲配制100g溶质质量分数为19.6%的稀硫酸,需这种浓硫酸多少克?
| |||||||||||||||


