题目内容
 现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.
现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.
(1)H2SO4的相对分子质量是
98
98
.(2)H2SO4分子中,H、S、O的原子个数比为
2:1:4
2:1:4
.(3)该瓶浓硫酸的质量为
920
920
g.(4)用100g98%的该浓硫酸稀释成19.6%的稀硫酸,需要水多少g?
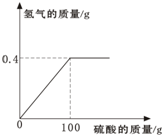
(5)某同学用锌粒与19.6%的稀硫酸反应制取氢气,反应所用的稀硫酸和生成氢气的关系如右图.
计算:
①至少需要多少g的锌粒?
②完全反应后所得溶液的溶质质量分数为多少?(保留一位小数点)
分析:(1)根据相对分子质量为各元素相对原子质量的和来计算硫酸的相对分子质量即可;
(2)利用化学式中各元素原子的角码判断分子中原子的个数比即可;
(3)依据密度公式ρ=
的变形可知该瓶硫酸的质量;
(4)使用98%的浓硫酸配制19.6%的稀硫酸需要进行加水稀释,加水稀释前后溶质硫酸的质量不变;根据溶质质量不变,由稀硫酸的质量可计算配制时所需要浓硫酸的质量和水的质量;
(5)依据图象中生成的氢气质量(或硫酸的质量)结合化学方程式的计算可求反应的锌的质量和生成的硫酸锌质量,据此进行计算即可.
(2)利用化学式中各元素原子的角码判断分子中原子的个数比即可;
(3)依据密度公式ρ=
| m |
| v |
(4)使用98%的浓硫酸配制19.6%的稀硫酸需要进行加水稀释,加水稀释前后溶质硫酸的质量不变;根据溶质质量不变,由稀硫酸的质量可计算配制时所需要浓硫酸的质量和水的质量;
(5)依据图象中生成的氢气质量(或硫酸的质量)结合化学方程式的计算可求反应的锌的质量和生成的硫酸锌质量,据此进行计算即可.
解答:解:(1)相对分子质量为各元素相对原子质量的和,所以H2SO4的相对分子质量=2×1+32+16×4=98;
(2)化学式中各元素原子的角码之比即是分子中原子的个数比,所以H2SO4分子中,H、S、O的原子个数比为2:1:4;
(3)依据密度公式ρ=
的变形可知m=ρV,所以该瓶硫酸的质量=1.84g/cm3×500ml=920g;
(4)解:设需要水质量为x
100g×98%=(100g+x)×19.6%
x=400g
(5)解:①设需要锌的质量为x,生成ZnSO4质量为y
H2SO4+Zn=ZnSO4+H2↑
65 161 2
x y 0.4g
=
=
x=13g
y=32.2g
②反应后所得溶液的质量为:100g+13g-0.4g,所以其溶质的质量分数为
×100%=28.6%
故答案为:(1)98;(2)2:1:4;(3)920;(4)答:需要水400g;(5)答:至少需要13g锌粒;②完全反应后所得溶液的溶质质量分数为28.6%.
(2)化学式中各元素原子的角码之比即是分子中原子的个数比,所以H2SO4分子中,H、S、O的原子个数比为2:1:4;
(3)依据密度公式ρ=
| m |
| v |
(4)解:设需要水质量为x
100g×98%=(100g+x)×19.6%
x=400g
(5)解:①设需要锌的质量为x,生成ZnSO4质量为y
H2SO4+Zn=ZnSO4+H2↑
65 161 2
x y 0.4g
| 65 |
| x |
| 2 |
| 0.4g |
| 161 |
| y |
x=13g
y=32.2g
②反应后所得溶液的质量为:100g+13g-0.4g,所以其溶质的质量分数为
| 32.2g |
| (100+13-0.4)g |
故答案为:(1)98;(2)2:1:4;(3)920;(4)答:需要水400g;(5)答:至少需要13g锌粒;②完全反应后所得溶液的溶质质量分数为28.6%.
点评:此题是对与稀硫酸相关的问题考查,解题的关键点和易错点是求反应后溶液的质量,解决的关键是依据质量守恒定律,反应后所得溶液的质量=参加反应金属锌的质量+消耗稀硫酸的质量-反应放出氢气的质量.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
 现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.请根据有关信息回答并计算:
现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.请根据有关信息回答并计算:| 硫酸(500mL) 品 名 硫酸 化学式 H2SO4 相对分子质量98 密 度 1.84g/cm3 质量分数98% (1)硫酸由 氢 氢 元素、硫 硫 元素、氧 氧 元素组成,它含氧元素,它不是 不是 (是、不是)氧化物;磷酸相对分子质量为98 98 ;你认为硫酸与磷酸含氧元素质量相等的条件是硫酸和磷酸的质量相等 硫酸和磷酸的质量相等 ;(2)该试剂瓶中硫酸溶液的质量是 920 920 g.(3)工会主席王赐用20g该浓硫酸配制20%的稀硫酸,以清洗钢铁表面的铁锈.他在配制该溶液时所用98%的浓硫酸与水的质量比应该为 10:39 10:39 .(4)某固体物质由氯化钠和氯化钡组成,取32.8g该固体混合物完全溶于水,并逐滴加入上述20%的稀硫酸,产生沉淀的质量与加入稀硫酸的质量有如图所示关系,计算32.8g固体混合物中氯化钠和氯化钡的质量. (5)若加入的稀硫酸刚好使沉淀达最大量时,将所得混合物过滤、洗涤,得滤液并将其稀释至200g(过程中损耗忽略不计),计算该滤液中溶质的质量分数为 氯化钠的质量分数为6%,氯化氢的质量分数为3.65% 氯化钠的质量分数为6%,氯化氢的质量分数为3.65% .(若溶液中含有多种溶质,则每种溶质的质量分数为该溶质的质量与溶液总质量之比)[注:(3)、(4)两问需写出计算过程].(6)喜欢探究又善于思考的周泽坤出这样题目考大家:把30g含Fe、Al、Mg、Zn的金属粉末投入适量的稀硫酸中全部溶解完,再将溶液蒸干得无水干燥固体126g,则同时产生的氢气质量为 2 2 g;探究中泽坤发现:用相同浓度的硫酸,与一瓶未变质、部分变质、全变质(杂质都是氢氧化钙)的生石灰样品反应,需要的硫酸质量都相等,其原因是氧化钙和碳酸钙都是每40g钙元素生成136g硫酸钙,消耗98g硫酸 氧化钙和碳酸钙都是每40g钙元素生成136g硫酸钙,消耗98g硫酸 .
|
| 实验次数 | 1 | 2 | 3 |
| 合金质量(g) | 10 | 10 | 10 |
| 稀硫酸质量(g) | 25 | 50 | 75 |
| 产生氢气的质量(g) | 0.1 | 0.2 | 0.2 |
 某校化学课外活动小组的同学需要一些硫酸做化学实验.现有一瓶未开启的浓硫酸,标签如图.请阅读标签上的说明,回答下列问题.
某校化学课外活动小组的同学需要一些硫酸做化学实验.现有一瓶未开启的浓硫酸,标签如图.请阅读标签上的说明,回答下列问题. 某校化学课外活动小组的同学需要一些硫酸做化学实验.现有一瓶未开启的浓硫酸,标签如图.请阅读标签上的说明,回答下列问题.
某校化学课外活动小组的同学需要一些硫酸做化学实验.现有一瓶未开启的浓硫酸,标签如图.请阅读标签上的说明,回答下列问题.
