摘要:课本习题一.三,1.2●板书设计第一节 氧族元素一.氧族元素原子结构与元素性质递变的关系二.氧族元素与同周期卤族元素的非金属性比较原子半径:氧族>卤族非金属性:氧族<卤族●教学说明氧族元素之前已学习过碱金属元素与卤族元素.对族元素的原子结构的特点和性质变化已有一定的了解.加上刚刚学完原子结构和元素周期律知识.因此.对氧族元素的学习可以说是原子结构.元素周期律的应用.为此.本节课首先组织学生根据氧族元素在周期表中的位置.运用元素周期律理论对原子结构特点及元素性质变化规律进行了大胆的推测.而后分析了课本所列相关数据与反应事实.最终验证了理论推测的正确性.由此.让学生真正体会到科学理论的指导作用.初步学会了运用理论知识指导学习元素化合物的方法.同时又是对学生思维.分析.推测能力的训练.本节第二部分着重对比了氧族元素与同周期卤族元素的非金属性.这一内容重在考查学生对已有知识的掌握和解决问题的能力.因此.将其设为难点.特以S.Cl2分别与变价金属Fe.Cu的反应为例作分析比较.得出了氧族元素比相应卤族元素非金属性弱的事实.后又引导学生用原子结构知识进行了解释.以突出结构对性质的决定性作用.强化了学生结构决定性质的思想.本节设计的主旨是:给学生以思想,给学生以方法,给学生以充分活动的时间与空间.以培养学生的能力为最终目的.
网址:http://m.1010jiajiao.com/timu_id_6819[举报]
下列①~⑨是元素周期表的前三周期中的部分元素,请从这些元素中选择填空:
(1)上述元素中,化学性质最稳定的是:
(2)⑥和⑦两种元素的最高价氧化物对应的水化物都是碱,则这两种碱的碱性强弱为:NaOH
(3)元素③和元素⑤形成的氢化物中,稳定性较强的是:
(4)画出元素②的原子结构示意图:
 ;
;
(5)元素①和元素⑧的单质均为气态,两气体在一定条件下反应之后的产物可溶于蒸馏水,此水溶液呈
查看习题详情和答案>>
族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
Ar
Ar
(填元素符号);(2)⑥和⑦两种元素的最高价氧化物对应的水化物都是碱,则这两种碱的碱性强弱为:NaOH
>
>
Mg(OH)2(填“>”、“<”或“=”);(3)元素③和元素⑤形成的氢化物中,稳定性较强的是:
HF
HF
(填化学式);(4)画出元素②的原子结构示意图:


(5)元素①和元素⑧的单质均为气态,两气体在一定条件下反应之后的产物可溶于蒸馏水,此水溶液呈
酸
酸
性(填“酸”、“碱”或“中”).表为元素周期表的一部分.
(1)表中元素 的非金属性最强;元素 的金属性最强;除稀有气体外表中原子半径最小的是 (填写元素符号);
(2)表中元素⑧的原子结构示意图是 ;
(3)表中元素⑨和⑩最高价氧化物对应水化物的酸性: > .
(4)最高价氧化物是两性氧化物的元素是 (填元素符号);写出它的氧化物的化学式: .
查看习题详情和答案>>
族 周期 |
ⅠA | ⅡB | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 三 | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)表中元素⑧的原子结构示意图是
(3)表中元素⑨和⑩最高价氧化物对应水化物的酸性:
(4)最高价氧化物是两性氧化物的元素是
如图是元素周期表的一部分,针对表中的①至⑩号元素,请按照要求回答以下问题.
(1)①至⑩号元素形成的气态氢化物中最稳定的是
(2)元素②和⑨,非金属性较强的是
(3)均由①④⑥⑨四种元素组成的两种化合物发生反应,能产生一种气体,该反应的化学方程式是:
(4)元素④的某一种氢化物常温下呈液态(每个分子由18个电子),将该氢化物滴到氯化亚铁溶液中,溶液的颜色发生明显变化,请写出该反应的离子方程式:
(5)元素⑥和⑨组成的化合物溶于水,溶液呈
(6)能说明非金属性⑤比⑩强的是
A.单质与氢气化合,⑤比⑩容易; B.最高价氧化物对应的水化物的酸性,⑤比⑩强;
C.气态氢化物的稳定性,⑤比⑩强; D.单质⑤能在水溶液中置换出单质⑩.
(7)元素⑧与⑩形成的化合物有两种,其中一种化合物各原子最外层均达到了8电子的稳定结构,该化合物的化学式为
查看习题详情和答案>>
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
HF
HF
(填氢化物的化学式);(2)元素②和⑨,非金属性较强的是
硫
硫
(填元素名称),请用一个离子方程式来说明这个结论:CO32-+2H+═H2O+CO2↑或HCO3-+H+═H2O+CO2↑
CO32-+2H+═H2O+CO2↑或HCO3-+H+═H2O+CO2↑
;(3)均由①④⑥⑨四种元素组成的两种化合物发生反应,能产生一种气体,该反应的化学方程式是:
NaHSO3+NaHSO4═Na2SO4+H2O+SO2↑
NaHSO3+NaHSO4═Na2SO4+H2O+SO2↑
;(4)元素④的某一种氢化物常温下呈液态(每个分子由18个电子),将该氢化物滴到氯化亚铁溶液中,溶液的颜色发生明显变化,请写出该反应的离子方程式:
2Fe2++H2O2+2H+═2Fe3++2H20
2Fe2++H2O2+2H+═2Fe3++2H20
;(5)元素⑥和⑨组成的化合物溶于水,溶液呈
碱性
碱性
(填“酸性”、“中性”或“碱性”),其原因是S2-+H2O?HS-+OH-
S2-+H2O?HS-+OH-
(用离子方程式表达),溶液中的各种离子按照浓度由大到小排列顺序是:Na+>S2->OH->HS->H+
Na+>S2->OH->HS->H+
.(6)能说明非金属性⑤比⑩强的是
AC
AC
.A.单质与氢气化合,⑤比⑩容易; B.最高价氧化物对应的水化物的酸性,⑤比⑩强;
C.气态氢化物的稳定性,⑤比⑩强; D.单质⑤能在水溶液中置换出单质⑩.
(7)元素⑧与⑩形成的化合物有两种,其中一种化合物各原子最外层均达到了8电子的稳定结构,该化合物的化学式为
PCl3
PCl3
.
下表是元素周期表的一部分,试根据元素周期律完成下列问题。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
一 | ① |
|
|
|
|
|
|
二 | ② | ③ | ④ |
| ⑤ | ⑥ |
|
三 |
| ⑦ | ⑧ |
|
| ⑨ | ⑩ |
(1)表中元素⑩的氢化物的化学式为________________,此氢化物的还原性比元素⑨的氢化物的还原性________________。(填“强”或“弱”)
(2)某元素原子的核外K层电子数比L层电子数少5,则该元素的元素符号是__________,其单质与⑦的反应方程式为_______________________________________________________。
(3)俗称为“矾”的一类化合物通常含有共同的元素是________________________。
(4)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式____________________________________________________________。
又如表中与元素⑦的性质相似的不同族元素是____________。(填元素符号)
(14分)下表为元素周期表的一部分,请参照元素①一⑧在表中的位置,回答下列问题:
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 一 | ① | | ||||||
| 二 | | | | ② | ③ | ④ | | |
| 三 | ⑤ | | ⑥ | ⑦ | | ⑧ | | |
(2)由表中元素可以组成多种漂白剂,试写出其中两种常用漂白剂的化学式: 、 。
(3)①、④、⑤三种元素形成的化合物中化学键的类型: 。
(4)②和④形成的化合物与④和⑤形成的化合物之间发生氧化还原反应,写出该反应的化学方程式: 。
(5)由表中元素形成的常见物质X、Y、Z、M、W可发生以下反应:
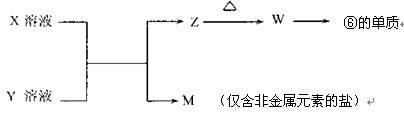
①X溶液与Y溶液反应的离子方程式为 ;
②已知M为硝酸盐,则M溶液中各离子浓度由大到小排列顺序为:
c( )>c( )>c( )>c( )(在括号内填离子符号)。 查看习题详情和答案>>