摘要:9g×0.4 0.040xmol x=3.35mol/L设置几组不同浓度硫酸的对照实验.步骤:1用热碱液洗废铁屑2次.玻棒搅拌.再用蒸馏水冲洗2烧杯中倒入40ml稀硫酸.加入足量废铁屑.使稀硫酸浸没所有铁屑.小心加热.直到有极少量气泡产生.溶液呈浅绿色.烧杯底部仍留有少量铁屑.3用少量热水通过过滤器.然后将溶液趁热过滤.4将滤液转入试管.用橡皮塞塞住管口.静置冷却结晶5将混合物倒入烧杯.取出晶体.用少量水洗涤2-3次.再用滤纸吸干.放在小广口瓶中.密闭保存.第五讲 定量实验 仪器: 天平.烧杯.玻棒.容量瓶.滴管 步骤:(1) 计算 (2) 称量或量取 (3) 溶解 (4) 转移.洗涤 (5) 定容.摇匀 ①小结实验的注意点:1检漏2称量3冷却4转移完全5定容平视凹面最低处②哪些因素可能引起误差.偏差如何?1容量瓶摇匀时漏水未补加 偏大2溶液未冷却转移 偏大 3定容时俯视 偏大 4滴水过量 偏小③弱酸强碱盐如AlCl3溶液配制时要采取什么特殊措施?加少量稀盐酸还原性物质如FeSO4呢? 加少量稀硫酸和铁粉 二.溶解度测定设计实验测定10℃ KNO3的溶解度(1)测定10℃ KNO3的溶解度必需的条件是什么?10℃100g水最多能溶解KNO3的质量(2)如何保证温度为10℃?水浴加热(3)怎样测得10℃时100g水能溶解KNO3最多克数?评价下列两个方案:①在天平上称出一定量KNO3晶体.往10℃的100g水中慢慢撒入KNO3.一边不断搅拌.当KNO3不再溶解时已饱和.称量剩下的KNO3的质量.前后两次KNO3质量之差便是10℃KNO3的溶解度.(原则上是对的.但费时.实际行不通)②量好100g水.保持10℃.一次加入定额过量的KNO3晶体.搅拌几分钟.保证达饱和.把溶液倒出.称量未溶的KNO3.计算溶解度.晶体上沾有水.实际上是沾有溶液.蒸发掉也不准确 你设计的实验步骤:取10ml水.加入KNO3晶体.搅拌.配成10℃饱和溶液.取饱和溶液称量后蒸发去水分.称量剩下的KNO3晶体. 内低外高水浴热 温度计在试管中 溶液饱和防溅失干燥器中冷却成 三.硫酸铜结晶水含量测定
网址:http://m.1010jiajiao.com/timu_id_572537[举报]
一定条件下将1mol A和1mol B投入一密闭容器中发生如下反应A(g)+B(g)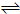 xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.
xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.
(1)若x=1,在恒温恒容时,共有C
(2)若x=1,在恒温恒压时,共有C
(3)若x=2,共有C
(4)若x=3,在恒温恒容时,共有C
查看习题详情和答案>>
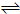 xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.
xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.(1)若x=1,在恒温恒容时,共有C
大于
大于
2amol,C的体积分数大于
大于
W%.(2)若x=1,在恒温恒压时,共有C
等于
等于
2amol,C的体积分数等于
等于
W%.(3)若x=2,共有C
等于
等于
2amol,C的体积分数等于
等于
W%.(4)若x=3,在恒温恒容时,共有C
小于
小于
2amol,C的体积分数小于
小于
W%.
一定条件下将1mol A和1mol B投入一密闭容器中发生如下反应A(g)+B(g)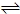 xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.
xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.
(1)若x=1,在恒温恒容时,共有C 2amol,C的体积分数 W%.
(2)若x=1,在恒温恒压时,共有C 2amol,C的体积分数 W%.
(3)若x=2,共有C 2amol,C的体积分数 W%.
(4)若x=3,在恒温恒容时,共有C 2amol,C的体积分数 W%. 查看习题详情和答案>>
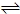 xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.
xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.(1)若x=1,在恒温恒容时,共有C 2amol,C的体积分数 W%.
(2)若x=1,在恒温恒压时,共有C 2amol,C的体积分数 W%.
(3)若x=2,共有C 2amol,C的体积分数 W%.
(4)若x=3,在恒温恒容时,共有C 2amol,C的体积分数 W%. 查看习题详情和答案>>
一定条件下将1mol A和1mol B投入一密闭容器中发生如下反应A(g)+B(g)

xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.
(1)若x=1,在恒温恒容时,共有C______2amol,C的体积分数______W%.
(2)若x=1,在恒温恒压时,共有C______2amol,C的体积分数______W%.
(3)若x=2,共有C______2amol,C的体积分数______W%.
(4)若x=3,在恒温恒容时,共有C______2amol,C的体积分数______W%.
查看习题详情和答案>>

xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.
(1)若x=1,在恒温恒容时,共有C______2amol,C的体积分数______W%.
(2)若x=1,在恒温恒压时,共有C______2amol,C的体积分数______W%.
(3)若x=2,共有C______2amol,C的体积分数______W%.
(4)若x=3,在恒温恒容时,共有C______2amol,C的体积分数______W%.