题目内容
一定条件下将1mol A和1mol B投入一密闭容器中发生如下反应A(g)+B(g)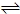 xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.
xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.(1)若x=1,在恒温恒容时,共有C 2amol,C的体积分数 W%.
(2)若x=1,在恒温恒压时,共有C 2amol,C的体积分数 W%.
(3)若x=2,共有C 2amol,C的体积分数 W%.
(4)若x=3,在恒温恒容时,共有C 2amol,C的体积分数 W%.
【答案】分析:(1)达到平衡时,再投1mol A和1mol B,可等效为开始投入2mol A和2mol B,即压强增大为原来的2倍,与原平衡相比,增大压强,平衡向气体体积减小的方向移动,即向正反应移动,反应物转化率增大,C的体积分数增大.
(2)达到平衡时,再投1mol A和1mol B,可等效为开始投入2mol A和2mol B,在恒温恒压,A、B的物质的量之比与原平衡相同,两平衡等效,转化率不变,各组分含量相同.
(3)达到平衡时,再投1mol A和1mol B,可等效为开始投入2mol A和2mol B,反应前后气体体积不变,A、B的物质的量之比与原平衡相同,两平衡等效,转化率不变,各组分含量相同.
(4)达到平衡时,再投1mol A和1mol B,可等效为开始投入2mol A和2mol B,即压强增大为原来的2倍,与原平衡相比,增大压强,平衡向气体体积减小的方向移动,即向逆反应移动,反应物转化率降低,C的体积分数减小.
解答:解:达到平衡时,再投1mol A和1mol B,可等效为开始投入2mol A和2molB,
(1)恒温恒容,压强增大为原来的2倍,与原平衡相比,增大压强,平衡向气体体积减小的方向移动,即向正反应移动,反应物转化率增大,C大于2amol,C的体积分数增大,C的体积分数大于W%,故答案为:大于;大于;
(2)在恒温恒压,A、B的物质的量之比与原平衡相同,两平衡等效,转化率不变,C等于2amol,各组分含量相同,C的体积分数等于W%,故答案为:等于;等于;
(3)反应前后气体体积不变,A、B的物质的量之比与原平衡相同,两平衡等效,转化率不变,C等于2amol,各组分含量相同,C的体积分数 等于W%,故答案为:等于;等于;
(4)恒温恒容,压强增大为原来的2倍,与原平衡相比,增大压强,平衡向气体体积减小的方向移动,即向逆反应移动,反应物转化率降低,C小于2amol,C的体积分数减小,C的体积分数小于W%,故答案为:小于;小于.
点评:考查等效平衡,难度较大,理解等效平衡规律:1、恒温恒容,反应前后气体体积不等,按化学计量数转化一边,对应物质满足等量;反应前后气体体积相等,按化学计量数转化一边,对应物质满足对比;
2:恒温恒压,按化学计量数转化一边,对应物质满足对比.
(2)达到平衡时,再投1mol A和1mol B,可等效为开始投入2mol A和2mol B,在恒温恒压,A、B的物质的量之比与原平衡相同,两平衡等效,转化率不变,各组分含量相同.
(3)达到平衡时,再投1mol A和1mol B,可等效为开始投入2mol A和2mol B,反应前后气体体积不变,A、B的物质的量之比与原平衡相同,两平衡等效,转化率不变,各组分含量相同.
(4)达到平衡时,再投1mol A和1mol B,可等效为开始投入2mol A和2mol B,即压强增大为原来的2倍,与原平衡相比,增大压强,平衡向气体体积减小的方向移动,即向逆反应移动,反应物转化率降低,C的体积分数减小.
解答:解:达到平衡时,再投1mol A和1mol B,可等效为开始投入2mol A和2molB,
(1)恒温恒容,压强增大为原来的2倍,与原平衡相比,增大压强,平衡向气体体积减小的方向移动,即向正反应移动,反应物转化率增大,C大于2amol,C的体积分数增大,C的体积分数大于W%,故答案为:大于;大于;
(2)在恒温恒压,A、B的物质的量之比与原平衡相同,两平衡等效,转化率不变,C等于2amol,各组分含量相同,C的体积分数等于W%,故答案为:等于;等于;
(3)反应前后气体体积不变,A、B的物质的量之比与原平衡相同,两平衡等效,转化率不变,C等于2amol,各组分含量相同,C的体积分数 等于W%,故答案为:等于;等于;
(4)恒温恒容,压强增大为原来的2倍,与原平衡相比,增大压强,平衡向气体体积减小的方向移动,即向逆反应移动,反应物转化率降低,C小于2amol,C的体积分数减小,C的体积分数小于W%,故答案为:小于;小于.
点评:考查等效平衡,难度较大,理解等效平衡规律:1、恒温恒容,反应前后气体体积不等,按化学计量数转化一边,对应物质满足等量;反应前后气体体积相等,按化学计量数转化一边,对应物质满足对比;
2:恒温恒压,按化学计量数转化一边,对应物质满足对比.

练习册系列答案
相关题目
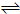 xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.
xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果. (2010?郑州一模)如图所示,一定条件下将1mol A2气体和3molB2气体充入一容积可变的密闭容器中,可滑动的活塞的位置如图1所示.在恒温恒压下发生如下反应:A2+3B2?2AB3.当反应达到平衡时,活塞位置如图2所示,则平衡时A的转化率是( )
(2010?郑州一模)如图所示,一定条件下将1mol A2气体和3molB2气体充入一容积可变的密闭容器中,可滑动的活塞的位置如图1所示.在恒温恒压下发生如下反应:A2+3B2?2AB3.当反应达到平衡时,活塞位置如图2所示,则平衡时A的转化率是( )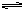 CO2(g)+H2(g),达到平衡时测得CO2为0.6mol。再通入4mol H2O(g),达到新平衡后,CO2的物质的量为
CO2(g)+H2(g),达到平衡时测得CO2为0.6mol。再通入4mol H2O(g),达到新平衡后,CO2的物质的量为