网址:http://m.1010jiajiao.com/timu_id_555492[举报]
Ⅰ.甲组方案:
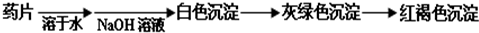
(提示:白色的Fe(OH)2在空气中会迅速变成灰绿色,最后变成红褐色)
甲组同学按照设计的方案完成实验,但遗憾的是他们没有得到预期的实验结果.分析甲组实验失败的可能原因:
Ⅱ.乙组同学在参考书上查得如下资料:
①人体胃液中有大量盐酸,能溶解多种物质.
②H2O2不稳定,光照、加热和微量杂质会促使其分解;H2O2中氧元素为-1价,它既有氧化性又有还原性.
他们认真思考了甲组实验失败的原因,模拟药服用后在人体中溶解的变化过程,重新设计并完成下列实验:
乙组方案:
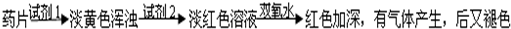
(1)试剂1为:
(2)加入试剂2后,溶液显淡红色的原因是:
(3)加双氧水后,红色加深的原因是:
Ⅲ.丙组同学对乙组实验中最后红色褪去的现象产生了浓厚的兴趣,欲探究其褪色的原因.根据粒子的组成,他们认为有两种可能原因:①[Fe(SCN)]2+中的三价铁被还原为亚铁;②
请你对其中一种可能进行实验验证:
实验方案(用文字叙述):
根据预期现象判断结论:
或在褪色后溶液中加入KSCN溶液
现象:变红色结论:褪色原因是因为②;不变红色结论:褪色原因是因为①
或在褪色后溶液中加入KSCN溶液
现象:变红色结论:褪色原因是因为②;不变红色结论:褪色原因是因为①
常见元素A、B、M组成的四种物质发生反应:甲+乙=丙+丁,其中甲由A和M组成,乙由B和M组成,丙只含有M。
(1)若甲为淡黄色固体,乙和丙均为常温下的无色无味气体。则乙的电子式为 ;生成标准状况下5.6L丙转移的电子数为 ;常温下丁溶液pH 7,用离子方程式解释 。
(2)若丁为能使品红褪色的无色气体,丙为常见红色金属,化合物甲、乙中原子个数比均为1:2(M均显+1价),原子序数B大于A。则①A在周期表中位置为 ②丁与水反应的化学方程式为 向反应后溶液中滴加两滴紫色石蕊试液的现象为
③正确书写上述生成丙的化学方程式
④向MCl2的溶液中通入丁,可观察到白色的MCl沉淀,写出该反应的离子方程式 。
查看习题详情和答案>>
常见元素X、Y、Z、W的原子序数依次增大,其相关信息如下表:
|
元素 |
相关信息 |
|
X |
X的基态原子核外只有三个能级,且各能级电子数相等 |
|
Y |
Y的基态原子最外层电子数是其内层电子总数的2.5倍 |
|
Z |
Z的基态价电子结构为nsn-1 |
|
W |
W单质常在火山口附近被发现,其氧化物是造成酸雨的主要原因之一 |
(1)Y位于元素周期表第 周期 族,其基态原子未成对电子有 个。
(2)X的电负性比W的 (填“大”或“小”);Y的最简单气态氢化物比X的最简单气态氢化物易液化,其主要原因是 。
(3)Z与同周期左右相邻的两种元素的原子相比较,三者第一电离能由大到小的顺序为 (用元素符号表示)。Y和Z形成的化合物为 晶体,该物质遇水强烈水解的化学方程式为 。
(4)在一定温度下,向一个容积不变的密闭容器中充入1molY2和3mol氢气,发生反应:Y2(g)+3H2(g) 2YH3(g) ΔH=-akJ/mol。在该条件下达到平衡时放出的热量为bkJ,其平衡常数表达式K= 。若起始向此容器中充入2molYH3,在相同温度下达到平衡时,反应过程中吸收的热量为ckJ,则a、b、c三者之间的关系为 (用一个式子表示)。
查看习题详情和答案>>
常见元素A、B、M组成的四种物质发生反应:甲+乙=丙+丁,其中甲由A和M组成,乙由B和M组成,丙只含有M。
(1)若甲为淡黄色固体,乙和丙均为常温下的无色无味气体。则乙的电子式为 ;生成标准状况下5.6L丙转移的电子数为 ;常温下丁溶液pH 7,用离子方程式解释 。
(2)若丁为能使品红褪色的无色气体,丙为常见红色金属,化合物甲、乙中原子个数比均为1:2(M均显+1价),原子序数B大于A。则①A在周期表中位置为 ②丁与水反应的化学方程式为 向反应后溶液中滴加两滴紫色石蕊试液的现象为
③正确书写上述生成丙的化学方程式
④向MCl2的溶液中通入丁,可观察到白色的MCl沉淀,写出该反应的离子方程式 。
常见元素X、Y、Z、W的原子序数依次增大,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的基态原子核外只有三个能级,且各能级电子数相等 |
| Y | Y的基态原子最外层电子数是其内层电子总数的2.5倍 |
| Z | Z的基态价电子结构为nsn-1 |
| W | W单质常在火山口附近被发现,其氧化物是造成酸雨的主要原因之一 |
(1)Y位于元素周期表第 周期 族,其基态原子未成对电子有 个。
(2)X的电负性比W的 (填“大”或“小”);Y的最简单气态氢化物比X的最简单气态氢化物易液化,其主要原因是 。
(3)Z与同周期左右相邻的两种元素的原子相比较,三者第一电离能由大到小的顺序为 (用元素符号表示)。Y和Z形成的化合物为 晶体,该物质遇水强烈水解的化学方程式为 。
(4)在一定温度下,向一个容积不变的密闭容器中充入1molY2和3mol氢气,发生反应:Y2(g)+3H2(g) 2YH3(g) ΔH=-akJ/mol。在该条件下达到平衡时放出的热量为bkJ,其平衡常数表达式K= 。若起始向此容器中充入2molYH3,在相同温度下达到平衡时,反应过程中吸收的热量为ckJ,则a、b、c三者之间的关系为 (用一个式子表示)。 查看习题详情和答案>>