网址:http://m.1010jiajiao.com/timu_id_548875[举报]
1
2
3
4
5
6
7
8
C
D
D
D
C
B
B
D
9
10
11
12
13
14
D
BC
BC
B
AB
CD
15.(10分) (1)① 氟离子 结构示意图 (1分)
② 取形状大小相同的镁片和铝片分别与体积相同、浓度相同的稀盐酸反应,观察产生气泡的快慢 (2分)(操作1分,观察指标1分。着重号部分缺一处扣1分。用金属与沸水反应、等浓度盐溶液碱性比较等合理方法均得分,方案无可行性不给分。)
③ Na2SO3 + SO2 + H2O = 2NaHSO3 (2分)(化学式错得0分,配平错扣1分)
有白色胶状沉淀生成,有无色刺激性气味气体产生 (2分)
(各占1分,着重号部分有缺漏合扣1分)
(2)① H2PO4-、HCO3-、HPO42- (2分) ② 强 (1分)
16.(11分)(1)除去表面的油污 CO32- + H2O  HCO3- + OH- (2分)
HCO3- + OH- (2分)
(2)不再有气泡产生(或只有极少量气泡产生) (1分)
(3)若控制不准确温度过高Fe2+易被氧化;由于有氢气生成,明火加热不安全
(两个方面各占1分)
(4)4Fe2+ + O2 + 4H+ = 4Fe3+ + 2H2O (2分) (化学式错得0分,配平错扣1分)
(5)6.6 (2分) (多写单位g不扣分)
(6)循环使用 (2分(具体说出如何循环使用同样得分,意思相近表达欠清晰扣1分)
17.(11分)
(1)2MnO4- +
5H
(化学式错得0分,配平错扣1分,漏↑扣1分,扣完为止)
(2)4 (2分)
(3)① 反应开始时:c(KMnO4)= =0.00067 mol?L-1 (1分)
=0.00067 mol?L-1 (1分)
反应时间: =
= =6.7min (1分)
=6.7min (1分)
KMnO4的平均反应速率:
ν(KMnO4)= =
= =1×10-4 mol?L-1?min-1 (1分)
=1×10-4 mol?L-1?min-1 (1分)
(一步完成计算且结果正确得3分,结果错误得0分。速率单位错误扣1分)
② 否(或:不可行) (1分) 取过量的体积相同、浓度不同的草酸溶液分别同时与体积相同、浓度相同的高锰酸钾酸性溶液反应。(3分)
(基本思路错误得0分,思路正确未强调草酸过量扣1分,未强调体积相同扣1分)
18


19.(12分)(1)增大 (1分)(2)不移动 (1分)(3)(4分)(各占2分,起点位置、曲线走势、终点与原曲线的相对高低等只要有一处错误则得0分。)
(4)(4分)0.60(2分) ν正_>_ν逆(2分)
(5)-787.0 (2分)(不带负号得0分,有效数字不准确扣1分。)
20.(每空2分,共10分)
(1) (2分) (2)均为氧化还原反应 (2分)
(2分) (2)均为氧化还原反应 (2分)
(3)3Fe+ 4H2O  Fe 3O4+4H2↑
(2分)
Fe 3O4+4H2↑
(2分)
(4)Fe+6H++3NO3-=Fe3++3NO2↑+3 H2O
3 Fe+8H++2NO3-=3Fe2++2NO ↑+4H2O (共2分)
(5)取少量样品于试管中,加入KSCN溶液,如果出现红色,说明变质;反之,没有变质 (2分)
21(1)a、d(1分); (2)3:2:3(1分); (3)C3H4O4(1分);


 (4)
+ CH2(COOH) 2
+H2O(2分)
(4)
+ CH2(COOH) 2
+H2O(2分)
(5)4种 (2分) (写出下列四种结构中的任意一种均可得2分)
 |
22.(10分)(1) C F (2分) (漏选1个扣1分,多选一个也扣1分,扣完为止。)
(2)① 3 (1分) 2 (1分)
② HCO3-中含有O-H键,相互之间可通过O-H┅O氢键缔合(1分)
(写出HCO3-化学式并指出离子之间有氢键作用才能得分)
(3)断裂C≡O中的一个π键消耗的能量是273kJ/mol,断裂N≡N中的一个π键消耗的能量是523.3kJ/mol, 断裂一个π键CO比N2更容易,所以CO更活泼。(2分)
 (叙述清楚,未具体计算出数值不扣分。)
(叙述清楚,未具体计算出数值不扣分。)
(4)① 1s22s22p63s23p63d84s2 (1分)
② 分子晶体 (1分)
③ (1分)
23.(10分) (1)FeC2O4?2H2O FeC2O4+2H2O,加热 减少的质量等于所含结晶水的质量 (2)FeO、CO、CO2;1:1:1。(3)30%。(4)6Fe2O3
FeC2O4+2H2O,加热 减少的质量等于所含结晶水的质量 (2)FeO、CO、CO2;1:1:1。(3)30%。(4)6Fe2O3 4Fe3O4+O2↑
4Fe3O4+O2↑
(共13分)粗食盐中除含有CaCl2、MgCl2、Na2SO4等可溶性杂质外,还含有泥砂等不溶性杂质。我们食用的精盐是用粗食盐提纯而得到的。已知:Mg(OH)2难溶于水,BaCO3难溶于水但可溶于盐酸,BaSO4既难溶于水又难溶于酸。
 某同学设计了一种制备精盐的实验方案,步骤如下(每次用于沉淀的试剂均过量)
某同学设计了一种制备精盐的实验方案,步骤如下(每次用于沉淀的试剂均过量)
⑴粗盐的提纯,使用的主要仪器,合理的组合有
①漏斗、②烧杯、③蒸发皿、④酒精灯、⑤量筒、⑥试管夹、⑦玻璃棒、⑧集气瓶
A.①②③④⑦ B.①②③④⑤
C.①②③⑥⑧ D.②③④⑦⑧
⑵如何运用最简方法检验溶液中有无SO42-离子,所用试剂 溶液。如何检验SO42-离子是否除净简单操作为
⑶除去粗食盐中镁离子所用试剂为 溶液。
化学反应方程式
⑷请用化学反应方程式表示第④步中,加入过量Na2CO3溶液的作用:
⑸实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯,②固定铁圈位置,③放上蒸发皿(蒸发皿中盛有NaCl溶液),④加热搅拌,⑤停止加热
其正确的操作顺序为 。当出现 时就可以停止加热。
查看习题详情和答案>>将A g粗盐样品溶于水,所得溶液中含有Ca2+、Mg2+等杂质离子,现设计实验,采用常见的试剂,精制食盐溶液。回答下列问题:
(1)为了除去粗盐中的CaCl2、MgCl2、Na2SO4及泥沙。可将粗盐溶于水,此时可以观察到的实验现象为 。溶解时玻璃棒的作用为 。
(2)在步骤(1)之后进行下列五项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。正确的操作顺序是________________(填代号)。
A.⑤④②①③ B.④①②⑤③ C.②⑤④①③ D.⑤②④①③
(3)在进行步骤(2)的实验中,检验SO42-沉淀是否完全的方法是
。
(4)检验提纯后的食盐溶液中是否含有SO42-的方法是:取少量溶液置于试管中,向溶液中加入足量的 ,然后加入几滴 溶液,若产生白色沉淀说明有SO42-;若不产生白色沉淀说明无SO42-。
(5)在蒸发NaCl溶液时,一般的有以下步骤:①放置酒精灯;②固定铁圈位置;③放上蒸发皿;④加热搅拌;⑤停止加热。正确的操作顺序是 。
(6)实验完毕得到Bg固体,则原样品中Na+质量为 g。
A.<23 A/58.5 B.> 23A/58.5 C.<23 B/58.5 D.> 23B/58.5
查看习题详情和答案>>将A g粗盐样品溶于水,所得溶液中含有Ca2+、Mg2+等杂质离子,现设计实验,采用常见的试剂,精制食盐溶液。回答下列问题:
(1)为了除去粗盐中的CaCl2、MgCl2、Na2SO4及泥沙。可将粗盐溶于水,此时可以观察到的实验现象为 。溶解时玻璃棒的作用为 。
(2)在步骤(1)之后进行下列五项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。正确的操作顺序是________________(填代号)。
A.⑤④②①③ B.④①②⑤③ C.②⑤④①③ D.⑤②④①③
(3)在进行步骤(2)的实验中,检验SO42-沉淀是否完全的方法是
。
(4)检验提纯后的食盐溶液中是否含有SO42-的方法是:取少量溶液置于试管中,向溶液中加入足量的 ,然后加入几滴 溶液,若产生白色沉淀说明有SO42-;若不产生白色沉淀说明无SO42-。
(5)在蒸发NaCl溶液时,一般的有以下步骤:①放置酒精灯;②固定铁圈位置;③放上蒸发皿;④加热搅拌;⑤停止加热。正确的操作顺序是 。
(6)实验完毕得到Bg固体,则原样品中Na+质量为 g。
A.<23 A/58.5 B.> 23A/58.5 C.<23 B/58.5 D.> 23B/58.5
查看习题详情和答案>>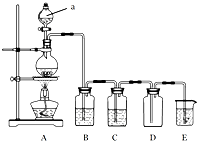 如图是实验室中制备气体或验证气体性质的装置图.
如图是实验室中制备气体或验证气体性质的装置图.(1)仪器a的名称是
(2)利用上图装置制备纯净、干燥的氯气.
①圆底烧瓶内发生反应的离子方程式为
| ||
| ||
②装置B中的溶液为
(3)利用上图装置证明SO2具有漂白性、还原性及生成气体中含有CO2.
圆底烧瓶内加入碳,a中加入浓硫酸,B、D中匀为少量品红溶液,C中为足量酸性高锰酸钾溶液,E中为澄清石灰水.
①证明SO2具有漂白性的装置是
②证明SO2具有还原性的现象是
③证明生成气体中含有CO2的现象是
④D装置的作用是