摘要:(NH2NH3++ H2O NH3NH32++OH- )w.w.w.k.s.5.u.c.o.m(2)N2H4 CO(NH2)2+ NaClO+ 2NaOH = N2H4+NaCl+Na2CO3 +H2O
网址:http://m.1010jiajiao.com/timu_id_500334[举报]
(2009?中山模拟)某研究性学习小组学习了工业“侯氏制碱法”的原理后:
[提出问题]能否在实验室模拟“侯氏制碱法”中制取NaHCO3的过程呢?
[实验原理]写出候氏制碱法反应的化学方程式为
请回答下列问题:
(1)检验A装置气密性的方法是:塞紧带长颈漏斗的橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水后,若
(2)D是连接在装置A与装置C之间的气体净化装置,进气口是
(3)实验时先向饱和NaCl溶液中通入较多的
①使CO2更易被吸收 ②NH3比CO2更易制取 ③CO2的密度比NH3大
(4)用
如果要制得纯碱,还需发生的反应是(写出反应的化学方程式):
[得出结论]利用“侯氏制碱法”在实验室可以制取NaHCO3.
查看习题详情和答案>>
[提出问题]能否在实验室模拟“侯氏制碱法”中制取NaHCO3的过程呢?
[实验原理]写出候氏制碱法反应的化学方程式为
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
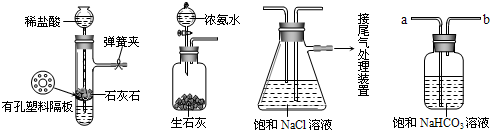
.[实验验证]如图是该学习小组进行模拟实验时所用到的部分主要装置.
请回答下列问题:
(1)检验A装置气密性的方法是:塞紧带长颈漏斗的橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水后,若
漏斗中与试管中的液(水)面差保持不再变化或漏斗中的液(水)面不再下降;
漏斗中与试管中的液(水)面差保持不再变化或漏斗中的液(水)面不再下降;
,说明装置不漏气.(2)D是连接在装置A与装置C之间的气体净化装置,进气口是
a
a
(填a或b),D的作用是除去HCl
HCl
气体.可否将瓶内试剂换为碳酸钠溶液否
否
(填“可”“否”).(3)实验时先向饱和NaCl溶液中通入较多的
NH3
NH3
,再通入足量的CO2
CO2
,其原因是①
①
.(填写序号)①使CO2更易被吸收 ②NH3比CO2更易制取 ③CO2的密度比NH3大
(4)用
过滤
过滤
的方法将生成的NaHCO3晶体从混合物中分离出来.如果要制得纯碱,还需发生的反应是(写出反应的化学方程式):
2NaHCO3
Na2CO3+H2O+CO2↑
| ||
2NaHCO3
Na2CO3+H2O+CO2↑
.
| ||
[得出结论]利用“侯氏制碱法”在实验室可以制取NaHCO3.
(2009?湛江二模)已探明我国锰矿储量占世界第三位,但富矿仅占6.4%,每年尚需进口大量锰矿石.有人设计了把我国的贫菱锰矿(MnCO3含量较低)转化为高品位“菱锰矿砂”(MnCO3含量高)的绿色工艺.该工艺流程如图所示:
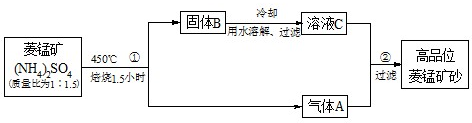
已知焙烧反应①的化学方程式:(NH4)2SO4+MnCO3
MnSO4+2NH3↑+CO2↑+H2O.
(1)写出反应②的离子方程式
(2)上述工艺流程中,可以循环利用的物质有(NH4)2SO4、
(3)向物质的量浓度均为0.01mol?L-1的MnCl2和BaCl2混合溶液中,滴加Na2CO3溶液,先沉淀的是
=
查看习题详情和答案>>

已知焙烧反应①的化学方程式:(NH4)2SO4+MnCO3
| ||
(1)写出反应②的离子方程式
Mn2++2NH3+CO2+H2O=2NH4++MnCO3↓
Mn2++2NH3+CO2+H2O=2NH4++MnCO3↓
.(2)上述工艺流程中,可以循环利用的物质有(NH4)2SO4、
NH3
NH3
、CO2
CO2
.从物料平衡角度看,理论上生产过程中不需要
不需要
(填“需要”或者“不需要”)添加(NH4)2SO4.(3)向物质的量浓度均为0.01mol?L-1的MnCl2和BaCl2混合溶液中,滴加Na2CO3溶液,先沉淀的是
Mn2+
Mn2+
(填离子符号);当两种沉淀共存时,溶液中| c(Ba2+) |
| c(Mn2+) |
450
450
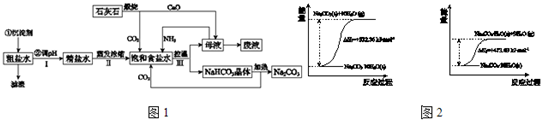
[Ksp(BaCO3)=8.1×10-9,Ksp(MnCO3)=1.8×10-11].(2012?西城区一模)工业上以粗食盐(含有少量Ca2+、Mg2+杂质)、氨、石灰石等为原料,可以制备Na2CO3.其过程如图1所示.
请回答:
(1)在处理粗盐水的过程中,可加入石灰乳和纯碱作为沉淀剂,则所得滤渣的成分除过量的沉淀剂外还有
(2)将CaO投入含有大量的NH4Cl的母液中,能生成可循环使用的NH3,该反应的化学方程式是
(3)向饱和食盐水中首先通入的气体是
(4)碳酸钠晶体失水的能量变化示意图如图2:
Na2CO3?H2O (s) 脱水反应的热化学方程式是
(5)产品纯碱中常含有NaCl.取a g混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b g固体.则该产品中Na2CO3的质量分数是
.
(6)熔融Na2CO3可作甲烷--空气燃料电池的电解质,该电池负极的反应式是
查看习题详情和答案>>

请回答:
(1)在处理粗盐水的过程中,可加入石灰乳和纯碱作为沉淀剂,则所得滤渣的成分除过量的沉淀剂外还有
CaCO3、Mg(OH)2
CaCO3、Mg(OH)2
.(2)将CaO投入含有大量的NH4Cl的母液中,能生成可循环使用的NH3,该反应的化学方程式是
2NH4Cl+CaO=CaCl2+2NH3↑+H2O
2NH4Cl+CaO=CaCl2+2NH3↑+H2O
.(3)向饱和食盐水中首先通入的气体是
NH3
NH3
,过程Ⅲ中生成NaHCO3晶体的反应的化学方程式是NH3+H2O+CO2+NaCl=NaHCO3↓+NH4Cl
NH3+H2O+CO2+NaCl=NaHCO3↓+NH4Cl
.(4)碳酸钠晶体失水的能量变化示意图如图2:
Na2CO3?H2O (s) 脱水反应的热化学方程式是
Na2CO3?H2O(s)=Na2CO3(s)+H2O(g)△H=+58.73kJ?mol-1
Na2CO3?H2O(s)=Na2CO3(s)+H2O(g)△H=+58.73kJ?mol-1
.(5)产品纯碱中常含有NaCl.取a g混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b g固体.则该产品中Na2CO3的质量分数是
| 106(b-a) |
| 11a |
| 106(b-a) |
| 11a |
(6)熔融Na2CO3可作甲烷--空气燃料电池的电解质,该电池负极的反应式是
CH4-8e-+4CO32-=5CO2+2H2O
CH4-8e-+4CO32-=5CO2+2H2O
.致冷剂是一种易被压缩、液化的气体,液化后在管内循环,蒸发时吸收热量,使环境温度降低,达到致冷目的.人们曾采用过乙醚、NH3、CH3Cl等作致冷剂,但它们不是有毒,就是易燃、于是科学家根据元素性质的递变规律来开发新的致冷剂
据现有知识,某些元素化合物的易燃性、毒性变化趋势如下:
(1)氢化物的易燃性:第二周期
(2)化合物的毒性:PH3>NH3; H2S
(3)已知CCl4的沸点为76.8℃,CF4的沸点为-128℃,新致冷剂的沸点范围应介于其间.经过较长时间反复试验,一种新的致冷剂氟里昂CF2Cl2终于诞生了,其它类似于CF2Cl2的物质还可能有
(4)根据周期表中元素及其化合物的
查看习题详情和答案>>
据现有知识,某些元素化合物的易燃性、毒性变化趋势如下:
(1)氢化物的易燃性:第二周期
CH4
CH4
>NH3
NH3
>H2O>HF;(2)化合物的毒性:PH3>NH3; H2S
>
>
H2O;CCl4>
>
CF4 (选填>或<).(3)已知CCl4的沸点为76.8℃,CF4的沸点为-128℃,新致冷剂的沸点范围应介于其间.经过较长时间反复试验,一种新的致冷剂氟里昂CF2Cl2终于诞生了,其它类似于CF2Cl2的物质还可能有
CFCl3(或CClF3)
CFCl3(或CClF3)
.(填一种);这类致冷剂的大量使用造成了当今的某一环境问题是臭氧层空洞
臭氧层空洞
(选填:温室效应、酸雨、臭氧层空洞、光化学烟雾).(4)根据周期表中元素及其化合物的
a
a
变化趋势来开发致冷剂的科学思维方法是值得借鉴的.(填写字母,多选扣分)①毒性 ②沸点 ③易燃性 ④水溶性 ⑤颜色 (a)①②③(b)②④⑤(c)②③④(2011?姜堰市二模)在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙.下图所示A-E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题.

(1)实验室制取、收集干燥的NH3,需选用上述仪器装置中的
(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是
(3)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级
查看习题详情和答案>>

(1)实验室制取、收集干燥的NH3,需选用上述仪器装置中的
ACDE
ACDE
.(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是
NH3
NH3
,写出制纳米级碳酸钙的化学方程式:CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl
CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl
.(3)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级
取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是
取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是
.