摘要:C.此反应在1000℃达平衡时.c(CO2)?c(H2)/[c(CO)?c(H2O)] 约为0.59
网址:http://m.1010jiajiao.com/timu_id_445410[举报]
 哈伯因发明了氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖,N2(g)+3H2(g)
哈伯因发明了氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖,N2(g)+3H2(g)| 催化 |
(1)此反应在50~60s时化学平衡常数为K1=
| 0.52 |
| 2.253×0.75 |
| 0.52 |
| 2.253×0.75 |
(2)反应进行到60s时,改变的条件可能是
C
C
.A.加入催化剂 B.扩大容器的体积
C.升高温度 D.减小氨气的浓度
在该条件下,氮气的化学反应速率
变大
变大
(填“变小”、“变大”或“不变”)(3)该反应在80S后化学平衡常数为K2,则K1
>
>
K2(填“>”,“<”或“=”),此时氮气的转化率为20%
20%
.(4)若在110s后向该平衡体系中再加入1mol氨气,则再次达平衡后,氨气在平衡体系中的体积分数
变大
变大
.(填“变小”、“变大”或“不变”)25℃时,在体积为2L的密闭容器中,气态物质A、B、C的物质的量n(mol)随时间t的变化如下图1所示.已知达平衡后,降低温度,A的转化率将增大.

(1)从反应开始到达第一次平衡时的平均速率v(A)为
(2)根据上图数据,写出该反应的化学方程式
(3)在5~7min内,若K值不变,则此处曲线变化的原因是
(4)下图2表示此反应的反应速率v和时间t的关系图,根据上图判断,在t3和t5时刻改变的外界条件分别是
查看习题详情和答案>>

(1)从反应开始到达第一次平衡时的平均速率v(A)为
0.05mol/(L?min)
0.05mol/(L?min)
.(2)根据上图数据,写出该反应的化学方程式
A+2B?2C
A+2B?2C
;求出此反应在25℃的平衡常数K=6.43L/mol
6.43L/mol
(保留2位小数).(3)在5~7min内,若K值不变,则此处曲线变化的原因是
增大压强
增大压强
.(4)下图2表示此反应的反应速率v和时间t的关系图,根据上图判断,在t3和t5时刻改变的外界条件分别是
升高温度
升高温度
和加入催化剂
加入催化剂
;A的转化率最大的一段时间是t2~t3
t2~t3
.哈伯因发明了氮气和氢气合成氨气的方法而获得1918年的诺贝尔化学奖,
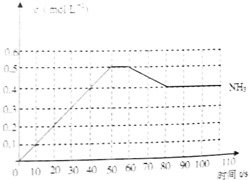
N2(g)+3H2(g)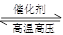 2NH3(g) △H<0。下图表示某温度时,向1L容器中加入1mol氮气,3mol氢气,该反应在110S内反应进行的程度:
2NH3(g) △H<0。下图表示某温度时,向1L容器中加入1mol氮气,3mol氢气,该反应在110S内反应进行的程度:

(1)此反应在50~60s时化学平衡常数为K1 = (列出计算式不用试算)。
(2)反应进行到60s时,改变的条件可能是 。
A.加入催化剂 B.扩大容器的体积
C.升高温度 D.减小氨气的浓度
在该条件下,氮气的化学反应速率 。(填“变小”、“变大”或“不变”)
(3)该反应在80s后化学平衡常数为K2,则K1 K2(填“>”、“<”或“=”),此时氮气的转化率为 。
(4)若在110s后向该平衡体系中再加入1mol氨气,则再次达平衡后,氨气在平衡体系中的体积分数 。(填“变小”、“变大”或“不变”)
查看习题详情和答案>>
哈伯因发明了氮气和氢气合成氨气的方法而获得1918年的诺贝尔化学奖,
N2(g)+3H2(g)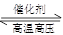 2NH3(g) △H<0。下图表示某温度时,向1L容器中加入1mol氮气,3mol氢气,该反应在110S内反应进行的程度:
2NH3(g) △H<0。下图表示某温度时,向1L容器中加入1mol氮气,3mol氢气,该反应在110S内反应进行的程度: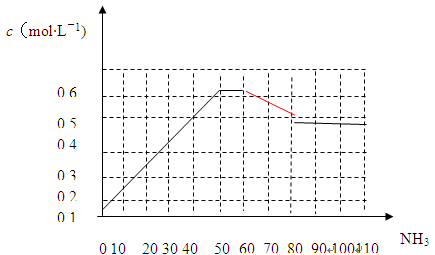
(1)此反应在50~60s时化学平衡常数为K1 = (列出计算式不用试算)。
(2)反应进行到60s时,改变的条件可能是 。
| A.加入催化剂 | B.扩大容器的体积 |
| C.升高温度 | D.减小氨气的浓度 |
(3)该反应在80s后化学平衡常数为K2,则K1 K2(填“>”、“<”或“=”),此时氮气的转化率为 。
(4)若在110s后向该平衡体系中再加入1mol氨气,则再次达平衡后,氨气在平衡体系中的体积分数 。(填“变小”、“变大”或“不变”) 查看习题详情和答案>>