摘要:被氧化剂氧化为酸(如Ag(NH3)+.Cu(OH)2.O2等)羧酸
网址:http://m.1010jiajiao.com/timu_id_441994[举报]
(2009?淮安二模)甲氧普胺(Metoclopramide)是一种消化系统促动力药.它的工业合成路线如下[已知氨基(-NH2)易被氧化剂氧化]:

请回答下列问题:
(1)已知A物质既能与酸反应又能与碱反应,长期暴露在空气中会变质. A物质中所含有的官能团除羧基外还有
(2)在B物质的同分异构体中,含有-NO2和手性碳原子且无甲基的取代苯结构的有
(3)反应②在合成过程中的作用是
(4)反应③的另一种有机产物与新制Cu(OH)2悬浊液反应的化学方程式为
(5)A物质的一种同分异构体H可以发生分子间缩合反应,形成一个含八元环的物质I,则I的结构简式为
 ;高聚物J由I通过肽键连接而成,则形成J的反应方程式为:
;高聚物J由I通过肽键连接而成,则形成J的反应方程式为:
查看习题详情和答案>>

请回答下列问题:
(1)已知A物质既能与酸反应又能与碱反应,长期暴露在空气中会变质. A物质中所含有的官能团除羧基外还有
氨基
氨基
、酚羟基
酚羟基
.(2)在B物质的同分异构体中,含有-NO2和手性碳原子且无甲基的取代苯结构的有
3
3
种.(3)反应②在合成过程中的作用是
保护氨基,防止在合成过程中被氧化剂(如Cl2)氧化
保护氨基,防止在合成过程中被氧化剂(如Cl2)氧化
.(4)反应③的另一种有机产物与新制Cu(OH)2悬浊液反应的化学方程式为
CH3CHO+2Cu(OH)2
CH3COOH+Cu2O↓+2H2O
| △ |
CH3CHO+2Cu(OH)2
CH3COOH+Cu2O↓+2H2O
.| △ |
(5)A物质的一种同分异构体H可以发生分子间缩合反应,形成一个含八元环的物质I,则I的结构简式为


n
 +(n-1)H2O
+(n-1)H2O

| 催化剂 |
 +(n-1)H2O
+(n-1)H2On
 +(n-1)H2O
+(n-1)H2O
.
| 催化剂 |
 +(n-1)H2O
+(n-1)H2O
硫代硫酸钠(Na2S2O3)可看成是一个S原子取代了Na2SO4中的一个O原子而形成.研究小组运用类比学习的思想,通过实验探究Na2S2O3的化学性质.
(1)他们提出如下猜想:猜想①:与BaCl2溶液反应有沉淀生成;猜想②:溶液呈中性,且不与酸反应;猜想③:无还原性,不能被氧化剂氧化.
他们提出上述猜想的依据是 .
(2)对上述猜想②、③,他们设计实验方案,并进行实验.请在答题卡上按下表格式完成相关的实验操作步骤、预期现象.请限选实验仪器与试剂:试管、玻璃棒、滴管、pH试纸:3mol?L-1H2SO4、新制氯水、1mol?L-1 BaCl2 溶液、Na2S2O3溶液、蒸馏水.
(3)小组同学为确证经操作三后Na2S2O3被氧化,提出如下实验方案 .
查看习题详情和答案>>
(1)他们提出如下猜想:猜想①:与BaCl2溶液反应有沉淀生成;猜想②:溶液呈中性,且不与酸反应;猜想③:无还原性,不能被氧化剂氧化.
他们提出上述猜想的依据是
(2)对上述猜想②、③,他们设计实验方案,并进行实验.请在答题卡上按下表格式完成相关的实验操作步骤、预期现象.请限选实验仪器与试剂:试管、玻璃棒、滴管、pH试纸:3mol?L-1H2SO4、新制氯水、1mol?L-1 BaCl2 溶液、Na2S2O3溶液、蒸馏水.
| 实验操作 | 实验现象或 预期实验现象 |
现象解释 (用离子方程式表示) |
结论 | |
| 猜想② | 操作一: |
溶液pH=8 | / | Na2S2O3溶液呈中性,能与酸反应,具有还原性,与Na2SO4的化学性质不相似. |
| 操作二: |
S2O32-+2H+=S↓+SO2↑+H2O | |||
| 猜想③ | 操作三: |
下表是周期表中的一部分,请回答下列问题:

(1)A是④的最高价含氧酸,其化学式为
(2)将③对应的单质投入A的稀溶液中,发生的反应属于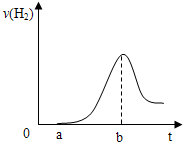
(3)把在空气中久置的③的单质投入A的稀溶液中,产生氢气的速率与反应时间的关系可用如图曲线表示:
曲线0→a段不产生氢气的原因是
曲线由b以后产生氢气速率逐渐减小的主要原因是
(4)①和②对应的单质在一个固定体积的密闭容器中发生可逆反应,该反应达到平衡的标志是
查看习题详情和答案>>

(1)A是④的最高价含氧酸,其化学式为
H2SO4
H2SO4
,A中所含的化学键类型为共价键
共价键
.(2)将③对应的单质投入A的稀溶液中,发生的反应属于
放热
放热
反应(填“吸热”或“放热”),该反应中反应物的总能量大于
大于
生成物的总能量(填“大于”或“小于”);若将③对应的单质和铁用导线连接后投入A的稀溶液中,组成的装置中能量转化形式主要是化学能转化为电能
化学能转化为电能
,该装置正极材料是Fe
Fe
.
(3)把在空气中久置的③的单质投入A的稀溶液中,产生氢气的速率与反应时间的关系可用如图曲线表示:
曲线0→a段不产生氢气的原因是
铝表面被O2氧化为致密的氧化膜,限制了铝与H2SO4的反应
铝表面被O2氧化为致密的氧化膜,限制了铝与H2SO4的反应
,曲线a→b段产生氢气速率逐渐增大的主要原因是反应放热,温度升高是影响反应速率的主要因素,使反应速率增大
反应放热,温度升高是影响反应速率的主要因素,使反应速率增大
,曲线由b以后产生氢气速率逐渐减小的主要原因是
随反应c(H+)减小,该因素变为影响化学反应速率的主要因素,化学反应速率开始下降
随反应c(H+)减小,该因素变为影响化学反应速率的主要因素,化学反应速率开始下降
.(4)①和②对应的单质在一个固定体积的密闭容器中发生可逆反应,该反应达到平衡的标志是
各成分的浓度(或质量、物质的量、压强等)不再变化
各成分的浓度(或质量、物质的量、压强等)不再变化
(请列举一项).(2010?惠州模拟)Na2S2O3可看成是Na2SO4中的一个0原子被一个S原子取代而成.某同学用类比的思想进行实验探究,同时比较Na2S2O3与Na2SO4的化学性质是否相似.
【提出猜想】
猜想①:溶液呈中性,且不与酸反应;
猜想②:无还原性,不能被氧化剂氧化.
【实验探究】基于上述猜想,设计方案并进行实验探究:

【实验结论】Na2S2O3溶液呈碱性能与酸反应,有还原性,与Na2SO4的化学性质不相似.
【问题讨论】
(1)甲同学向“猜想②并所得的部分溶液中滴加AgNO3溶液,产生白色沉淀,由此他认为氯水可将Na2S2O3氧化.该结论是否正确?
(2)乙同学向“猜想②”所得的另一部分溶液中滴加
查看习题详情和答案>>
【提出猜想】
猜想①:溶液呈中性,且不与酸反应;
猜想②:无还原性,不能被氧化剂氧化.
【实验探究】基于上述猜想,设计方案并进行实验探究:

【实验结论】Na2S2O3溶液呈碱性能与酸反应,有还原性,与Na2SO4的化学性质不相似.
【问题讨论】
(1)甲同学向“猜想②并所得的部分溶液中滴加AgNO3溶液,产生白色沉淀,由此他认为氯水可将Na2S2O3氧化.该结论是否正确?
不正确
不正确
,理由为因氯水过量,氯水中含有Cl-
因氯水过量,氯水中含有Cl-
.(2)乙同学向“猜想②”所得的另一部分溶液中滴加
用盐酸盐化的氯化钡溶液
用盐酸盐化的氯化钡溶液
,观察到有有白色沉淀产生
有白色沉淀产生
的现象时,可以证明S2O43-被氯水氧化成SO42-.KClO3和KIO3在日常生活、工农业生产和科研方面有着广泛的应用.
(1)实验室可用KClO3分解制取O2,KClO3受热分解的反应分两步进行:①4KClO3(s)=3KClO4(s)+KCl(s);②KClO4(s)=KCl(s)+2O2(g).已知:
K(s)+
Cl2(g)=KCl(s)△H=-437kJ?mol-1
K(s)+
Cl2(g)+
O2(g)=KClO3(s)△H=-398kJ?mol-1
K(s)+
Cl2(g)+2O2(g)=KClO4(s)△H=-433kJ?mol-1
则反应4KClO3(s)=3KClO4(s)+KCl(s)的△H=
(2)Ca(IO3)2是食品及饲料添加剂补充碘源的优良品种.工业上生产Ca(IO3)2的方法通常有两类:
方法一:氧化剂氧化法.如:用KClO3在盐酸存在条件下,将碘单质氧化为HIO3(KClO3被还原为Cl2),然后加Ca(OH)2中和制得Ca(IO3)2.
方法二:电化学氧化法.用适宜浓度的KOH溶液溶解工业精碘作为阳极液(3I2+6KOH=5KI+KIO3+3H2O),用稀KOH溶液为阴极液,电解氧化制 备KIO3,与CaCl2反应得到Ca(IO3)2.
①用KClO3氧化碘单质是一剧烈的放热反应,所以要控制加料速度,与电解氧化法相比缺点主要有
②电化学氧化法电解时的阳极反应式是
③某工厂用电化学氧化法制取Ca(IO3)2,每1kg碘单质理论上可生产纯度为97.8%Ca(IO3)2的质量为
查看习题详情和答案>>
(1)实验室可用KClO3分解制取O2,KClO3受热分解的反应分两步进行:①4KClO3(s)=3KClO4(s)+KCl(s);②KClO4(s)=KCl(s)+2O2(g).已知:
K(s)+
| 1 |
| 2 |
K(s)+
| 1 |
| 2 |
| 3 |
| 2 |
K(s)+
| 1 |
| 2 |
则反应4KClO3(s)=3KClO4(s)+KCl(s)的△H=
-144kJ/mol
-144kJ/mol
kJ/mol.(2)Ca(IO3)2是食品及饲料添加剂补充碘源的优良品种.工业上生产Ca(IO3)2的方法通常有两类:
方法一:氧化剂氧化法.如:用KClO3在盐酸存在条件下,将碘单质氧化为HIO3(KClO3被还原为Cl2),然后加Ca(OH)2中和制得Ca(IO3)2.
方法二:电化学氧化法.用适宜浓度的KOH溶液溶解工业精碘作为阳极液(3I2+6KOH=5KI+KIO3+3H2O),用稀KOH溶液为阴极液,电解氧化制 备KIO3,与CaCl2反应得到Ca(IO3)2.
①用KClO3氧化碘单质是一剧烈的放热反应,所以要控制加料速度,与电解氧化法相比缺点主要有
反应剧烈,需要控制速率;反应过程中产生氯气,对生产操作环境有较大污染
反应剧烈,需要控制速率;反应过程中产生氯气,对生产操作环境有较大污染
.②电化学氧化法电解时的阳极反应式是
I-+6OH--6e-=IO3-+3H2O
I-+6OH--6e-=IO3-+3H2O
.③某工厂用电化学氧化法制取Ca(IO3)2,每1kg碘单质理论上可生产纯度为97.8%Ca(IO3)2的质量为
1.57kg
1.57kg
kg(计算结果保留叁位有效数字).