网址:http://m.1010jiajiao.com/timu_id_441444[举报]
某化学兴趣小组的同学为进行物质性质的探究,用维持烧瓶内压强与分液漏斗内压强相等,使液体能顺利滴下
下图所示装置进行实验。请回答下列问题:(加热及固定装置已略去)

(1)装置A中反应的化学方程式为
(2)装置C 中的试剂是 ( 填序号).
A.氢氧化钠溶液 B. 酸性高锰酸钾溶液 C.亚硫酸氢钠溶液
发生反应的离子方程式为 ,其说明了SO2具有 ,该实验操作的名称是 。
(3)在上述实验中,能说明碳的非金属性比硅强的实验现象是
(4)B中的溶液无明显现象,当滴加氯水时有白色沉淀,写出SO2表现还原性并生成白色沉淀的总离子方程式为
查看习题详情和答案>>
H:0.1 |
|
|
|
|
|
|
Li:1.0 | Be:1.5 | B:2.0 | C:2.5 | N:3.0 | O:3.5 | F:4.0 |
Na:0.9 | Mg:1.2 | Al:1.5 | Si:1.8 | P:2.1 | S:2.5 | Cl:3.0 |
K:0.8 | Ca:1.0 | Ga:1.6 | Ge:1.8 | As:2.0 | Se:2.4 | Br:2.8 |
Rb:0.8 | Sr:1.0 | In:1.7 | Sn:1.8 | Sb:1.9 | Te:χ | I:2.5 |
Cs:0.7 | Ba:0.9 | Tl:1.8 | Pb:1.9 | Bi:1.9 | Po:2.0 | At:2.5 |
Fr:0.7 | Ra:0.9 |
|
|
|
|
|
回答下列问题:
(1)写出上述元素电负性在同周期或同主族中的递变规律(任定一种):___________________。
(2)预测Te元素χ的值为_________,它的非金属性比I元素_________ (选填“强”或“弱”)。
(3)你认为Linus Pauling提出电负性的概念是确定化合物中原子_________(选填“失电子”或“得电子”)能力的相对大小。
(4)大量事实表明,当两种元素的Χ值相差大于或等于1.7时,形成的化合物一般是离子化
合物,根据此经验规律,AlCl3中化学键的类型应该是_________。
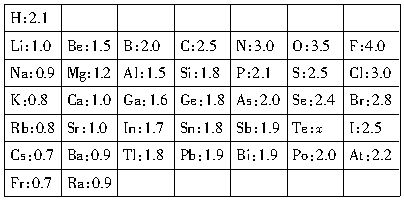
试回答下列问题:
(1)写出上述元素电负性在同周期、同主族中的递变规律:_____________________
___________________________________________________________。
(2)预测Te元素的x值范围:
________,它的非金属性比I元素的________(填“强”或“弱”)。
(3)你认为Linus Pauling提出电负性的概念是确定化合物中原子______(填“失电子”或“得电子”)能力的相对强弱。
(4)大量事实表明,当两种元素的x值相差大于
1.7时,组成的化合物一般是离子化合物,根据此经验规律,AlCl3中的化学键类型应该是________。 查看习题详情和答案>>

(1)仪器A中应盛放的药品是
(2)B中发生反应的离子方程式为:
(3)该实验能证明硫与碳的非金属性的强弱的理论依据是:
 如图是元素周期表的一部分,X、Y、Z、W均为短周期元素,X、Z的质子数之和为21.下列说法正确的是( )
如图是元素周期表的一部分,X、Y、Z、W均为短周期元素,X、Z的质子数之和为21.下列说法正确的是( )