网址:http://m.1010jiajiao.com/timu_id_439294[举报]
说明:
1. 本答案供阅卷评分使用,试题的参考解答是用来说明评分标准的,考生如按其他方法或步骤解答,正确的同样给分;有错的,根据错误的性质,参照评分标准中相应的规定评分。
2. 化学专用名词中出现错别字、元素符号有错误,都要参照评分标准扣分。
3. 化学方程式、离子方程式未配平的,都不给分。
4. 计算只有最后答案而无演算过程的,不给分。
第Ⅰ卷(选择题,共50分)
一、选择题(本题包括25小题,每小题2分,共50分。每小题只有一个选项符合题意)
1. D 2. B 3. C 4. D 5. B 6. D 7. C 8. A 9. A 10. C 11. C 12. B 13. B 14. A
15. D 16. D 17. B 18. A 19. A 20. C 21. C 22. A 23. B 24. C 25. D
第Ⅱ卷(非选择题,共50分)
二、填空题(本题包括6小题,每空1分,共25分)
26.(4分) > > 10-7 mol?L-1 10-14
27.(6分)2 失去2 3 FeS Fe+Cu2+===Fe2++Cu 2Fe+3Cl2点燃=====2FeCl3
28.(4分)→ ← ← ―
 29.(2分)正 氧化
29.(2分)正 氧化
 30.(5分)(1)Al 3 ⅢA (2)钠
30.(5分)(1)Al 3 ⅢA (2)钠
31.(4分)
三、简答题(本题包括3小题,共15分)
32.(共7分,每空1分)(1)2Al+Fe2O3高温=====2Fe+Al2O3 铝(或Al)
(2)大量气泡 2H2O2MnO2======2H2O+O2↑
(3)红 变深 增大任何一种反应物的浓度,都促使化学平衡向正反应方向移动
33.(共4分,每空1分)酸 Fe3++3H2O Fe(OH)3+3H+
盐酸(或HCl)
Fe(OH)3+3H+
盐酸(或HCl)
抑制Ag+ 的水解,防止溶液变浑浊
34.(共4分)(1)气体颜色加深(1分) 气体颜色变浅(1分) (2)升高温度,化学平衡向吸热反应方向移动;降低温度,平衡向放热反应方向移动(2分)
四、计算题(本题包括2小题,共10分)
 35. 解:HNO3+KOH===KNO3+H2O ……………………………………………(1分)
35. 解:HNO3+KOH===KNO3+H2O ……………………………………………(1分)
c(HNO3)?V[HNO3(aq)]=c(KOH)?V[KOH(aq)] ……………………………(1分)
c(HNO3)===0.5018 mol/L (2分)
答:这种HNO3溶液的物质的量浓度为0.5018 mol/L。
36. 解:合金粉末与过量的NaOH溶液混合,只有Al与NaOH反应。
2Al+2NaOH+2H2O===2NaAlO2+3H2↑ 
2×27 g
3×22.4 L
m(Al)
3.36 L …………………………………(2分)
m(Al)= =2.7 g ……………………………………………(2分)
=2.7 g ……………………………………………(2分)
合金中镁的质量分数w(Mg)=×100 %=32.5 % ………………(2分)
答:合金中镁的质量分数为32.5 % 。

(1)反应前混合气体的平均相对分子质量为
(2)达到平衡时混合气体中的氨的物质的量等于
(3)平衡时N2的转化率等于
将N2和H2按一定比例混合,在相同状况下其密度是H2的3.6倍,取0.5 mol该混合气体通入密闭容器内,使之发生反应并在一定条件下达到平衡.已知反应达到平衡后容器内压强是相同条件下反应前压强的0.76倍,试求:
(1)反应前混合气体的平均相对分子质量为________,其中N2和H2的体积比等于________;
(2)达到平衡时混合气体中的氨的物质的量等于________;
(3)平衡时N2的转化率等于________.
(1)B在周期表中位于第
(2)A、C两元素按原子数目比3:1和2:1构成分子M和N,N的电子式为
(3)由C、E组成的化合物乙是汽车安全气囊中的一种成分.现取13.0g乙,加热使其完全分解,生成一种气体单质(标准状况下的体积为6.72L)和一种固体单质,则乙的化学式是
(4)近年来太原市汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物.汽车内燃机工作时引起反应:C2(g)+D2(g)?2CD(g),是导致汽车尾气中含有CD的原因之一.T℃时,向容积为2L的密闭容器中充入10molC2与5molD2,达到平衡后CD的物质的量为2mol,则T℃时该反应的平衡常数K=
(5)当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染.
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ?mol-1
CH4(g)+4NO(g)=CO2(g)+2H2O(g)+2N2(g)△H2
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H3=-867kJ?mol-1
△H2=
某化工厂以甲烷为主要原料来制取合成甲醇及合成氨的原料,其主要反应为:
CH4(g)+H2(g)![]() CO(g)+3H2(g)……①(反应中CH4转化率为1)
CO(g)+3H2(g)……①(反应中CH4转化率为1)
2CO4(g)+O2(g)![]() 2CO(g)+4H2(g)……②(反应中CH4转化率为1)
2CO(g)+4H2(g)……②(反应中CH4转化率为1)
CO(g)+2H2(g)![]() CH3OH(g)……(反应中CO转化率为2/3)
CH3OH(g)……(反应中CO转化率为2/3)
合成工艺如下:

请回答下列问题(所有气体体积均折算为标准状况):
1.若只用反应器①来直接合成甲醇.当充入反应器①的甲烷和水蒸汽的体积分别为672 m3和2240 m3时,反应剩余物中CO为________mol、H2为________mol;
2.若CH4同时和H2O(g)及O2(g)反应,则am3CH4按上述两式完全反应,产物气体的体积V的范围为________.
3.若充入反应器①的甲烷和水蒸汽的体积分别为l体积和3体积,反应剩余物中:V(H2)∶V(N2)∶V(CO)=3∶1∶1.则充入反应器②的富氧空气(只含N2和H2)的体积为________;富氧空气中氧气体积分数为________.
4.若将25%的富氧空气、CH4和H2O(g)混合并充分反应,反应的产物中n(H2)/n(N2)=3∶1,来合成氨气,则反应中的H2O(g)和富氧空气的物质的量之比为________.
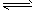 NH3(g) △H=xkJ/mol。请回答:
NH3(g) △H=xkJ/mol。请回答:(1)为提高上述反应的速率,工业上常采用催化剂。目前,最好的催化剂组成为n(Fe2+):n(Fe3+)=0.5,若以FeO、Fe2O3和Fe3O4为原料,则三者的物质的量之比为___________________。
(2)将N2及H2按物质的量之比1:3充入密闭容器中,相等时间内,不同温度下,在催化剂表面反应,N2的转化率与反应温度的关系如图1所示,下列说法正确的是______________。

B.v(N2)=2v(NH3)时,说明已达平衡
C.该催化剂约在500℃时活性较大
D.若增大压强,N2的转化率一定提高
(3)已知:保持温度、容积不变时,各气体的压强(分压)与它们的物质的量成正比。若用Kp表示平衡常数,p(N2)、p(H2)、p(NH3)分别表示N2、H2、NH3的分压。 写出上述反应的平衡常数表达式:
Kp=____。
(4)合成氨工业中,平衡耐NH3的含量[用φ(NH3)表示]与反应的总压、温度、氢氮比[用γ= n(H2)/n(N2)表示]和惰性气体含量(用xi表示)存在一定关系。下列两图是探究γ、xi对合成氨生产影响时所得到的。