摘要:9.下列分子中.所有原子都处在同一平面的是( ) A.环已烯 B.丙炔 C.乙烷 D.苯 答案:D 考点:本题考查了原子共面的判断. 解析:苯属于平面结构.所有原子都处在同一平面.
网址:http://m.1010jiajiao.com/timu_id_4390592[举报]
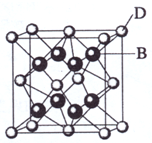 (2009?海南)已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图.
(2009?海南)已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图.请回答:
(1)A元素的名称是
氢
氢
;(2)B的元素符号是
F
F
,C的元素符号是Cl
Cl
,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是氟化氢分子间存在氢键,氯化氢分子间没有氢键
氟化氢分子间存在氢键,氯化氢分子间没有氢键
(3)E属元素周期表中第
四
四
周期,第VIIB
VIIB
族的元素,其元素名称是锰
锰
,它的+2价离子的电子排布式为1s22s22p63s23p63d5
1s22s22p63s23p63d5
:(4)从图中可以看出,D跟B形成的离子化合物的化学式为
CaF2
CaF2
;该离子化合物晶体的密度为a g?cm-3,则晶胞的体积是| 4×78g/mol |
| ag?cm-3×6.02×1023/mol |
| 4×78g/mol |
| ag?cm-3×6.02×1023/mol |
A、B、C、D、E是除稀有气体以外的5种短周期元素,原子序数依次增大并分占三个周期.B、C、D为同一周期依次相邻的3种元素,B和D的原子序数之比为3:4,E原子的电子层数等于最外层电子数.请回答相关问题:
(1)B元素在周期表中的位置
(2)比较D和E简单离子半径的大小(用离子符号表示):
(3)A和D形成的含18电子化合物的化学式为
(4)元素E形成的简单离子的水溶液与C的氢化物的水溶液反应的离子方程式为:
(5)2007年7月2日,美、德两国科学家成功合成了具有独特化学特性的E2A6化合物,该物质在D2中能燃烧,写出它在D2中完全燃烧的化学方程式:
查看习题详情和答案>>
(1)B元素在周期表中的位置
第二周期第IVA族
第二周期第IVA族
,C元素是N
N
(填元素符号)(2)比较D和E简单离子半径的大小(用离子符号表示):
O2->Al3+
O2->Al3+
(3)A和D形成的含18电子化合物的化学式为
H2O2
H2O2
(4)元素E形成的简单离子的水溶液与C的氢化物的水溶液反应的离子方程式为:
Al3++3NH3.H2O=Al(OH)3↓+3NH4+
Al3++3NH3.H2O=Al(OH)3↓+3NH4+
(5)2007年7月2日,美、德两国科学家成功合成了具有独特化学特性的E2A6化合物,该物质在D2中能燃烧,写出它在D2中完全燃烧的化学方程式:
Al2H6+3O2
Al2O3+3H20
| ||
Al2H6+3O2
Al2O3+3H20
.
| ||
2007年4月18日,全国铁路实施第六次大面积提速,这为鲜活水产品的运输提供了有利条件。在鲜活鱼苗的长途运输中,需要保持水中有适量的O2,及时排除CO2,防止细菌大量繁殖。现有四种在水中能起供氧灭菌作用的物质,其性质如下表。你认为长距离运输鲜活鱼苗时应选择( )
| 选项[] | A | B | C | D |
| 物质 | Na2O2 | CaO2 | NaClO | Ca(ClO)2 |
| 溶解性 | 易溶 | 微溶 | 易溶 | 可溶 |
| 化学性质 | 相似 | 相似 | ||