摘要:氯水中存在平衡Cl2 + H2O HCl + HClO.由于2HClO == 2HCl + O2↑.HClO 不断分解.使上述平衡右移.最终Cl2耗尽全部转化为O2.由总关系式为:2Cl2-O2
网址:http://m.1010jiajiao.com/timu_id_438180[举报]
(1)对于下列反应:2SO2+O2?2SO3,如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用SO2浓度变化来表示的化学反应速率为
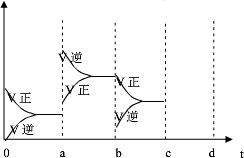
(2)如图表示在密闭容器中反应:2SO2+O2?2SO3△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是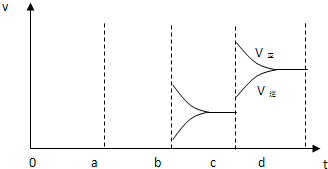
 .
.
(3)请用化学平衡移动知识解释久置的氯水(尤其是长期放置在见光环境),最后浅绿色消失,溶液变成稀盐酸:
查看习题详情和答案>>
2mol/(L?min)
2mol/(L?min)
,用O2浓度变化来表示的反应速率为1mol/(L?min)
1mol/(L?min)
.
(2)如图表示在密闭容器中反应:2SO2+O2?2SO3△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是
升温
升温
;b c过程中改变的条件可能是减小SO3浓度
减小SO3浓度
; 若增大压强时,反应速度变化情况画在c~d处

(3)请用化学平衡移动知识解释久置的氯水(尤其是长期放置在见光环境),最后浅绿色消失,溶液变成稀盐酸:
在氯水中存在平衡:Cl2+H2O?HCl+HClO,HClO见光易分解为HCl和O2,使得平衡体系中HClO浓度减小,平衡向正反应方向移动,Cl2浓度减小.HCl浓度增大,最后浅绿色消失,溶液变成稀盐酸
在氯水中存在平衡:Cl2+H2O?HCl+HClO,HClO见光易分解为HCl和O2,使得平衡体系中HClO浓度减小,平衡向正反应方向移动,Cl2浓度减小.HCl浓度增大,最后浅绿色消失,溶液变成稀盐酸
.在一定温度下,饱和氯水中存在平衡:Cl2+H2O?H++Cl-+HClO.下列说法中,正确的是( )
查看习题详情和答案>>
A.光照一段时间后,
| ||
| B.加入碳酸钙粉末后,溶液的pH增大 | ||
| C.稀释溶液,由水电离的c(H+)减小 | ||
| D.加入NaOH固体,一定有c(Na+)>c(Cl-)>c(H+)>c(ClO-) |
 增大
增大 在新制的氯水中存在平衡:Cl2+H2O
HCl+HClO。加入少量下列物质能使c(HClO)增大
在新制的氯水中存在平衡:Cl2+H2O
HCl+HClO。加入少量下列物质能使c(HClO)增大