摘要:金属晶体:简单立方.钾型.镁型和铜型
网址:http://m.1010jiajiao.com/timu_id_437450[举报]
下列有关晶体的说法错误的是( )
| A、氯化钠晶体中,每个晶胞中平均含有4个钠离子和4个氯离子 | B、在金刚石晶体中,1 mol碳原子形成2 mol碳碳共价键 | C、只有金属Po的晶体采取简单立方堆积,其空间利用率最高 | D、在干冰晶体中,每一个二氧化碳分子周围有12个二氧化碳分子紧密相邻 |
下列有关晶体的说法中,正确的是( )
| A、分子晶体中的分子间作用力越大,分子越稳定 | B、原子晶体中的共价键键长越短、键能越大,晶体的熔点越高 | C、在面心立方堆积的金属晶体中,每个金属原子周围紧邻有4个金属原子 | D、在氯化钠晶体中,钠离子或氯离子的配位数都为8 |
 有A、B、C、D、E、M、X七种元素.其相关信息如下:
有A、B、C、D、E、M、X七种元素.其相关信息如下:| 相关信息 | |
| ① | A的基态原子2p轨道中有三个未成对电子 |
| ② | A、B元素的常见单质是构成空气的主要成分 |
| ③ | C是电负性最大的元素 |
| ④ | D是主族元素,基态原子有四个能层,且最外能层上只有两个电子 |
| ⑤ | D、E、M、X四种元素处于同一周期; M与E又位于同一族,M的原子序数比E多1,M的基态原子中含有三个未成对电子; X原子外围电子排布式为3d104s1 |
(1)A元素的电负性与B的电负性相比,电负性较大的是
O
O
(填写元素符号).M的原子序数为27
27
;X元素在周期表中的位置是第四周期第IB族
第四周期第IB族
.(2)A与C组成AC3分子的VSEPR模型为
四面体
四面体
,AB3-离子的空间构型为平面三角形
平面三角形
.(3)画出B元素原子的核外电子排布图
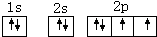

1s22s22p63s23p63d5
1s22s22p63s23p63d5
.;(4)E、X晶体晶体的堆积模型依次为体心立方堆积、面心立方最紧密堆积,其配位数依次为
8、12
8、12
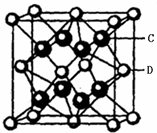
.(5)C与D可形成离子化合物,其晶胞结构如右图所示.若该晶胞的边长为500.0pm.若该晶体的密度为
4.15
4.15
g/cm3(列式并计算).有关晶体的下列说法中不正确的是( )
| A、在NaCl晶体中,距Na+最近的Cl-形成正八面体 | B、在NaCl晶体中,每个晶胞平均占有4个Na+ | C、在CsCl晶体中,每个晶胞平均占有8个Cs+ | D、铜晶体为面心立方堆积,铜原子的配位数(距离一个铜原子最近的其它铜原子的个数)为12 |