网址:http://m.1010jiajiao.com/timu_id_4367370[举报]
在电解质溶液中,阴、阳离子放电的先后顺序为:
(1)阳离子:_________>_________>_________>_________>_________(H+浓度较大时) _________>_________> _________>_________>_________(H+浓度较小时)_________> _________>_________>_________>_________。
(2)阴离子_________>_________>_________>_________>_________>________>________。
查看习题详情和答案>>在电解质溶液中,阴、阳离子放电的先后顺序为:
(1)阳离子:_________>_________>_________>_________>_________(H+浓度较大时) _________>_________> _________>_________>_________(H+浓度较小时)_________> _________>_________>_________>_________。
(2)阴离子_________>_________>_________>_________>_________>________>________。
查看习题详情和答案>>酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、黏合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:CH3COOH+C2H5OH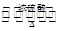 CH3COOC2H5+H2O。请根据要求回答下列问题:
CH3COOC2H5+H2O。请根据要求回答下列问题:
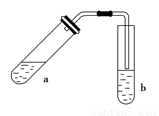
(1)试管a中需加入浓硫酸、冰醋酸和乙醇各2 mL,正确的加入顺序及操作是
________________________________________________________________________。
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是
________________________________________________________________________。
(3)实验中加热试管a的目的是:①__________________;
②________________________________________________________________________。
(4)此反应以浓硫酸为催化剂,可能会造成____________、____________________等问题。
(5)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)。
|
同一反应时间 |
同一反应温度 |
||||
|
反应温度/℃ |
转化率/% |
选择性/% |
反应时间/h |
转化率/% |
选择性/% |
|
40 |
77.8 |
100 |
2 |
80.2 |
100 |
|
60 |
92.3 |
100 |
3 |
87.8 |
100 |
|
80 |
92.6 |
100 |
4 |
92.3 |
100 |
|
120 |
94.5 |
98.7 |
6 |
93.0 |
100 |
|
选择性100%表示反应生成的产物是乙酸乙酯和水 |
①根据表中数据,下列________(填字母)为该反应的最佳条件。
A.120 ℃,4 h B.80 ℃,2 h
C.60 ℃,4 h D.40 ℃,3 h
②当反应温度达到120 ℃时,反应选择性降低的原因可能为
________________________________________________________________________。
查看习题详情和答案>>
 某实验小组的甲同学用如图所示装置制取少量乙酸乙酯(加热设备及夹持固定装置均略去).
某实验小组的甲同学用如图所示装置制取少量乙酸乙酯(加热设备及夹持固定装置均略去).①试管a中需要加入浓硫酸、冰醋酸和乙醇各2mL,正确的加入顺序及操作是
②试管a中加入碎瓷片的作用是
A.立即补加 B.不需补加 C.冷却后补加 D.重新配料
③实验中加热试管a的目的是:
(1)
④试管b中盛有饱和Na2CO3溶液,其作用是
⑤反应结束后,振荡试管b,静置.观察到的现象是
 短周期元素X、Y、Z、W、Q在元素周期表中相对位置如图所示.下列说法正确的是( )
短周期元素X、Y、Z、W、Q在元素周期表中相对位置如图所示.下列说法正确的是( )| A、工业上常用电解法生产Z、Y、Q的单质 | B、形成简单离子的半径顺序r(Z)>r(Q)>r(Y) | C、Z的最高价氧化物对应水化物是三元弱酸 | D、元素W形成氢化物的稳定性比X的强 |