网址:http://m.1010jiajiao.com/timu_id_436279[举报]
第Ⅰ卷(选择题 共45分)
选择题 (1~15题,每题3分,共45分)
题 号
1
2
3
4
5
6
7
8
选 项
B
A
D
D
B
A
D
C
题 号
9
10
11
12
13
14
15
选 项
D
A
B
C
B
C
B
第Ⅱ卷(非选择题 共55分)
说明:1.合理答案均可酌情给分,但不得超过原题分数。
2.若化学方程式2分,不写条件扣1分,不配平扣1分。不写可逆符号扣1分,不得
负分。若化学方程1分,不写条件或不配平不得分。
3.除标注外,其余每空1分,不出现0.5分。
16.(共6分)
(1)4FeS2+11O2  2Fe2O3+8SO2
2Fe2O3+8SO2
(2)C
(3)A B(2分。多选、错选均不得分;选对一个且正确得1分)
(4)氨水 (NH4)2SO3+H2SO4  (NH4)2SO4+H2O+SO2↑(写出NH4HSO3也可)
(NH4)2SO4+H2O+SO2↑(写出NH4HSO3也可)
 17.(共7分)
17.(共7分)
(1)CH3CH2OH
CH2 CH2↑+ H2
O ①④⑤(多选、少选、错选均不
CH2↑+ H2
O ①④⑤(多选、少选、错选均不
得分)
 (2) 三角锥形 3Fe+8H++2NO
(2) 三角锥形 3Fe+8H++2NO
 3Fe2++2NO↑+4H2O
3Fe2++2NO↑+4H2O
(3)Al3+
+3AlO +6H2O
+6H2O  4Al(OH)
3↓ 2Al+2H2O+2OH
4Al(OH)
3↓ 2Al+2H2O+2OH
 2AlO
2AlO +3H2↑
+3H2↑
18.(共9分)
(1)2H2O2 2H2O+ O2↑
2H2O+ O2↑
(2)①③ (2分。多选、错选均不得分;选对一个且正确得1分)
(3)c(S2-)= [c(Na+)+c(H+)
[c(Na+)+c(H+) c (HS-)
c (HS-) c(OH
c(OH )]
)]
或c(S2-)= c (Na+)
c (Na+) c(HS
c(HS )
) c (H2S) (2分)
c (H2S) (2分)
(4)
19.(共8分)
(1)Fe3+、Al3+、Mg2+、H+(多写、少写、写错均不得分)
(2)SiO2+ Si+2CO↑
Si+2CO↑
AlO +CO2+ 2H2 O
+CO2+ 2H2 O  Al(OH)3↓+HCO
Al(OH)3↓+HCO (2分)
(2分)
(3)c d(2分。多选,错选均不得分;选对一个且正确得1分)
(4)电解 防止Mg2+水解,并带走水分,(答出“防止Mg2+水解”即可给分)
20.(共11分)
Ⅰ.(1)分液漏斗
B中棉花位置
①
②
③
④
所蘸试剂
现象
变红
褪色
体现的性质
还原性
(2)I2+SO2+2H2O
 4H+ +SO
4H+ +SO +2I
+2I
Ⅱ.(1)浓H2SO4
(2)Cl2+2I
 I2+2Cl
I2+2Cl b
b
(3)先由紫色变红色,后褪色
(4)5Cl2
+I2+6H2O  10Cl
10Cl +2IO
+2IO +12H+(2分)
+12H+(2分)
21.(共9分)
 |
22.(共5分)
(1)0.01 mol/L?s
(2)③④
(3)75%,<,

有关氢氧化物沉淀的pH见下表:
| 金属阳离子 | 氢氧化物开始沉淀时的pH | 氢氧化物完全沉淀时的pH |
| Fe3+ | 1.9 | 3.2 |
| Mg2+ | 9.4 | 11.6 |
(2)操作④中滤液E与过量CO2反应生成沉淀G的离子方程式为:
(3)操作⑤中调节pH到5~6时,可以用到的试剂(填序号)
a. NaOH溶液 b.氨水 c. Fe2O3 d. Mg(OH)2
(4)从滤液H制取金属Mg的流程如下:

Ⅰ.流程中由滤液H中得到MgCl2?6H2O的方法是
Ⅱ.在干燥的HCl气流中加热MgCl2?6H2O制取无水氯化镁的原因是
Ⅲ.冶炼镁的方法用化学方程式表示为
| ||
| 熔融 |
| ||
| 熔融 |
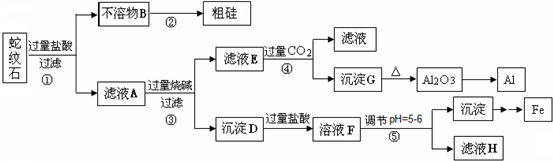
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3和SiO2组成.某实验小组设计如下流程欲分别制得单质Al、Fe、Mg和Si.
有关氢氧化物沉淀的pH见下表:
| 金属阳离子 | 氢氧化物开始沉淀时的pH | 氢氧化物完全沉淀的pH |
| Fe3+ | 1.9 | 3.2 |
| Mg2+ | 9.4 | 11.6 |
(1)滤液A中含有的阳离子有______.
(2)操作②中涉及的化学方程式为______,
操作④中生成沉淀G的离子方程式为______.
(3)操作⑤中调节pH到5~6时,可以用到的试剂(填序号)______.
a.NaOH溶液 b.氨水 c.MgO d.Mg(OH)2
(4)从滤液H制取金属Mg的流程如下:
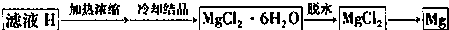
流程中由MgCl2冶炼Mg的方法是______.在干燥的HCl气流中加热MgCl2?6H2O制取无水氯化镁的原因是______. 查看习题详情和答案>>
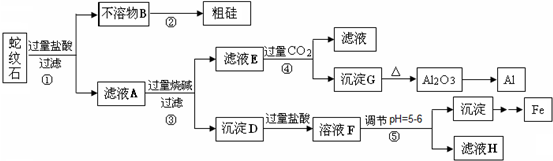
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3和SiO2组成.某实验小组设计如下流程欲分别制得单质Al、Fe、Mg和Si.
有关氢氧化物沉淀的pH见下表:
| 金属阳离子 | 氢氧化物开始沉淀时的pH | 氢氧化物完全沉淀时的pH |
| Fe3+ | 1.9 | 3.2 |
| Mg2+ | 9.4 | 11.6 |
(2)操作④中滤液E与过量CO2反应生成沉淀G的离子方程式为:______.
(3)操作⑤中调节pH到5~6时,可以用到的试剂(填序号)______.
a. NaOH溶液 b.氨水 c. Fe2O3 d. Mg(OH)2
(4)从滤液H制取金属Mg的流程如下:
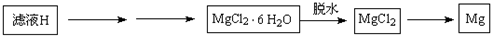
Ⅰ.流程中由滤液H中得到MgCl2?6H2O的方法是______、______、过滤、洗涤;
Ⅱ.在干燥的HCl气流中加热MgCl2?6H2O制取无水氯化镁的原因是______.(应用离子方程式和简要文字说明)
Ⅲ.冶炼镁的方法用化学方程式表示为______. 查看习题详情和答案>>

有关氢氧化物沉淀的pH见下表:
| 金属阳离子 | 氢氧化物开始沉淀时的pH | 氢氧化物完全沉淀的pH |
| Fe3+ | 1.9 | 3.2 |
| Mg2+ | 9.4 | 11.6 |
(1)滤液A中含有的阳离子有______.
(2)操作②中涉及的化学方程式为______ Si+2CO↑ 查看习题详情和答案>>

有关氢氧化物沉淀的pH见下表:
| 金属阳离子 | 氢氧化物开始沉淀时的pH | 氢氧化物完全沉淀时的pH |
| Fe3+ | 1.9 | 3.2 |
| Mg2+ | 9.4 | 11.6 |
(2)操作④中滤液E与过量CO2反应生成沉淀G的离子方程式为:______.
(3)操作⑤中调节pH到5~6时,可以用到的试剂(填序号)______.
a. NaOH溶液 b.氨水 c. Fe2O3 d. Mg(OH)2
(4)从滤液H制取金属Mg的流程如下:

Ⅰ.流程中由滤液H中得到MgCl2?6H2O的方法是______、______、过滤、洗涤;
Ⅱ.在干燥的HCl气流中加热MgCl2?6H2O制取无水氯化镁的原因是______.(应用离子方程式和简要文字说明)
Ⅲ.冶炼镁的方法用化学方程式表示为______熔融Mg+Cl2↑ 查看习题详情和答案>>