摘要:求活创新.凸现能力 从表面形式上看09年的化学试题对元素化合物知识考查有所淡化.事实上这部分内容不但没有淡化.反而在基本概念与理论.化学实验中涉及的更多.这说明09年的化学命题呈现出了更加综合.新颖.灵活的特点.充分体现了对能力考查的加强.这也与新课标倡导的注重过程与方法.学会分析与运用能力有关.能力考查主要集中在知识综合运用.分析推理.实验设计与评价.图标分析与计算技巧等方面.如福建卷第11题就巧妙地把原电池知识与化学平衡状态的判断结合在一起.给人以亮感之觉.更有利于考查对原电池实质.电极判断与化学平衡特征的理解.再如山东卷30题.以分析实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3的实验流程图来设计了离子的除杂.检验.试剂及器材选择.浓度测定等.其实质上就是常见离子的检验.物质的分离.中和滴定等实验的组合及延伸而已.凸现了试题的求活创新特点.较好地考查了学生的实验能力.思维能力.计算能力.知识迁移和类比推理能力.
网址:http://m.1010jiajiao.com/timu_id_4352036[举报]
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养.某同学在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验.
(1)请写出该反应的化学方程式: .
(2)下列收集Cl2的正确装置是: .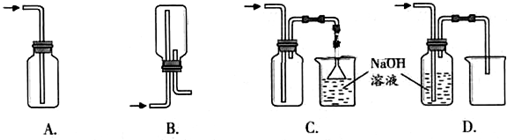
(3)将Cl2通入水中,所得溶液中具有强氧化性的含氯元素的分子有 和 .
(4)该同学设计实验比较Cl2和Br2的氧化性,操作与现象是:取适量NaBr溶液于试管中,用胶头滴管向试管中滴加适量的新制氯水,然后再加入CCl4,振荡静置,观察现象.此时液体分层,下层溶液呈 .写出此置换反应的化学方程式: .
查看习题详情和答案>>
(1)请写出该反应的化学方程式:
(2)下列收集Cl2的正确装置是:

(3)将Cl2通入水中,所得溶液中具有强氧化性的含氯元素的分子有
(4)该同学设计实验比较Cl2和Br2的氧化性,操作与现象是:取适量NaBr溶液于试管中,用胶头滴管向试管中滴加适量的新制氯水,然后再加入CCl4,振荡静置,观察现象.此时液体分层,下层溶液呈
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养.
(1)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验.写出制取Cl2的离子方程式 ;某小组要从该混合物中回收MnO2并提取MnCl2晶体,则要多次用到的玻璃仪器是 .
(2)下图A~G都是常见的与气体制备、收集、尾气吸收有关的装置.例如,B、C都可以收集H2、CH4、NH3、Cl2等.如果收集Cl2并进行尾气处理,不能选用 ;如用B收集Cl2,应该从 (甲、乙)端进气.
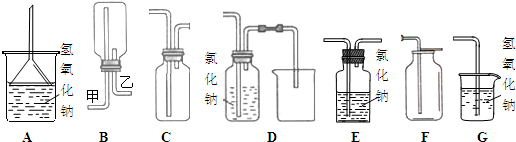
(3)工业常用Cl2从海水中制备Br2,反应离子方程式是 .实验室模拟该实验,分离出Br2的操作是:取混合溶液于分液漏斗中,加入CCl4,振荡,静置分层, .
(4)次氯酸盐有强氧化性,如NaClO可以氧化NH3制备高能燃料N2H4,反应方程式是: .现有14.9g NaClO最多可以制备 mol N2H4.
查看习题详情和答案>>
(1)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验.写出制取Cl2的离子方程式
(2)下图A~G都是常见的与气体制备、收集、尾气吸收有关的装置.例如,B、C都可以收集H2、CH4、NH3、Cl2等.如果收集Cl2并进行尾气处理,不能选用

(3)工业常用Cl2从海水中制备Br2,反应离子方程式是
(4)次氯酸盐有强氧化性,如NaClO可以氧化NH3制备高能燃料N2H4,反应方程式是:
(2012?开封一模)1.某化工厂排放的污水中,常溶有某些对人体有害的物质,初步认为可能含有Fe3+、Ba2+、K+、OH-、Cl-、CO2-3、SO2-4.为了进一步确认,取样进行实验检测:
①取污水仔细观察,呈无色、透明、均一状态.
②向取样的污水中,滴入稀硫酸,有大量白色沉淀产生,再加稀硝酸,白色沉淀不消失.
③用pH试纸测定污水的pH,试纸显深蓝色.
(1)由此可知,该污水中肯定含有的离子是
(2)简述通过实验进一步确定溶液中可能存在离子的操作步骤及现象
2.实验室为化学兴趣小组的同学准备了四种红色溶液,它们分别可能是KMnO4酸性溶液、滴有酚酞的NaOH溶液、滴有石蕊的稀硫酸和品红溶液.另外还提供了常见的仪器和药品.为了培养同学们的创新精神和实践能力,只允许选用一种试剂对上述四种溶液加以鉴别.
(1)甲组同学选用了FeCl2溶液,试写出该组同学鉴别出NaOH溶液的有关离子方程式:
(2)乙组同学选用了Na2SO3溶液,他们直接能鉴别出来的溶液及对应的现象分别是
(3)丙组同学选用了一种试剂,一次性鉴别出上述四种溶液,他们选择的试剂可能是
查看习题详情和答案>>
①取污水仔细观察,呈无色、透明、均一状态.
②向取样的污水中,滴入稀硫酸,有大量白色沉淀产生,再加稀硝酸,白色沉淀不消失.
③用pH试纸测定污水的pH,试纸显深蓝色.
(1)由此可知,该污水中肯定含有的离子是
Ba2+、OH-
Ba2+、OH-
,肯定没有的离子是Fe3+、CO32-、SO42-
Fe3+、CO32-、SO42-
,可能含有的离子是K+、Cl-
K+、Cl-
.(2)简述通过实验进一步确定溶液中可能存在离子的操作步骤及现象
用铂丝蘸取少量的待测液在酒精灯上灼烧,透过蓝色的钴玻璃观察,若发现火焰呈现紫色,则说明含有钾离子,另取少量的待测液于一支洁净的试管中,加几滴硝酸银,若有白色沉淀生成,再加入硝酸,沉淀不溶解,证明含有氯离子
用铂丝蘸取少量的待测液在酒精灯上灼烧,透过蓝色的钴玻璃观察,若发现火焰呈现紫色,则说明含有钾离子,另取少量的待测液于一支洁净的试管中,加几滴硝酸银,若有白色沉淀生成,再加入硝酸,沉淀不溶解,证明含有氯离子
.2.实验室为化学兴趣小组的同学准备了四种红色溶液,它们分别可能是KMnO4酸性溶液、滴有酚酞的NaOH溶液、滴有石蕊的稀硫酸和品红溶液.另外还提供了常见的仪器和药品.为了培养同学们的创新精神和实践能力,只允许选用一种试剂对上述四种溶液加以鉴别.
(1)甲组同学选用了FeCl2溶液,试写出该组同学鉴别出NaOH溶液的有关离子方程式:
Fe2++2OH-=Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4Fe(OH)3
Fe2++2OH-=Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4Fe(OH)3
;(2)乙组同学选用了Na2SO3溶液,他们直接能鉴别出来的溶液及对应的现象分别是
KMnO4酸性溶液、硫酸溶液;红色褪去、产生无色有刺激性气味的气体
KMnO4酸性溶液、硫酸溶液;红色褪去、产生无色有刺激性气味的气体
;(3)丙组同学选用了一种试剂,一次性鉴别出上述四种溶液,他们选择的试剂可能是
(NH4)2SO3或NH4HSO3或(NH4)2S
(NH4)2SO3或NH4HSO3或(NH4)2S
.
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养.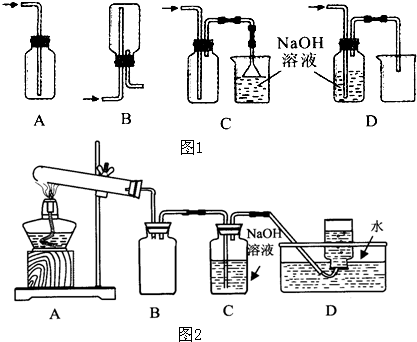
(1)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验,如图1所示.
①写出该反应的离子方程式 ;
②下列收集Cl2的装置正确装置是 ;
③将Cl2通入水中,所得溶液中具有氧化性的含氯粒子是 ;
④设计实验比较Cl2和Br2的氧化性,操作与现象是:取少量新制氯水和CCl4于试管中, .
(2)某化学兴趣小组为了探究AgNO3的热稳定性,设计了如下实验.
用如图2所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体.当反应结束以后,试管中残留固体为黑色.
①装置B的作用是 .
②经小组讨论并验证该无色气体为O2,其验证方法是 .
【查阅资料】Ag2O和粉末的Ag均为黑色;Ag2O可溶于氨水.
【提出假设】试管中残留的黑色固体可能是:ⅠAg;ⅡAg2O;ⅢAg和Ag2O
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验.
【实验评价】根据上述实验,③不能确定固体产物成分的实验是 (填实验编号).
【实验结论】根据上述实验结果,④该小组得出的AgNO3固体热分解的化学方程式为 .
查看习题详情和答案>>

(1)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验,如图1所示.
①写出该反应的离子方程式
②下列收集Cl2的装置正确装置是
③将Cl2通入水中,所得溶液中具有氧化性的含氯粒子是
④设计实验比较Cl2和Br2的氧化性,操作与现象是:取少量新制氯水和CCl4于试管中,
(2)某化学兴趣小组为了探究AgNO3的热稳定性,设计了如下实验.
用如图2所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体.当反应结束以后,试管中残留固体为黑色.
①装置B的作用是
②经小组讨论并验证该无色气体为O2,其验证方法是
【查阅资料】Ag2O和粉末的Ag均为黑色;Ag2O可溶于氨水.
【提出假设】试管中残留的黑色固体可能是:ⅠAg;ⅡAg2O;ⅢAg和Ag2O
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验.
| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硝酸,振荡 | 黑色固体溶解,并有气体产生 |
【实验结论】根据上述实验结果,④该小组得出的AgNO3固体热分解的化学方程式为
