摘要:前线轨道理论: 化学反应的本质是电子转移.最容易的电子转移必然是:发生在:电子从最高占据轨道转移到最低空轨道.所以.从电子转移的角度说.化学反应只有一种可能的反应模式即: 前线轨道理论的应用-环加成反应: 反应条件:加热△与光照hn虽然都是提供能量的手段.但它们绝然不同. 热量是连续的物理量.分子中的电子能是量子化的物理量.按照物理学的基本原理.这两类不同性质的物理量不同相互转化.因此在加热条件下.电子不可能被激发.分子处于基态. 而光能是量子化的物理量.在光照条件下.电子可以吸收相应的光能被激发.体系中既有基态分子.也有激发态分子(但体系中的分子不可能同时被激发). 激发态分子的HOMO 和 LUMO与基态分子不同.如: 分子的 HOMO 和 LUMO与反应的条件相关: 乙烯 丁二烯 苯 HOMO 基态(△): p ψ2 ψ2 或 ψ3 激发态(hn): p* ψ3* ψ4*或ψ5* LUMO 基态(△): p* ψ3* ψ4*或ψ5* 激发态(hn): σ* ψ4* ψ5*或ψ4* 在环加成反应中.如果一个分子的HOMO和另一个分子的LUMO的节面都是奇数.那么它们可以实现同号重迭.两个分子的MO之间不存在节面.电子可以顺利发生转移.反应则是允许的.否则是禁阻的. 如: 4 + 2 反应(Alder-Diels反应.加热允许.hv禁阻): 在加热条件下.丁二烯和乙烯体系都处于基态.丁二烯的HOMO是y2 .只有1个节面.乙烯的LUMO是p*.也只有1个节面.二者节面都是奇数.所以反应是加热允许的.当然.也可以用丁二烯的LUMO-y*3和乙烯的HOMO-p来判断.二者都有2个节面.节面同为偶数.也是加热允许的: 在光照条件下.如果丁二烯被激发.其HOMO为y3*1.而乙烯处于基态.其LUMO为p*.前者有2个节面.后者只有1个节面.所以是禁阻的,如果乙烯被激发.只能使用其HOMO-p*1.而基态丁二烯必然使用其LUMO-y3*0.同样是禁阻的: 2+2反应 在加热条件下.乙烯都处于基态.一个分子的HOMO(为p)与另一个分子的LUMO.节面数目偶奇不同.所以2+2反应加热是禁阻的. 在光照条件下.体系中既有基态乙烯分子.也有激发态乙烯分子.反应可以在激发态乙烯的HOMO-p*1与基态乙烯分子的LUMO-p*0之间进行.二者相同.当然节面都是奇数(1个).所以2+2反应是光照允许的. 环加成反应的选择性: ①烯烃构型保持:4+2和2+2都是同面-同面反应.平面内的构型在反应中保留. ②4+2反应次级效应和空间效应:endo和exo exo endo Y饱和 主 次 Y不饱和 次 主 如: ③4+2的区域选择性──邻对位规则
网址:http://m.1010jiajiao.com/timu_id_4283006[举报]
图1是元素周期表的前三周期,回答下列问题:
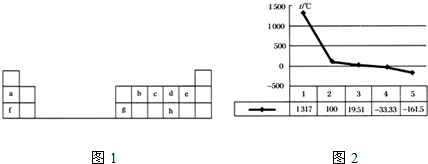
(1)g的单质能与f元素的最高价氧化物对应水化物的溶液反应,请写出该反应的离子方程式
(2)a、b、c、d、e的氢化物的沸点直角坐标图如图2所示,序号“5”的氢化物的化学式为
(3)电子排布式为[Ne]3s23p4的元素名称为
查看习题详情和答案>>

(1)g的单质能与f元素的最高价氧化物对应水化物的溶液反应,请写出该反应的离子方程式
2OH-+2Al+2H2O═2AlO2-+3H2↑
2OH-+2Al+2H2O═2AlO2-+3H2↑
.(2)a、b、c、d、e的氢化物的沸点直角坐标图如图2所示,序号“5”的氢化物的化学式为
CH4
CH4
,并用杂化轨道理论解释该分子在空间的立体构型在形成CH4分子时,碳原子的2s轨道和3个2p轨道会发生杂化形成4个能量相等的sp3杂化轨道,4个sp3杂化轨道分别与4个氢原子的1s轨道重叠形成CH4分子,sp3杂化轨道的夹角为109°28′,所以呈正四面体形
在形成CH4分子时,碳原子的2s轨道和3个2p轨道会发生杂化形成4个能量相等的sp3杂化轨道,4个sp3杂化轨道分别与4个氢原子的1s轨道重叠形成CH4分子,sp3杂化轨道的夹角为109°28′,所以呈正四面体形
.(3)电子排布式为[Ne]3s23p4的元素名称为
硫
硫
,其氢化物的立体构型为V形
V形
,并用价层电子对互斥理论模型解释该分子在空间的立体构型H2S的中心原子硫原子上有2对孤电子对,跟中心原子周围的2个σ键加起来是4,它们相互排斥,形成四面体,但四面体的两个顶点被孤电子对占据,所以H2S分子呈V形
H2S的中心原子硫原子上有2对孤电子对,跟中心原子周围的2个σ键加起来是4,它们相互排斥,形成四面体,但四面体的两个顶点被孤电子对占据,所以H2S分子呈V形
.有关“物质和结构”研究方法的表述错误的是( )
| A、价层电子对互斥理论不能预测所有分子的立体结构 | B、杂化轨道理论是鲍林为了解释分子的立体结构提出来的 | C、金属和非金属、无机物和有机物之间并没有严格的界限,分类的研究方法不科学 | D、规律是对经常出现的客观现象的归纳,对例外的深入探究是科学发展的内在动力 |
用VSEPR模型和杂化轨道理论相关知识填表:
查看习题详情和答案>>
| 分子或离子 | 孤对电子对数 | 杂化轨道数 | 中心原子轨道杂化形式 | 分子或离子的立体结构 | ||
| NH3 | ||||||
| BeCI2 | ||||||
| SO3 | ||||||
NH
|
||||||
SO
|
||||||
| NCI2 |
下列叙述不正确的是( )
| A、分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构 | B、分子中中心原子通过sp2杂化轨道成键时,该分子不一定为平面三角形 | C、杂化轨道理论与价层电子互斥理论都可以分析分子的空间构型 | D、四面体型结构的分子一定是非极性分子 |
[化学选修物质结构与性质]图1中几种“俄罗斯方块”均裁剪于长式元素周期表.特同答下列问题:
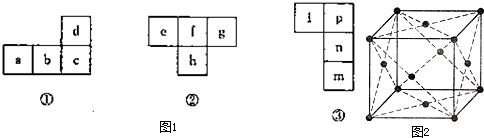
(1)a、d都是日常生活中的常见金属,常温下d在浓硝酸中发生钝化,则:元素c在周期表中的位置为第 周期 族; a的单质晶胞结构如图2.构成晶体的微粒之间的作用为 .每个晶胞中含有的原 子数为 个,晶体巾距离每个a原子最近且等距离的a原子有 个.
(2)短周期元素h的最外层电子数是其核外电子总数的
,则e、f、g的简单氢化物的沸点由高到低的次序为: > > (用化学式表达),根据杂化轨道理论和价层电子对互斥理论,h的三氯化物中h原子的杂化类型为 ,分子的空间形状为: .
(3)n的双原子分子常温下为液态.则图23一③中的四种元素均属于周期表的 区元素,m、n、p元素的电负性依次 (填“增强”或“减弱”).
查看习题详情和答案>>

(1)a、d都是日常生活中的常见金属,常温下d在浓硝酸中发生钝化,则:元素c在周期表中的位置为第
(2)短周期元素h的最外层电子数是其核外电子总数的
| 1 | 3 |
(3)n的双原子分子常温下为液态.则图23一③中的四种元素均属于周期表的