摘要:卤素的特殊性 (1)碘单质遇淀粉显示出蓝色.该性质可用于检验Cl2.Cl2可使湿润的KI淀粉试纸变蓝.实质是:Cl2+2I-===I2+2Cl-.I2再作用于淀粉显示出蓝色.另外碘单质还易升华. (2)氢氟酸能腐蚀玻璃(4HF+SiO2===SiF4↑+2H2O).因此.氢氟酸必须保存在塑料试剂瓶中.制备HF时.反应必须在铅制器皿中进行. (3)氯气具有漂白性.其实质是Cl2与H2O反应生成的次氯酸具强氧化性使有机色质褪色.次氯酸是一种强氧化性的弱酸.
网址:http://m.1010jiajiao.com/timu_id_4240390[举报]
(1)已知钠能与液氨(NH3)发生反应,且跟钠与水的反应相似,写出钠与液氨反应的化学方程式
(2)已知SO2能被Cl2氧化成+6价的SO3,而氯元素本身被还原成-1价的氯,试写出Cl2将SO2的水溶液氧化成硫酸的离子方程式
(3)卤素互化物也称类卤互或拟卤素(如ICl、IBr等),其化学性质与卤素的性质相似,可与水发生反应生成卤化氢和次卤酸.试写出BrCl与水发生反应的化学反应方程式
查看习题详情和答案>>
2Na+2NH3═2NaNH2+H2↑
2Na+2NH3═2NaNH2+H2↑
;(2)已知SO2能被Cl2氧化成+6价的SO3,而氯元素本身被还原成-1价的氯,试写出Cl2将SO2的水溶液氧化成硫酸的离子方程式
Cl2+SO2+2H2O═4H++SO42-+2Cl-
Cl2+SO2+2H2O═4H++SO42-+2Cl-
;(3)卤素互化物也称类卤互或拟卤素(如ICl、IBr等),其化学性质与卤素的性质相似,可与水发生反应生成卤化氢和次卤酸.试写出BrCl与水发生反应的化学反应方程式
BrCl+H2O═HBrO+HCl
BrCl+H2O═HBrO+HCl
. (2010?枣庄一模)卤素单质的性质活泼,卤素的化合物应用广泛,研究卤素单质及其化合物具有重要意义.
(2010?枣庄一模)卤素单质的性质活泼,卤素的化合物应用广泛,研究卤素单质及其化合物具有重要意义.(1)氯元素的原子结构示意图为


(2)二氧化氯(ClO2)是一种广泛用于水处理消毒剂,与Cl2相比,ClO2不但具有更显著的杀菌能力,而且不会产生对人体有害的有机氯化物.制备ClO2的方法有以下两种:
2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O…①
2NaClO2+H2O2+H2SO4=2C1O2↑+O2↑+Na2SO4+2H2O …②
你认为哪种方法最佳
②
②
(填序号),理由是ClO2中混有O2,不会产生对人体有害的物质
ClO2中混有O2,不会产生对人体有害的物质
.(3)工业上用电解饱和食盐水的方法制取烧碱和氯气,请写出反应的离子方程式
2C1-+2H2O
Cl2↑+H2↑+2OH-
| ||
2C1-+2H2O
Cl2↑+H2↑+2OH-
.
| ||
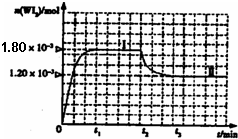
(4)碘钨灯具有比白炽灯寿命长且环保节能的特点.一定温度下,灯泡内封存的少量碘与使用过程中沉积在管壁上的钨可以发生反应:W(s)+I2(g)
的密闭容器中,加热使其反应.如图是WI2(g)的物质的量随时间变化关系图象,其中曲线I(0~t2时间段)的反应温度为T1,曲线II(从t2开始)的反应温度为T2,且T2>T1.则:
①该反应的△H
小于
小于
0(填“大于”或“等于”或“小于”)②从反应开始到t1时间内的平均反应速率v(I2)=
| 0.036 |
| t1 |
| 0.036 |
| t1 |
③下列说法中不正确的是
A
A
(填序号).A.该反应的平衡常数表达式是K=
| [WI2] |
| [W][I2] |
B.灯丝附近温度越高,灯丝附近区域WI2越易变为W而重新沉积到灯丝上
C.利用该反应原理可以提纯钨
(5)25℃时,向5mL含有KCl和KI浓度均为0.1mol/L的混合液中,滴加6mL0.1mol/L的AgNO3溶液,先生成的沉淀是
AgI
AgI
,溶液中离子浓度由大到小的顺序是c(K+)>c(NO-3)>c(Cl-)>c(Ag+)>c(I-)
c(K+)>c(NO-3)>c(Cl-)>c(Ag+)>c(I-)
[不考虑H+和OH-.25℃时KSP(AgCl)=1.8×10-10、KSP(AgI)=8.3×10-17].(6)Mg常用作提纯Ti的试剂,已知:
①Mg(s)+Cl2(g)=MgCl2(s)△H=-641kJ/mol
②Ti(s)+2Cl2(g)=TiCl4(l)△H=-770kJ/mol
请写出Mg与液态TiCl4反应提纯钛的热化学方程式
2Mg(s)+TiCl4(1)=2MgCl2(s)+Ti(s)△H=-512kJ?mol-1
2Mg(s)+TiCl4(1)=2MgCl2(s)+Ti(s)△H=-512kJ?mol-1
.海水中含有多种盐类,除可获得NaCl、MgCl2外,也是自然界提取卤素的重要来源.
(1)由于溴离子在海水中浓度很低(0.067g/L),要进行溴元素的浓缩、富集.实验室若要直接浓缩海水时,下面的仪器肯定不需要的是(填编号)
A.玻璃棒 B.三脚架 C.酒精灯 D.蒸发皿 E.坩埚
(2)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的.吸收工艺常用的方法是“空气吹出法”,其原理为:SO2+Br2+2H2O=2HBr+H2SO4.另一种方法是用纯碱浓溶液代替SO2吸收溴,请完成下列方程式的配平(酸性条件下该反应逆向进行):
(3)现有一份吸收了溴的无色溶液(采用上述两种方法之一,且吸收剂和溴恰好完全反应),请你通过实验探究该溶液究竟是采用那种方法吸收溴的.
①提出合理假设 (以下可不填满)
假设1:采用纯碱吸收法,吸收液中含大量Na+、Br -、BrO3-.
假设2:
假设3:
②设计方案、进行实验,验证假设:请在表中写出实验步骤以及预期现象和结论.限选实验试剂和仪器:10mL量筒、小烧杯、试管、胶头滴管;无水乙醇、苯、0.10mol/LAgNO3、0.10mol/LBaCl2、2mol/LHCl
查看习题详情和答案>>
(1)由于溴离子在海水中浓度很低(0.067g/L),要进行溴元素的浓缩、富集.实验室若要直接浓缩海水时,下面的仪器肯定不需要的是(填编号)
E
E
:A.玻璃棒 B.三脚架 C.酒精灯 D.蒸发皿 E.坩埚
(2)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的.吸收工艺常用的方法是“空气吹出法”,其原理为:SO2+Br2+2H2O=2HBr+H2SO4.另一种方法是用纯碱浓溶液代替SO2吸收溴,请完成下列方程式的配平(酸性条件下该反应逆向进行):
3
3
Na2CO3+3
3
Br2=5
5
NaBr+1
1
NaBrO3+3CO2↑
3CO2↑
(3)现有一份吸收了溴的无色溶液(采用上述两种方法之一,且吸收剂和溴恰好完全反应),请你通过实验探究该溶液究竟是采用那种方法吸收溴的.
①提出合理假设 (以下可不填满)
假设1:采用纯碱吸收法,吸收液中含大量Na+、Br -、BrO3-.
假设2:
采用空气吹出吸收法,吸收液中含大量H+、Br-、SO42-
采用空气吹出吸收法,吸收液中含大量H+、Br-、SO42-
.假设3:
无
无
.②设计方案、进行实验,验证假设:请在表中写出实验步骤以及预期现象和结论.限选实验试剂和仪器:10mL量筒、小烧杯、试管、胶头滴管;无水乙醇、苯、0.10mol/LAgNO3、0.10mol/LBaCl2、2mol/LHCl
| 实验步骤 | 预期现象和结论 |
| 步骤1:用量筒取样品溶液2mL于试管中,再滴加足量的2mol/L盐酸,充分振荡,观察 | 若 溶液由无色变黄色 溶液由无色变黄色 ,则假设1可能成立;若溶液无明显变化 溶液无明显变化 ,则假设2可能成立 假设2可能成立 . |
| 步骤2:往步骤1 的试管中加入 1mL苯 1mL苯 ,充分振荡,观察 |
若溶液分层,上层有机层出现橙色或橙红色,则假设2成立; 若溶液只分层,无颜色变化,则假设1成立 若溶液分层,上层有机层出现橙色或橙红色,则假设2成立; 若溶液只分层,无颜色变化,则假设1成立 |
氰[(CN)2]为无色可燃气体、剧毒、有苦杏仁味,是拟卤素的一种.拟卤素的性质与卤素相似.
(1)写出氰与苛性钠溶液反应的化学方程式: .
(2)已知氰分子中键角为180°,分子具有对称性,(CN)2的结构式为 ,(CN)2的分子为(填“极性”或“非极性”) 分子.
(3)CN-中电子数为 .
查看习题详情和答案>>
(1)写出氰与苛性钠溶液反应的化学方程式:
(2)已知氰分子中键角为180°,分子具有对称性,(CN)2的结构式为
(3)CN-中电子数为
(11分)某液态卤代烷RX(R是烷基,X是某种卤素原子)的密度是a g/cm3。该RX可以跟稀碱发生水解反应生成ROH(能跟水互溶)和HX。为了测 定RX的相对分子质量,拟定的实验步骤如下:①准确量取该卤代烷b mL,放入锥形瓶中。②在锥形瓶中加入过量稀NaOH溶液,塞上带有长玻璃管的塞子,加热,发生反应。③反应完成后,冷却溶液,加稀HNO3酸化,滴加AgNO3溶液,得白色沉淀。④过滤、洗涤、干燥后称重,得到c g固体。
定RX的相对分子质量,拟定的实验步骤如下:①准确量取该卤代烷b mL,放入锥形瓶中。②在锥形瓶中加入过量稀NaOH溶液,塞上带有长玻璃管的塞子,加热,发生反应。③反应完成后,冷却溶液,加稀HNO3酸化,滴加AgNO3溶液,得白色沉淀。④过滤、洗涤、干燥后称重,得到c g固体。
完成下面问题:
(1)装置中长玻璃管的作用是_________________。
(2)步骤④中,洗涤的目的是为了除去沉淀物上吸附的____________离子。
(3)该卤代烷中所含卤素的名称是_________,判断的依据是___ ________________________________________________。
(4)该卤代烷的相对分子质量是____________ (列出算式)。
(5)如果在步骤③中加入HNO3的量不足,没有将溶液酸化,则步骤④中测得的c值(填下列选项代码) ____________。
| A.偏大 | B.偏小 |
| C.不变 | D.大小不定 |