摘要:SiO2有哪些用途? [过渡]
网址:http://m.1010jiajiao.com/timu_id_4231596[举报]
(2011?自贡模拟)TiO2在工业生产和日常生活中有重要用途.
I.工业上用钛矿石(FeTiO3,含FeO、Al2O3、SiO2等杂质)经过下述反应制得:

其中,步骤②发生的反应为:2H2SO4+FeTiO3=TiOSO4+FeSO4+2H2O.
(1)净化钛矿石时,是否需要除去杂质FeO?答:
(2)净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的化学方程式.
II.TiO2可通过下述两种方法制备金属钛:
“方法一”是电解TiO2来获得Ti:将处理过的TiO2作阴极,石墨为阳极,熔融CaO为电解液,用碳块作电解槽池.
(3)阴极反应的电极反应式为
“方法二”是先将TiO2与Cl2、C反应得到TiCl4,再用镁还原得到Ti.因下述反应难于发生:
TiO2(s)+2Cl2(g)?TiCl4(l)+O2(g)△H=+151kJ?mol-1所以不能直接由TiO2和Cl2反应(即氯化反应)来制取TiCl4.当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行.
(4)已知:C(s)+O2(g)=CO2(g);△H=-394kJ?mol-1.
请写出TiO2与Cl2、C反应制各TiCl4的热化学方程式:
(5)从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因.
查看习题详情和答案>>
I.工业上用钛矿石(FeTiO3,含FeO、Al2O3、SiO2等杂质)经过下述反应制得:

其中,步骤②发生的反应为:2H2SO4+FeTiO3=TiOSO4+FeSO4+2H2O.
(1)净化钛矿石时,是否需要除去杂质FeO?答:
不需要
不需要
(填“需要”或“不需要”).(2)净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的化学方程式.
Al2O3+2NaOH=2NaAlO2+H2O
Al2O3+2NaOH=2NaAlO2+H2O
;SiO2+2NaOH=Na2SiO3+H2O
SiO2+2NaOH=Na2SiO3+H2O
.II.TiO2可通过下述两种方法制备金属钛:
“方法一”是电解TiO2来获得Ti:将处理过的TiO2作阴极,石墨为阳极,熔融CaO为电解液,用碳块作电解槽池.
(3)阴极反应的电极反应式为
TiO2+4e-=Ti+2O2-
TiO2+4e-=Ti+2O2-
.“方法二”是先将TiO2与Cl2、C反应得到TiCl4,再用镁还原得到Ti.因下述反应难于发生:
TiO2(s)+2Cl2(g)?TiCl4(l)+O2(g)△H=+151kJ?mol-1所以不能直接由TiO2和Cl2反应(即氯化反应)来制取TiCl4.当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行.
(4)已知:C(s)+O2(g)=CO2(g);△H=-394kJ?mol-1.
请写出TiO2与Cl2、C反应制各TiCl4的热化学方程式:
TiO2(s)+2Cl2(g)+C(s)=TiCl4(l)+CO2(g);△H=-243KJ?mol-1
TiO2(s)+2Cl2(g)+C(s)=TiCl4(l)+CO2(g);△H=-243KJ?mol-1
.(5)从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因.
如图所示是电子工业中某原料的生产流程,其中反应②③是你在课本习题中见过,其目的是为了提纯B;物质A-H均为短周期元素组成;G为五原子非极性分子;A-D均是单质且元素原子的最外层电子数目的关系为C>A=B>D;H极易溶于水,且其水溶液为-种强酸.

请回答下列问题:
(1)B的电子排布式:
(2)反应①的化学方程式:
(3)与反应①类型相同,且两种单质分属同一主族和不同主族的反应,用化学方程式各写-例:
①单质属同-主族:
(4)F在工业上有多种用途,写出其中一种用途的化学方程式:
查看习题详情和答案>>

请回答下列问题:
(1)B的电子排布式:
1s22s22p63s23p2
1s22s22p63s23p2
;固体E的晶体类型原子晶体
原子晶体
;H中的键型为δ
δ
(填“π”或“δ”);(2)反应①的化学方程式:
SiO2+2C
Si+2CO↑
| ||
SiO2+2C
Si+2CO↑
.
| ||
(3)与反应①类型相同,且两种单质分属同一主族和不同主族的反应,用化学方程式各写-例:
①单质属同-主族:
2H2S+O2=2S↓+2H2O
2H2S+O2=2S↓+2H2O
;②单质属不同主族:2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
.
| ||
(4)F在工业上有多种用途,写出其中一种用途的化学方程式:
3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
.
| ||
(2013?德阳模拟)重铬酸钠(Na2Cr2O7?2H2O)俗称红矾钠,在工业方面有广泛用途.我国目前主要是以铬铁矿(主要成份为FeO?Cr2O3,还含有Al2O3、MgO、SiO2等杂质)为主要原料进行生产,其主要工艺流程如下:

①中涉及的主要反应有:
主反应:4FeO?Cr2O3+8Na2CO3+7O2
8Na2CrO4+2Fe2O3+8CO2
副反应:SiO2+Na2CO3
Na2SiO3+CO2↑、Al2O3+Na2CO3
2NaAlO2+CO2↑
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
试回答下列问题:
(1)“①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是
(2)“③”中调节pH至4.7,目的是
(3)“⑤”中加硫酸酸化的目的是使CrO42-转化为Cr2O72-,请写出该平衡转化的离子方程式:
(4)称取重铬酸钠试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol?L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol?L-1Na2S2O3标准溶液滴定
(I2+2S2O32-=2I-+S4O62-).
①判断达到滴定终点的依据是:
②若实验中共用去Na2S2O3标准溶液40.00ml,所得产品的中重铬酸钠的纯度(设整个过程中其它杂质不参与反应)
查看习题详情和答案>>

①中涉及的主要反应有:
主反应:4FeO?Cr2O3+8Na2CO3+7O2
| ||
副反应:SiO2+Na2CO3
| ||
| ||
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
| 完全沉淀时溶液pH | 4.7 | 3.7 | 11.2 | 5.6 |
(1)“①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是
使反应物接触更充分,加快反应速率
使反应物接触更充分,加快反应速率
(2)“③”中调节pH至4.7,目的是
除去溶液中的AlO2-、SiO32-
除去溶液中的AlO2-、SiO32-
.(3)“⑤”中加硫酸酸化的目的是使CrO42-转化为Cr2O72-,请写出该平衡转化的离子方程式:
2CrO42-+2H+ Cr2O72-+H2O
Cr2O72-+H2O
 Cr2O72-+H2O
Cr2O72-+H2O2CrO42-+2H+ Cr2O72-+H2O
Cr2O72-+H2O
. Cr2O72-+H2O
Cr2O72-+H2O(4)称取重铬酸钠试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol?L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol?L-1Na2S2O3标准溶液滴定
(I2+2S2O32-=2I-+S4O62-).
①判断达到滴定终点的依据是:
当滴加最后一滴硫代硫酸钠溶液时,溶液蓝色褪去,半分钟内不变色
当滴加最后一滴硫代硫酸钠溶液时,溶液蓝色褪去,半分钟内不变色
;②若实验中共用去Na2S2O3标准溶液40.00ml,所得产品的中重铬酸钠的纯度(设整个过程中其它杂质不参与反应)
83.84%
83.84%
. 已知A、B、C、D组成的元素都属于短周期,它们之间的简单转化关系如图所示.
已知A、B、C、D组成的元素都属于短周期,它们之间的简单转化关系如图所示.请按要求写出有关反应的化学方程式:
(1)若其中A、D为单质且同主族,B、C为氧化物:(该反应在工业上有重要用途)
2C+SiO2
Si+2CO↑
| ||
2C+SiO2
Si+2CO↑
.
| ||
(2)若A、D为常态下的气体单质且不同主族,B、C为化合物且B为水:
2F2+2H2O═4HF+O2
2F2+2H2O═4HF+O2
.(3)若A、B、C均为化合物且C为水,单质D常态下为固体:
SO2+2H2S═3S+2H2O
SO2+2H2S═3S+2H2O
.(4)若A、B、C均为氧化物,D为单质,反应是在高温下进行:
CO+H2O(g)
CO2+H2
| ||
CO+H2O(g)
CO2+H2
.
| ||
(5)若A、D为固体单质且不同主族,B、C为氧化物:
2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
.
| ||
(20分)
(I)多项选择题(6分)
下列关于水处理的说法正确的是 。
A.FeSO4·7H2O是常用的混凝剂,它除去悬浮固体颗粒的过程只是物理过程
B.用纯碱和生石灰处理硬水,既可以除去暂时硬度,也可以除去永久硬度
C.永久硬度的水可以采用离子交换法进行软化,其主要就是利用了离子交换膜技术
D.污水处理中的三级处理是采用化学方法,对污水进行深度处理和净化
E.电渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜
(II)(14分)
下列是工业合成氨的简要流程示意图:
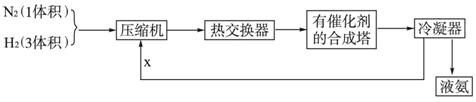
请回答下列问题:
(1)H2通常用碳氢化合物与水反应,写出有关的反应方程式 ,从冷凝器回流到压缩机中的X是 。
(2)比较工业上合成氨和SO2的催化氧化反应,其生产条件有哪些异同,并解释原因
。
(3)将N2、H2按体积比1∶3进入合成塔,从合成塔出来的混合气中,氨的体积分数为15%,则H2的体积分数为______________。
(4)NH3的用途之一是制造化肥,但在化肥的使用过程中要注意铵态氮肥不可以和草木灰混用,解释其原因 。
(5)NH3是一种重要的化工原料,除了制造化肥之外,再列举出两种NH3的用途
。
查看习题详情和答案>>