网址:http://m.1010jiajiao.com/timu_id_4224093[举报]
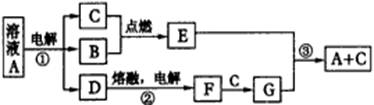
(08上海重点中学第二次联考)A、B、C、D、E、F、G是由短周期元素组成的七种物质,其中B、C、F是单质;常温下B、C、E为气体;A物质的焰色反应呈黄色。(下图中反应②的部分产物未表示出来。)
|
各物质间的转化关系 |
根据上图所示转化关系回答:
(1)经测定G属于离子化合物,其电子式为___________。
(2)写反应②的电极反应式:
阳极___________ ; 阴极___ 。
(3)反应③的化学方程式为___ 。
(4)这七种物质中含有共价键的有___________ (用化学式回答)。
查看习题详情和答案>>(08上海重点中学第二次联考)某校化学课外小组用硫酸铁废液(含少量硫酸铜和稀硫酸),制备硫酸亚铁晶体并进行如下实验。制备硫酸亚铁晶体主要的操作流程如下:
 |
请根据题目要求回答下列问题:
(1)A的化学式为 ,上述操作过程中用到的玻璃仪器有:①烧杯、
②玻璃棒、③酒精灯、④温度计、⑤ 。
(2)趁热过滤的目的是 。
(3)结晶操作过程中应控制滤液酸性的原因是 。
(4)已知硫酸亚铁铵[(NH4)2Fe(SO4)2]比硫酸亚铁稳定,常用在分析化学中。硫酸亚铁铵可用硫酸铵和硫酸亚铁反应制得。实验室利用硫酸亚铁铵溶液和草酸溶液反应生成草酸亚铁沉淀来制备草酸亚铁。写出硫酸亚铁铵溶液与草酸溶液反应的离子方程式
________________________________________________ 。
(5)草酸亚铁晶体(相对分子质量180)受热易分解,某课外小组设计如图的实验装置来检验其分解产物。
 ①该装置中最不合理的部分 (填字母),原因是 。
①该装置中最不合理的部分 (填字母),原因是 。
②改用正确装置实验开始后,B处变蓝,说明草酸亚铁晶体中有 ;C处有白色沉淀,E处部分黑色粉末变为红色,说明草酸亚铁分解产生 (填化学式)。
查看习题详情和答案>>(2010·武汉部分重点中学联考)已知NaHSO4在水中的电离方程式为:NaHSO4===Na++H++SO42-。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH=2。对于该溶液,下列叙述中不正确的是( )
A.该溶液的温度高于25℃
B.由水电离出来的c(H+)=1×10-10mol·L-1
C.c(H+)=c(OH-)+c(SO42-)
D.该温度下加入等体积pH=12的NaOH溶液可使反应后的溶液恰好呈中性
查看习题详情和答案>>
[2012·江西省重点中学协作体高三第二次联考] X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g/L;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是 ( )
A.原子半径:W>Z>Y>X>M
B.XZ2、X2M2、W2Z2均为直线型的共价化合物
C.由X元素形成的单质不一定是原子晶体
D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键
查看习题详情和答案>>
[2012·江西省重点中学协作体高三第二次联考]某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42-、NO3-、Cl-中的4种离子,所含离子的物质的量均为1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。下列说法不正确的是( )
A.若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g
B.若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色
C.若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色
D.该溶液中所含的离子是:Fe2+、Na+、SO42-、NO3-
查看习题详情和答案>>