摘要:6. B 点拨:根据化合价升降规律确定(1)Cl-<G<Q, G<Y<Q,(4)Q<Z<X.
网址:http://m.1010jiajiao.com/timu_id_4205895[举报]
A、B、C、D是原子序数依次增大的四种短周期元素。请根据表中信息回答下列问题。
| 元素 | A | B | C | D |
| 性质或结构信息 | 与同主族元素原子序数相差2 | 原子的最外层电子排布式为nsnnp2n-1 | 原子序数是A、B两元素原子序数之和的2倍 | 原子半径在所属周期中最小 |
(1)写出B原子的最外层轨道排布式______________________。
(2) A与B的单质可化合生成M,A与D的单质可化合生成N,M的空间构型为_____________。M与N可以在空气中化合生成E,E的电子式为____________________,写出在E溶于水所得的溶液中各离子浓度由大到小的顺序________________________。
(3)C的单质在空气中燃烧可生成气体F,写出F与A、C形成的化合物反应的方程式,并标出电子转移的方向和数目 _ ,F与A、B、D单质中的一种在溶液中充分反应可生成两种酸,写出该反应的离子方程式 。
查看习题详情和答案>> 如图所示,弹簧秤下挂着一重物A,烧杯中盛有溶液B,试根据要求回答下列问题:
如图所示,弹簧秤下挂着一重物A,烧杯中盛有溶液B,试根据要求回答下列问题:(1)若A为铝块,B为稀硫酸,将A放入B中,过一会儿,弹簧秤的读数将
(2)若A为铁块,B为硫酸铜溶液,将A放入B中,过一会儿,弹簧秤的读数将
目前,全球有16亿人有不同程度的缺碘现象,其中包括6亿儿童,科研表明,人的一生只要能摄入一小茶匙的碘就能正常发育,健康生活.目前预防缺碘的有效办法是食用含碘食盐.这种食盐含( )
查看习题详情和答案>>
A、B、C、D、E是中学化学常见单质,构成它们的元素的原子序数分别为a、b、c、d、е;且3(a+b)=2(a+c)=3(d-a);X、Y、Z、M、N、W、H、K是常见化合物,X是B和C的化合产物,它们之间有如下转化关系(图中反应物和产物中的H2O已略去):
(1)Y的电子式为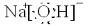
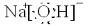 ,构成E单质的元素的原子结构示意图为:
,构成E单质的元素的原子结构示意图为: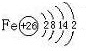
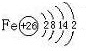 .
.
(2)反应③的离子方程式为
(3)E的氧化物与D在一定条件下反应的化学方程式为:
(4)已知常温下,1gA的单质与C的单质在点燃条件下完全反应,放出的热量为92.3kJ,写出W分解生成A和C的热化学方程式
(5)用离子方程式表示Z溶液显碱性的原因:
(6)固体N常温下即挥发,183℃升华,几乎溶于所有的有机溶剂和H2O中,据此判断N为
(7)25℃时,PH=5的W和N的水溶液中由H2O电离出来的H+离子浓度之比为
查看习题详情和答案>>

(1)Y的电子式为
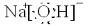
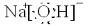
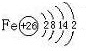
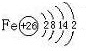
(2)反应③的离子方程式为
Al3++3AlO2-+6H2O=4Al(OH)3↓
Al3++3AlO2-+6H2O=4Al(OH)3↓
.(3)E的氧化物与D在一定条件下反应的化学方程式为:
Fe2O3+2Al
2Fe+Al2O3
| ||
Fe2O3+2Al
2Fe+Al2O3
,在实验室中,引发该反应的实验操作为
| ||
将铝粉与氧化铁粉末混合均匀,在混合物上方撒少量氯酸钾,插上一根镁条,并点燃镁条
将铝粉与氧化铁粉末混合均匀,在混合物上方撒少量氯酸钾,插上一根镁条,并点燃镁条
.(4)已知常温下,1gA的单质与C的单质在点燃条件下完全反应,放出的热量为92.3kJ,写出W分解生成A和C的热化学方程式
2HCl(g)═H2(g)+Cl2(g)△H=+184.6kJ/mol
2HCl(g)═H2(g)+Cl2(g)△H=+184.6kJ/mol
.(5)用离子方程式表示Z溶液显碱性的原因:
AlO2-+2H2O?Al(OH)3+OH-
AlO2-+2H2O?Al(OH)3+OH-
.(6)固体N常温下即挥发,183℃升华,几乎溶于所有的有机溶剂和H2O中,据此判断N为
分子
分子
晶体.(7)25℃时,PH=5的W和N的水溶液中由H2O电离出来的H+离子浓度之比为
1:104
1:104
.