摘要:(1)该氢氧化钠溶液的物质的量浓度为 .(2)在b点.c(Na+) c(CH3COO―) .(3)氢氧化钠溶液与醋酸溶液恰好完全反应的点位于曲线的 .A.a点 B.b点 C.d点 D.a.b间的某点 E.b.d间的某点(4)在d点.溶液中所有离子浓度由大到小的顺序为: .
网址:http://m.1010jiajiao.com/timu_id_420312[举报]
 为了测出某氢氧化钠溶液的物质的量浓度,某研究性学习小组先用广泛pH试纸测出该溶液的pH,发现该溶液的pH=14.于是他们用碱式滴定管量取25.00mL待测氢氧化钠溶液盛放在锥形瓶中,把0.1000mol/L的标准盐酸溶液注入50mL的酸式滴定管中,然后进行中和滴定操作.
为了测出某氢氧化钠溶液的物质的量浓度,某研究性学习小组先用广泛pH试纸测出该溶液的pH,发现该溶液的pH=14.于是他们用碱式滴定管量取25.00mL待测氢氧化钠溶液盛放在锥形瓶中,把0.1000mol/L的标准盐酸溶液注入50mL的酸式滴定管中,然后进行中和滴定操作.回答下列问题:
(1)用酚酞作指示剂,50.00mL标准盐酸溶液滴定完全后,锥形瓶内溶液颜色仍然呈红色,原因是
(2)为了继续完成该实验,他们取待测氢氧化钠溶液25mL稀释成250mL,然后再进行中和滴定.稀释该氢氧化钠溶液的玻璃仪器有
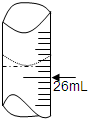
(3)用标准盐酸溶液滴定稀释后的碱溶液25.00mL,滴定前滴定管内液面读数为1.10mL,滴定后液面如图所示,则消耗标准溶液的体积为
(4)以下操作会导致结果偏高的是
A.待测碱溶液要空气中暴露时间较长B.未用标准液润洗酸式滴定管C.滴定终点读数时发现滴定管尖嘴处悬挂一滴溶液D.滴定终点读数时俯视滴定管的刻度,其他操作都正确
E.锥形瓶用蒸馏水润洗后再用待测液润洗.
 在25mL氢氧化钠溶液中逐滴加入0.2mol?L-1醋酸溶液,滴定曲线如图所示.
在25mL氢氧化钠溶液中逐滴加入0.2mol?L-1醋酸溶液,滴定曲线如图所示.(1)写出氢氧化钠溶液与醋酸溶液反应的离子方程式:
OH-+CH3COOH═CH3COO-+H2O
OH-+CH3COOH═CH3COO-+H2O
.(2)该氢氧化钠溶液的物质的量浓度为
0.1
0.1
mol?L-1.(3)在B点,a
>
>
12.5mL(填“>”、“<”或“=”,下同).若由体积相等的氢氧化钠和醋酸溶液混合而且恰好呈中性,则混合前c(NaOH)<
<
c(CH3COOH),混合前酸中c(H+)和碱中c(OH-)的关系:c(H+)<
<
c(OH-).(4)在D点,溶液中离子浓度大小关系为:
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
. 向20mL氢氧化钠溶液中逐滴加入0.2mol/L醋酸溶液,滴定曲线如图所示,下列说法不正确的是( )
向20mL氢氧化钠溶液中逐滴加入0.2mol/L醋酸溶液,滴定曲线如图所示,下列说法不正确的是( )