摘要:2.操作和现象向装有10mL红色品红溶液的试管中.通入SO2.直到溶液褪色.达到饱和为止.然后.在试管口套上一只小气球.用线扎紧.用酒精灯加热试管底部.溶液又渐渐变红.同时气球膨胀起来.撤去酒精灯.试试管冷却后.双手挤压气球.溶液颜色又渐渐退去.如此反复.用以向学生揭示温度.压力对气体溶解度的影响规律.此外.用气球还可演示气体密度的大小.例如.将H2.CO.O2分别充入三只气球内.扎好口后.让它们在空中自由升降.根据气球的沉浮.可说明H2.CO.O2的密度的相对大小.根据电子云的形状.晶体中原子的排特征.选用颜色.数量适当的气球.充气后.按需要连接.堆积.或用棉线对气球作变形处理.可制作出s.p.dxy.dxz.dyz.dz2.dx2-y2等电子云.sp3.sp2.sp等杂化轨道模型.金属晶体的各种堆积模型.模型轻巧.体积较大.立体感强.形象逼真.装置如图6和7所示
网址:http://m.1010jiajiao.com/timu_id_412500[举报]
(2012?河西区二模)某研究小组为探究铁和浓硫酸的反应,设计了如下图所示装置进行实验.请按要求回答下列问题:

(1)上图装置存在不足,请在图中C处画出所需装置并标注试剂名称
 .
.
(2)实验前要检查A、B装置的气密性,其操作为在接口E处接一导气管F,将F的末端浸入液面以下,
(3)为探究该反应产生的气体性质,将网个棉球上分别滴加少量试剂,按图示安好装置,加热试管A,观察四个棉球颜色变化情况,并记录,请填写下表空白:
(4)反应结束拆卸装置前,不需打开胶塞,就可使装置中残留的有毒气体完全吸收,应采取的操作足
(5)为探究试管A反应后的溶液中产物种类,小组同学提出3种假设,①只含有Fe3+②只含有Fe2+③既含有Fe3+又含有Fe2+,完成此探究实验所需试剂至少有
查看习题详情和答案>>

(1)上图装置存在不足,请在图中C处画出所需装置并标注试剂名称


(2)实验前要检查A、B装置的气密性,其操作为在接口E处接一导气管F,将F的末端浸入液面以下,
向A试管加水至玻璃管D末端浸入液面以下
向A试管加水至玻璃管D末端浸入液面以下
,安好装置,用酒精灯微热试管人,观察导气管F管口处有气泡冒出
导气管F管口处有气泡冒出
,停止加热,F中有一段液柱,证明该装置的气密性好.(3)为探究该反应产生的气体性质,将网个棉球上分别滴加少量试剂,按图示安好装置,加热试管A,观察四个棉球颜色变化情况,并记录,请填写下表空白:
| 棉球 | 棉球上滴加的试剂 | 实验现象 | 解释或结论 |
| i | 品红溶液 品红溶液 |
棉球变为白色,微热后又恢复红色 | |
| ii | FeCl3溶液 FeCl3溶液 |
棉球变为浅绿色 | 离子方程式: SO2+2Fe3++2H2O=2Fe3++SO42ˉ+4H+ SO2+2Fe3++2H2O=2Fe3++SO42ˉ+4H+ 结论: SO2有还原性 SO2有还原性 |
| iii | Na2S溶液 | 棉球变为浅黄色 | 解释:浅黄色物质是 S S 结论: SO2有氧化性 SO2有氧化性 |
| iv | 石蕊试液 石蕊试液 |
棉球变为红色 | 化学方程式: SO2+H2O?H2SO3 SO2+H2O?H2SO3 结论:该气体属于酸性氧化物 |
从D管口向试管A中鼓入足量空气
从D管口向试管A中鼓入足量空气
.(5)为探究试管A反应后的溶液中产物种类,小组同学提出3种假设,①只含有Fe3+②只含有Fe2+③既含有Fe3+又含有Fe2+,完成此探究实验所需试剂至少有
KSCN溶液和K3[Fe(CN)6]溶液或KSCN溶液和KMnO4溶液
KSCN溶液和K3[Fe(CN)6]溶液或KSCN溶液和KMnO4溶液
.(2012?南充模拟)硬质玻璃管是化学实验中经常使用的一种仪器,分析下列实验(固定装置略)并回答:
(1)进行微量实验:如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如下表.

 (2)如图所示,将硬质玻璃管改装为燃烧管.挤压软塑瓶壁,向装有固体B的锥形瓶中加入溶液A,同时往燃烧管中通入气体C并点燃,可看到明显的燃烧现象(金属网用以防止气体混合爆炸).
(2)如图所示,将硬质玻璃管改装为燃烧管.挤压软塑瓶壁,向装有固体B的锥形瓶中加入溶液A,同时往燃烧管中通入气体C并点燃,可看到明显的燃烧现象(金属网用以防止气体混合爆炸).
①用此装置模拟工业合成盐酸,则关于试剂选择正确的是
②若溶液A为饱和食盐水,气体C为氧气,燃烧管内观察到明亮火焰与浓烈的黑烟,则固体B为
查看习题详情和答案>>
(1)进行微量实验:如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如下表.

| 棉球 | 棉球上滴加试剂 | 实验现象 | 解释或结论 |
| a | 品红溶液 品红溶液 |
棉球变白,微热后又恢复红色 | 解释: SO2与品红反应生成无色不稳定物质,遇热分解又生成SO2和品红 SO2与品红反应生成无色不稳定物质,遇热分解又生成SO2和品红 结论:该气体具有漂白性. |
| b | 含酚酞的NaOH溶液 | 棉球变为白色 | 离子方程式: SO2+OH-=HSO3- SO2+OH-=HSO3- |
| c | 淀粉和 碘 碘 的混合溶液 |
棉球变为白色 | 化学方程式: SO2+I2+2H2O=H2SO4+2HI SO2+I2+2H2O=H2SO4+2HI 结论:该气体具有 还原 还原 性. |
 (2)如图所示,将硬质玻璃管改装为燃烧管.挤压软塑瓶壁,向装有固体B的锥形瓶中加入溶液A,同时往燃烧管中通入气体C并点燃,可看到明显的燃烧现象(金属网用以防止气体混合爆炸).
(2)如图所示,将硬质玻璃管改装为燃烧管.挤压软塑瓶壁,向装有固体B的锥形瓶中加入溶液A,同时往燃烧管中通入气体C并点燃,可看到明显的燃烧现象(金属网用以防止气体混合爆炸).①用此装置模拟工业合成盐酸,则关于试剂选择正确的是
d
d
(填序号),管口可观察到苍白
苍白
色火焰.| 溶液A | 固体B | 气体C | |
| a. | 稀硫酸 | Zn | Cl2 |
| b. | 浓盐酸 | MnO2 | H2 |
| c. | 稀硝酸 | Fe | Cl2 |
| d. | 浓盐酸 | KMnO4 | H2 |
CaC2
CaC2
(填化学式).此火焰温度极高,常用于切割焊接金属.资料显示:在煤中加入适量石灰石粉可使煤(含S)燃烧时产生的SO2转化成固体CaSO4,从而减少SO2排放,该方法被称为钙基固硫.这一过程是通过以下两步反应实现的:
㈠CaCO3
CaO+CO2 ㈡2CaO+2SO2+O2=2CaSO4
对此,某实验小组利用下列实验装置和药品对其可行性进行了模拟探究.

已知实验所用样品:Ⅰ---S粉与CaCO3粉末的混合物Ⅱ---CaSO4 粉末
(1)实验一:①取样品Ⅰ装入A中.连续通入过量O2,加热至500℃左右,充分反应发现,B中红色消失、C中出现大量白色浑浊.停止该步实验的正确操作是 .
②取反应后D中溶液滴加过量盐酸,无明显现象.由此得知实验一过程中:A中发生反应的化学方程式是 ;C中反应的离子方程式是 .
③要获得与以上实验事实相一致的结论,可替代B中品红溶液的是 .
a.酚酞的NH3?H2O溶液 b.酸性KMnO4溶液
c.酚酞的NaHCO3溶液 d.Br2的CCl4溶液
(2)实验二:①取样品Ⅰ装入A中.连续通入过量O2,并迅速加热升温,控制在1000℃左右,充分反应.发现B中红色消失,C中出现白色浑浊.
②取反应后D中溶液滴加过量盐酸,出现大量无色气泡,反应的离子方程式是 .
③反应结束后,将A中余下固体溶入水中,取其上层清液,滴加BaCl2溶液,立即有白色沉淀出现.
由此得知实验二:A中发生的反应有 (填选“㈠”、“㈡”).
(3)实验三:取样品Ⅱ装入A中.连续通入过量O2,加热至1200℃左右,充分反应,B中红色消失,则A中发生反应的化学方程式是 .比较实验一、二、三可知,如用该方法固硫,可行的基本条件是 .
(4)在中学化学实验室里,装置A通常只能选 为材料制作的玻璃管,但这种选择有一点不妥,其理由用化学方程式解释是: .
(5)实验所需O2若改由空气提供,且对上述实验探究事实不产生影响,应在A前添加一装有某药品的装置.请将该药品和装置图示在图中的虚线框内 .
查看习题详情和答案>>
㈠CaCO3
| ||
对此,某实验小组利用下列实验装置和药品对其可行性进行了模拟探究.

已知实验所用样品:Ⅰ---S粉与CaCO3粉末的混合物Ⅱ---CaSO4 粉末
(1)实验一:①取样品Ⅰ装入A中.连续通入过量O2,加热至500℃左右,充分反应发现,B中红色消失、C中出现大量白色浑浊.停止该步实验的正确操作是
②取反应后D中溶液滴加过量盐酸,无明显现象.由此得知实验一过程中:A中发生反应的化学方程式是
③要获得与以上实验事实相一致的结论,可替代B中品红溶液的是
a.酚酞的NH3?H2O溶液 b.酸性KMnO4溶液
c.酚酞的NaHCO3溶液 d.Br2的CCl4溶液
(2)实验二:①取样品Ⅰ装入A中.连续通入过量O2,并迅速加热升温,控制在1000℃左右,充分反应.发现B中红色消失,C中出现白色浑浊.
②取反应后D中溶液滴加过量盐酸,出现大量无色气泡,反应的离子方程式是
③反应结束后,将A中余下固体溶入水中,取其上层清液,滴加BaCl2溶液,立即有白色沉淀出现.
由此得知实验二:A中发生的反应有
(3)实验三:取样品Ⅱ装入A中.连续通入过量O2,加热至1200℃左右,充分反应,B中红色消失,则A中发生反应的化学方程式是
(4)在中学化学实验室里,装置A通常只能选
(5)实验所需O2若改由空气提供,且对上述实验探究事实不产生影响,应在A前添加一装有某药品的装置.请将该药品和装置图示在图中的虚线框内
二氧化硫是污染大气形成酸雨的主要有害物质之一,如果了解二氧化硫的性质,它在我们的生活中也有广泛的用途.
(1)下列可产生二氧化硫污染大气的是 .(填序号).
A.含硫矿石的冶炼 B.大量化石燃料的燃烧
C.大量烟花爆竹的燃放 D.硫酸厂排放的工业尾气
(2)某课外小组采集了一份雨水样品,每隔一段时间测定该雨水样品的pH变化数据如下
分析雨水样品pH变化的原因(用文字和化学方程式说明) .
(3)某实验小组欲探究二氧化硫的化学性质,设计如下实验,请完成实验报告.
(4)目前通常采用滴定法测定食品中残留二氧化硫的含量.具体实验方法主要是:样品经处理后,加入氢氧化钾使残留的二氧化硫以亚硫酸盐的形式固定,再加入硫酸使二氧化硫游离,用碘标准溶液滴定二氧化硫.在滴定时用 (填名称)作指示剂,滴定终点的现象是 .
查看习题详情和答案>>
(1)下列可产生二氧化硫污染大气的是
A.含硫矿石的冶炼 B.大量化石燃料的燃烧
C.大量烟花爆竹的燃放 D.硫酸厂排放的工业尾气
(2)某课外小组采集了一份雨水样品,每隔一段时间测定该雨水样品的pH变化数据如下
| 测试时间段 | 0 | 1 | 2 | 3 | 4 |
| 雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
(3)某实验小组欲探究二氧化硫的化学性质,设计如下实验,请完成实验报告.
| 序号 | 二氧化硫的性质 | 主要操作和现象 | 化学方程式 |
| ① | 将二氧化硫通入装有品红溶液的试管中,品红由红色变为无色 | ||
| ② | 氧化性 | ||
| ③ | 将二氧化硫通入装有新制氯水的试管中,氯水由浅黄绿色变为无色 |
一次性筷子、一次性饭盒的安全受到社会的关注.专家介绍说,正规的一次性筷子所用的
原料都是质地较好的木材,不用特殊加工.但是很多小作坊为了降低成本,使用劣质木材,为筷子看上去
白一些,他们常用硫磺进行熏蒸漂白,结果造成二氧化硫严重超标,同时硫磺中含铅、汞等重金属,也会
对人体造成铅中毒或汞中毒.
(1)“硫磺熏蒸”是应用二氧化硫的漂白性质,写出硫磺燃烧的化学方程式
(2)防止、减小毒筷“中毒”最简单的方法是用凉水清洗筷子表面,减少二氧化硫的含量.为研究SO2的溶解性质,某学生做如下实验:如右图,集气瓶中收集的是SO2,瓶塞系着瘪气球,向瓶中滴加紫色石蕊试液,实验现象是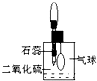 生取出瓶中溶液,将其滴入品红溶液,充分振荡,实验现象为
生取出瓶中溶液,将其滴入品红溶液,充分振荡,实验现象为
(3)在制一次性筷子时有“抛光”程序:加入滑石粉和木签一起搅拌,起到干燥、打磨的作用,使筷子变得光滑,以免毛疵划人的口腔.已知滑石粉是一种含水的具有层状结构的硅酸盐矿物.其质量组成为MgO 31.88%,SiO263.37%,H2O 4.75%,其化学式为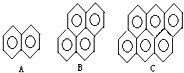
(4)有的厂家用石蜡代替“滑石粉抛光”,石蜡是含碳原子数(C20~C30)较多的稠环芳香烃,常温下为固体,温度高时熔化后可随食物进入人体致使慢性中毒.有如右的一系列物质,则A的分子式为
查看习题详情和答案>>
原料都是质地较好的木材,不用特殊加工.但是很多小作坊为了降低成本,使用劣质木材,为筷子看上去
白一些,他们常用硫磺进行熏蒸漂白,结果造成二氧化硫严重超标,同时硫磺中含铅、汞等重金属,也会
对人体造成铅中毒或汞中毒.
(1)“硫磺熏蒸”是应用二氧化硫的漂白性质,写出硫磺燃烧的化学方程式
S+O2
SO2
| ||
S+O2
SO2
| ||
(2)防止、减小毒筷“中毒”最简单的方法是用凉水清洗筷子表面,减少二氧化硫的含量.为研究SO2的溶解性质,某学生做如下实验:如右图,集气瓶中收集的是SO2,瓶塞系着瘪气球,向瓶中滴加紫色石蕊试液,实验现象是
紫色石蕊试液变红、气球鼓胀起来
紫色石蕊试液变红、气球鼓胀起来
;为比较SO2 和CO2溶解性的大小,某学生采取同样的装置和操作,能说明SO2在水中的溶解性大于CO2在水中溶解性的实验现象是SO2溶解时气球鼓胀的程度大于CO2溶解时气球的鼓胀程度
SO2溶解时气球鼓胀的程度大于CO2溶解时气球的鼓胀程度
.某学 生取出瓶中溶液,将其滴入品红溶液,充分振荡,实验现象为
生取出瓶中溶液,将其滴入品红溶液,充分振荡,实验现象为品红溶液的红色褪去(品红、SO2结合成不稳定的化合物),溶液显浅紫色(石蕊的颜色)
品红溶液的红色褪去(品红、SO2结合成不稳定的化合物),溶液显浅紫色(石蕊的颜色)
,接着向溶液中加入足量氯水,实验现象为 先变红后褪色(足量氯水能氧化SO2、石蕊和品红试液)
先变红后褪色(足量氯水能氧化SO2、石蕊和品红试液)
,再滴加BaCl2溶液,实验现象为生成白色沉淀(BaSO4)
生成白色沉淀(BaSO4)
.(3)在制一次性筷子时有“抛光”程序:加入滑石粉和木签一起搅拌,起到干燥、打磨的作用,使筷子变得光滑,以免毛疵划人的口腔.已知滑石粉是一种含水的具有层状结构的硅酸盐矿物.其质量组成为MgO 31.88%,SiO263.37%,H2O 4.75%,其化学式为
Mg3(Si4O10)(OH)2或3MgO?4SiO2?H2O
Mg3(Si4O10)(OH)2或3MgO?4SiO2?H2O
.
(4)有的厂家用石蜡代替“滑石粉抛光”,石蜡是含碳原子数(C20~C30)较多的稠环芳香烃,常温下为固体,温度高时熔化后可随食物进入人体致使慢性中毒.有如右的一系列物质,则A的分子式为
C10H8
C10H8
,A、B、C可以互称同系物吗?为什么?不能
不能
因为A、B、C相差n个C6H2,不是n个CH2
因为A、B、C相差n个C6H2,不是n个CH2
.该系列化合物里碳的最大质量分数为97.3%
97.3%
;若E是A的一个氢原子被羟基取代的产物,预测E可能具有哪些化学性质(至少举2条)E能与溴水发生取代反应、
E能与溴水发生取代反应、
E与FeCl3能发生显色反应、E能和碳酸钠溶液反应
E与FeCl3能发生显色反应、E能和碳酸钠溶液反应
.