网址:http://m.1010jiajiao.com/timu_id_409942[举报]
(1)该合成路线对于环境保护的价值在于
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂.用离子方程式表示乙醇胺水溶液呈弱碱性的原因:
(3)CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式:
(4)科学家发明了一种基于如图所示原理的廉价光电化学电池装置,写出光照时半导体电极表面发生的电极反应式
a.在自然界中存在大量的单质硅
b.硅可以通过化学方法“再生”
c.硅具有较强的亲氧性,燃烧放出的热量多
d.硅的化学性质不活泼,便于安全运输、贮存.
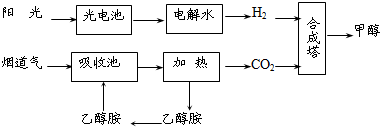
(11分)在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,其过程如下图所示,试回答下列问题:
 |
⑴ 该合成路线对于环境保护的价值在于 。
 ⑵ 15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂。
⑵ 15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂。
用离子方程式表示乙醇胺水溶液呈弱碱性的原
因: 。
⑶ CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=
-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化
学方程式: 。
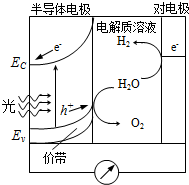
⑷ 科学家发明了一种基于右图所示原理的廉价光电化学电池
装置,写出光照时半导体电极表面发生的电极反应
式 。目前应用最多的半
导体材料是Si,甚至有人提出硅是“21世纪的能源”,硅可
作为新能源的原因可能的是 。
a.在自然界中存在大量的单质硅 b.硅可以通过化学方法“再生”
c.硅具有较强的亲氧性,燃烧放出的热量多 d.硅的化学性质不活泼,便于安全运输、贮存
查看习题详情和答案>>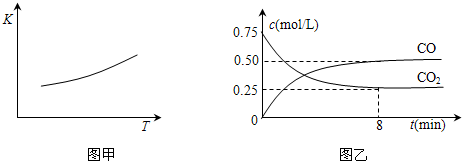
(1)该反应的平衡常数表达式K=
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图乙所示.
8分钟内,CO的平均反应速率v(CO)=
(3)下列措施中能使平衡时c(CO)/c(CO2)增大的是
A.升高温度 B.增大压强
C.充入一定量CO D.再加入一些铁粉
(4)铁的重要化合物高铁酸钠是一种新型饮用水消毒剂,具有氧化能力强、安全性好等优点.
①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O
| 电解 |
②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化纳和水,该反应的离子方程式为
一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)![]() FeO(s)+CO(g),已知该反应的平衡常数(K)与温度(T)的关系如图甲所示:
FeO(s)+CO(g),已知该反应的平衡常数(K)与温度(T)的关系如图甲所示:
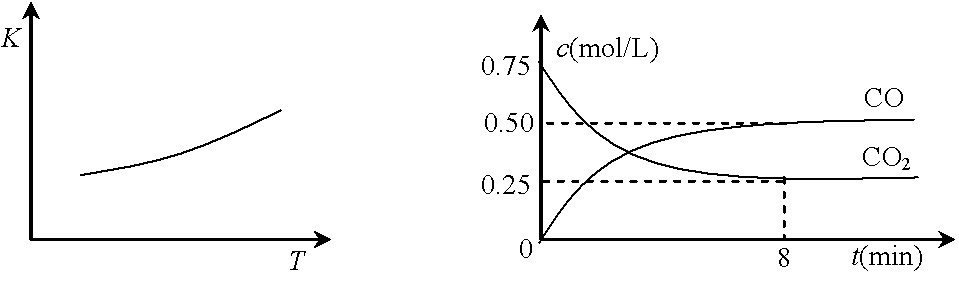
图甲 图乙
⑴该反应的平衡常数表达式K= ▲ 。
⑵一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图乙所示。
8分钟内,CO的平均反应速率v(CO)= ▲ mol/(L·min)。
⑶下列措施中能使平衡时c(CO)/c(CO2)增大的是 ▲ (填序号)。
A.升高温度 B.增大压强
C.充入一定量CO D.再加入一些铁粉
⑷铁的重要化合物高铁酸钠是一种新型饮用水消毒剂,具有氧化能力强、安全性好等优点。
①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O![]() Na2FeO4+3H2↑,则电解时阳极的电极反应式是 ▲ 。
Na2FeO4+3H2↑,则电解时阳极的电极反应式是 ▲ 。
②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化纳和水,该反应的离子方程式为 ▲ 。
查看习题详情和答案>>