摘要:化学研究小组的同学为了测定某铜矿中碱式碳酸铜[化学式为Cu2(OH)2CO3,相对分子质量为222]的质量分数.称取该铜矿样品30g.加入132.2g稀盐酸时恰好完全反应.共生成CO2气体4.4g.反应的化学方程式如下: Cu2(OH)2CO3+4HCl===2CuCl2+3H2O+CO2↑ 请你计算: (1) 铜矿样品中碱式碳酸铜的质量是多少克?其质量分数是多少? (2) 反应后所得溶液中溶质质量分数是多少? (假设铜矿中的杂质不与稀盐酸反应.也不溶于水)
网址:http://m.1010jiajiao.com/timu_id_4066779[举报]
某化学兴趣小组的同学对食品保鲜袋进行了如下研究.
【研究课题】食品保鲜袋的元素组成.
【查阅资料】碱石灰是由NaOH和CaO组成的吸湿剂;无水硫酸铜可作吸水剂,且吸水后由白色变为蓝色.
【提出猜想】保鲜袋可能由“碳、氢、氧”中的两种或三种元素组成.
【实验设计】小组同学设计了如下实验装置,利用燃烧法测定保鲜袋的元素组成.
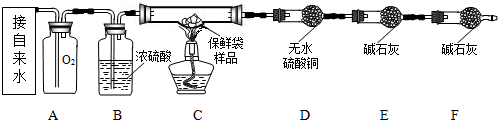
【实验步骤】
(1)按上图图示连接好仪器.
(2)检查装置的气密性.
(3)按图示装好药品和1.4g剪碎的保鲜袋样品,除D、E、F外将仪器按原图组装.
(4)向A中缓慢注水一段时间后,将已称重的D、E两干燥管和未称重的F干燥管接到C的尾端.
(5)点燃C处的酒精灯,直至保鲜袋子碎片完全燃烧.
(6)熄灭酒精灯并继续向A中注水一段时间.
(7)分别对D、E进行第2次称重.
【实验分析】
(1)B处的浓硫酸的作用是 .F处干燥管的作用是 .
(2)在点燃酒精灯前,要向A中缓慢注水一段时间是为了 .
(3)熄灭酒精灯后继续向A中注水一段时间是为了 .
(实验结论)第1次对D、E称重质量分别为54.2g、48.0g;第2次对D、E称重质量分别为56.0g、52.4g,则该食品保鲜袋的元素组成为 .
查看习题详情和答案>>
【研究课题】食品保鲜袋的元素组成.
【查阅资料】碱石灰是由NaOH和CaO组成的吸湿剂;无水硫酸铜可作吸水剂,且吸水后由白色变为蓝色.
【提出猜想】保鲜袋可能由“碳、氢、氧”中的两种或三种元素组成.
【实验设计】小组同学设计了如下实验装置,利用燃烧法测定保鲜袋的元素组成.

【实验步骤】
(1)按上图图示连接好仪器.
(2)检查装置的气密性.
(3)按图示装好药品和1.4g剪碎的保鲜袋样品,除D、E、F外将仪器按原图组装.
(4)向A中缓慢注水一段时间后,将已称重的D、E两干燥管和未称重的F干燥管接到C的尾端.
(5)点燃C处的酒精灯,直至保鲜袋子碎片完全燃烧.
(6)熄灭酒精灯并继续向A中注水一段时间.
(7)分别对D、E进行第2次称重.
【实验分析】
(1)B处的浓硫酸的作用是
(2)在点燃酒精灯前,要向A中缓慢注水一段时间是为了
(3)熄灭酒精灯后继续向A中注水一段时间是为了
(实验结论)第1次对D、E称重质量分别为54.2g、48.0g;第2次对D、E称重质量分别为56.0g、52.4g,则该食品保鲜袋的元素组成为
某化学兴趣小组的同学对食品保鲜袋进行了如下研究.
研究课题:食品保鲜袋的元素组成.
查阅资料:碱石灰是由NaOH和CaO组成的吸湿剂;无水硫酸铜可作吸水剂,且吸水后由白色变为蓝色.
提出猜想:保鲜袋可能由“碳、氢、氧”中的两种或三种元素组成.
实验设计:小组同学设计了如下实验装置,利用燃烧法测定保鲜袋的元素组成.

实验步骤
(1)按上图图示连接好仪器.
(2)检查装置的气密性.
(3)按图示装好药品和1.4g剪碎的保鲜袋样品,除D、E、F外将仪器按原图组装.
(4)向A中缓慢注水一段时间后,将已称重的D,E两干燥管和未称重的F干燥管接到C的尾端.
(5)点燃C处的酒精灯,直至保鲜袋子碎片完全燃烧.
(6)熄灭酒精灯并继续向A中注水一段时间.
(7)分别对D,E进行第2次称重.
实验分析
(1)B处的浓硫酸的作用是 .F处干燥管的作用是 .
(2)在点燃酒精灯前,要向A中缓慢注水一段时间是为了 .
(3)熄灭酒精灯后继续向A中注水一段时间是为了 .
实验结论:第1次对D,E称重质量分别为2克和3克;第2次对D,E称重质量分别为3.8克和7.4克,则该食品保鲜袋的元素组成为 .
查看习题详情和答案>>
研究课题:食品保鲜袋的元素组成.
查阅资料:碱石灰是由NaOH和CaO组成的吸湿剂;无水硫酸铜可作吸水剂,且吸水后由白色变为蓝色.
提出猜想:保鲜袋可能由“碳、氢、氧”中的两种或三种元素组成.
实验设计:小组同学设计了如下实验装置,利用燃烧法测定保鲜袋的元素组成.

实验步骤
(1)按上图图示连接好仪器.
(2)检查装置的气密性.
(3)按图示装好药品和1.4g剪碎的保鲜袋样品,除D、E、F外将仪器按原图组装.
(4)向A中缓慢注水一段时间后,将已称重的D,E两干燥管和未称重的F干燥管接到C的尾端.
(5)点燃C处的酒精灯,直至保鲜袋子碎片完全燃烧.
(6)熄灭酒精灯并继续向A中注水一段时间.
(7)分别对D,E进行第2次称重.
实验分析
(1)B处的浓硫酸的作用是
(2)在点燃酒精灯前,要向A中缓慢注水一段时间是为了
(3)熄灭酒精灯后继续向A中注水一段时间是为了
实验结论:第1次对D,E称重质量分别为2克和3克;第2次对D,E称重质量分别为3.8克和7.4克,则该食品保鲜袋的元素组成为
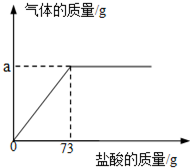 为了测定生铁中铁的质量分数,某校化学学习小组进行了实验研究,取6g生铁与溶质的质量分数为10%的盐酸反应(生铁中杂质不溶于水,也不与盐酸、硫酸铜溶液反应),并绘制了加入盐酸质量与放出气体质量的关系图.
为了测定生铁中铁的质量分数,某校化学学习小组进行了实验研究,取6g生铁与溶质的质量分数为10%的盐酸反应(生铁中杂质不溶于水,也不与盐酸、硫酸铜溶液反应),并绘制了加入盐酸质量与放出气体质量的关系图.(1)a=
(2)6g生铁与溶质的质量分数为10%的盐酸恰好完全反应时所得不饱和溶液中溶质的质量分数为多少?(保留一位小数)
(3)小华同学又设计了一个实验方案:另取6g该生铁粉末与溶质的质量分数为20%的硫酸铜溶液反应来测定生铁中铁的质量分数.当加入80g硫酸铜溶液时,所得固体的质量为

 为了测定生铁中铁的质量分数,某校化学学习小组进行了实验研究,取6g生铁与溶质的质量分数为10%的盐酸反应(生铁中杂质不溶于水,也不与盐酸、硫酸铜溶液反应),并绘制了加入盐酸质量与放出气体质量的关系图.
为了测定生铁中铁的质量分数,某校化学学习小组进行了实验研究,取6g生铁与溶质的质量分数为10%的盐酸反应(生铁中杂质不溶于水,也不与盐酸、硫酸铜溶液反应),并绘制了加入盐酸质量与放出气体质量的关系图.