摘要:C.粉末中一定不含有和
网址:http://m.1010jiajiao.com/timu_id_405506[举报]
生铁中含碳和硫等元素.化学兴趣小组对某生铁样品成分及其含量进行探究.
Ⅰ.生铁中碳和硫元素的定性检验
(1)将以下装置进行连接以完成实验(夹持仪器已略去,填接口字母代号)
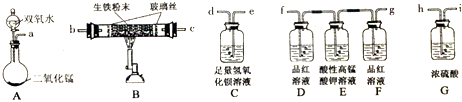
a→ → → → → → →
(2)将样品研磨成粉末的目的是 .
(3)确认样品中含有碳元素的现象是 .
Ⅱ.生铁中碳、硫质量分数的测定
(4)甲同学认为,以上装置可以粗略测定样品中碳的含量.称取样品m1g进行实验,充分反应后,测得C中生成的沉淀为m2g,该样品中碳的质量分数不小于 (用含m1、m2的式子表示)
(5)乙同学认为,待一定量样品充分反应后,向E装置中加入过量氯化钡溶液,根据沉淀质量可以计算样品中硫的质量分数,此方案是否合理? (填“是”或“否”);说明理由 .
(6)丙同学提议:为测定样品中硫的含量,可将c装置中试剂改为足量的30%双氧水,并按A→G→B→C装置连接进行实验,充分反应后,请你简述后续的实验方案 .
查看习题详情和答案>>
Ⅰ.生铁中碳和硫元素的定性检验
(1)将以下装置进行连接以完成实验(夹持仪器已略去,填接口字母代号)

a→
(2)将样品研磨成粉末的目的是
(3)确认样品中含有碳元素的现象是
Ⅱ.生铁中碳、硫质量分数的测定
(4)甲同学认为,以上装置可以粗略测定样品中碳的含量.称取样品m1g进行实验,充分反应后,测得C中生成的沉淀为m2g,该样品中碳的质量分数不小于
(5)乙同学认为,待一定量样品充分反应后,向E装置中加入过量氯化钡溶液,根据沉淀质量可以计算样品中硫的质量分数,此方案是否合理?
(6)丙同学提议:为测定样品中硫的含量,可将c装置中试剂改为足量的30%双氧水,并按A→G→B→C装置连接进行实验,充分反应后,请你简述后续的实验方案
A、B、C、D、E、F为短周期元素,A~F原子序数依次增大,质子数之和为56;B、C同周期;A与D、C与F同主族;A、C能形成两种液态化合物A2C和A2C2;E是地壳中含量最多的金属元素.试回答:
(1)F元素在周期表中的位置是 ;B单质的结构式为 .
(2)C、D元素形成的淡黄色粉末状物质D2C2,其含有的化学键类型为 .
(3)A、C两元素原子可形成一种10电子粒子X-.Y与X-具有相同的原子种类及数目,但Y不带电,是决定醇类物质化学性质的官能团,请写出Y的电子式: ,Y作为醇类物质官能团的名称是 .
(4)将F的低价氧化物通入其氢化物的水溶液中产生淡黄色沉淀,写出该反应的化学方程式为 .
(5)将D的单质投入A2C中,反应后得到一种无色溶液.E的单质能与该无色溶液反应,写出该反应的离子方程式 .
查看习题详情和答案>>
(1)F元素在周期表中的位置是
(2)C、D元素形成的淡黄色粉末状物质D2C2,其含有的化学键类型为
(3)A、C两元素原子可形成一种10电子粒子X-.Y与X-具有相同的原子种类及数目,但Y不带电,是决定醇类物质化学性质的官能团,请写出Y的电子式:
(4)将F的低价氧化物通入其氢化物的水溶液中产生淡黄色沉淀,写出该反应的化学方程式为
(5)将D的单质投入A2C中,反应后得到一种无色溶液.E的单质能与该无色溶液反应,写出该反应的离子方程式
有一固体粉末,可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3、K2SO4中的一种或几种,现按下列步骤进行实验。⑴将该粉末溶于水得无色溶液和白色沉淀;⑵在滤出的沉淀中加入稀硝酸,部分沉淀溶解,同时产生无色气体;⑶取滤液做焰色反应,可以看到黄色火焰,透过蓝色钴玻璃片,观察不到紫色火焰。由上述现象可推断:
A、可能有Na2CO3 B、一定有Na2SO4 C、一定无NaCl D、一定有K2SO4
查看习题详情和答案>>